
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Барометрическая формула. Распределение Больцмана. Закон равномерного распределения энергии по степеням свободы
|
|
|
|
1) 2) 3)
Распределение молекул по скоростям. Определение и свойства функции Максвелла. Наиболее вероятная скорость.
Скорости молекул газа имеют различные значения и направления, причем из-за огромного числа соударений, которые ежесекундно испытывает молекула, скорость ее постоянно изменяеться. Поэтому нельзя определить число молекул, которые обладают точно заданной скоростью v в данный момент времени, но можно подсчитать число молекул, скорости которых имеют значение, лежащие между некоторыми скоростями v1 и v2.
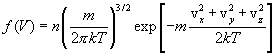 Согласно распределению Максвелла, вероятное число молекул в единице объема:
Согласно распределению Максвелла, вероятное число молекул в единице объема:
где m - масса молекулы, n — число молекул в единице объема. Отсюда следует, что число молекул, абсолютные значения скоростей которых лежат в интервале от v до v + dv, имеет вид:
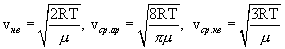
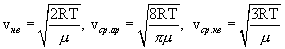
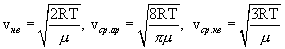
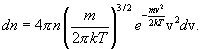
1) наиболее вероятная; 2)средняя арифметическая; 3) средняя квадратичная.
С повышением температуры наиболее вероятная скорость возрастает, поэтому максимум распределения молекул по скоростям сдвигается в сторону больших скоростей, а его абсолютная величина уменьшается. Следовательно, при нагревании газа доля молекул, обладающих малыми скоростями уменьшается, а доля молекул с большими скоростями увеличивается.
Барометрическая формула:
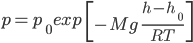 где p — давление газа в слое, расположенном на высоте h,
где p — давление газа в слое, расположенном на высоте h,
p0 — давление на нулевом уровне h = h0,
M — молярная масса газа,
R — газовая постоянная,
T — абсолютная температура.
В присутствии гравитационного поля (или, в общем случае, любого потенциального поля) на молекулы газа действует сила тяжести. В результате, концентрация молекул газа оказывается зависящей от высоты в соответствии с законом распределения Больцмана:
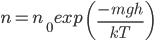 Где:
Где:
n — концентрация молекул на высоте h,
n0 — концентрация молекул на начальном уровне h = 0,
m — масса частиц,
g — ускорение свободного падения,
k — постоянная Больцмана,
T — температура.
В статистической физике выводится закон Больцмана о равномерном распределении энергии по степеням свободы молекул: для статистической системы, которая находится в состоянии термодинамического равновесия, на каждую поступательную и вращательную степени свободы приходится в среднем кинетическая энергия, равная 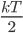 , а на каждую колебательную степень свободы — в среднем энергия, равная kT. Колебательная степень обладает вдвое большей энергией, т.к. на нее приходится как кинетическая энергия (как в случае поступательного и вращательного движений), так и потенциальная, причем средние значения потенциальной и кинетической и энергии одинаковы. Значит, средняя энергия молекулы:
, а на каждую колебательную степень свободы — в среднем энергия, равная kT. Колебательная степень обладает вдвое большей энергией, т.к. на нее приходится как кинетическая энергия (как в случае поступательного и вращательного движений), так и потенциальная, причем средние значения потенциальной и кинетической и энергии одинаковы. Значит, средняя энергия молекулы:
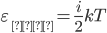 где i — сумма числа поступательных, числа вращательных в удвоенного числа колебательных степеней свободы молекулы: i = iпост. + iвращ. + 2iколеб.
где i — сумма числа поступательных, числа вращательных в удвоенного числа колебательных степеней свободы молекулы: i = iпост. + iвращ. + 2iколеб.
Закон равнораспределения показывает, что при тепловом равновесии, любая степень свободы (компоненты векторов положения или скорость частицы), которая появляется только как квадратичная функция в энергии, обладает средней энергией равной ½k в T и поэтому вносит вклад ½k в теплоёмкость системы.
Внутренняя энергия газа: определение и расчет. Теплота и работа. Первое начало термодинамики. Определение теплоемкости.
Внутренняя энергия — энергия тела, зависящая только от его внутреннего состояния. Понятие внутренней энергии объединяет все виды энергии тела, за исключением энергии его движения как целого и потенциальной энергии, которой тело может обладать, если оно находится в поле каких-нибудь сил (например, в поле сил тяготения).
Рассчитывается по формуле:
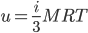 , где M — молярная масса.
, где M — молярная масса.
Тела могут быть нагреты не только в процессе теплообмена, но и в результате совершения над ними механической работы (трение, деформация). Оба указанных способа приводят к увеличению внутренней энергии тела. Об изменении внутренней энергии можно судить по изменению температуры тела.
|
|
|
|
|
Дата добавления: 2014-12-25; Просмотров: 1251; Нарушение авторских прав?; Мы поможем в написании вашей работы!