
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Рівняння термодинамічного стану реальних ґазів
|
|
|
|
Для опису термодинамічного стану реальних ґазів запропоновано понад 150 рівнянь.
- У першому наближенні одним із найпростіших рівнянь для помірного тиску і температури Т<Тк і Т≥Тк є рівняння Яна ван-дер-Ваальса (van-der-Waals), яке враховує дві складові відмінностей реального ґазу від ідеального:
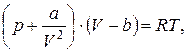 (3.72)
(3.72)
де Тк – критична температура реального ґазу;
 [Н/м2] – внутрішній (додатковий тиск);
[Н/м2] – внутрішній (додатковий тиск);
b – стала, що враховує власний об’єм молекул;
a – стала, що враховує силу взаємодії між молекулами.
- Рівняння Вукаловича-Новікова враховує всі три складові відмінностей реального ґазу від ідеального:

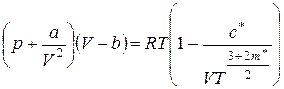 , (3.73)
, (3.73)
де сталі с*, m* враховують число неасоційованих молекул і подвійних асоціатів.
- Продуктивними рівняннями (особливо для високого тиску) є рівняння Бітті-Бриджмена:
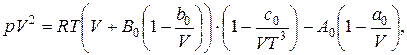 (3.74)
(3.74)
де B0, A0, a0, b0, c0 – емпіричні коефіцієнти, які залежать від природи ґазу;
та рівняння Боголюбова-Майєра:
 (3.75)
(3.75)
де Bi – виріальні коефіцієнти, які виражаються через потенціальну енергію взаємодії молекул певного ґазу і абсолютної температури;
і=2,3,4,.. – номер виріального коефіцієнта.
Часто в розрахунках обмежуються двома виріальними коефіцієнтами:
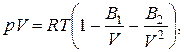 (3.76)
(3.76)
де B1, B2=f(T) – перший і другий виріальний коефіцієнт.
|
|
|
|
|
Дата добавления: 2014-12-25; Просмотров: 390; Нарушение авторских прав?; Мы поможем в написании вашей работы!