
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Принцип Паули. Принцип наименьшей энергии. Правило Гунда. Порядок заполнения атомных орбиталей электронами
|
|
|
|
Ответ: Принцип Паули (1925г.) В атоме не может быть 2-ух электронов – с одинаковыми значениями всех четырёх квантовых чисел. ИЛИ; Любые 2 (два) электрона в атоме – должны отличаться друг от друга – значением хотя бы одного квантового числа. ИЛИ: На орбитали может находиться – не более (менее) двух электронов, которые должны иметь – противоположные спины.  - “вакантная” орбиталь;
- “вакантная” орбиталь;  - “холостой” электрон;
- “холостой” электрон; 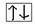 - “неподелённая” пара электрона;
- “неподелённая” пара электрона; 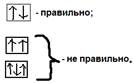 Следствия: 1)Максимальное число электронов на уровне – равно удвоенному квадрату главного квантового числа:
Следствия: 1)Максимальное число электронов на уровне – равно удвоенному квадрату главного квантового числа: 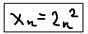 n=1; Xn=2; n=2; Xn=8; n=3; Xn=18. 2)Максимальное число электронов на подуровне – равно удвоенному числу значение магнитного квантового числа – для этого подуровня:
n=1; Xn=2; n=2; Xn=8; n=3; Xn=18. 2)Максимальное число электронов на подуровне – равно удвоенному числу значение магнитного квантового числа – для этого подуровня: 
 =0 (s-) – 2 электрона;
=0 (s-) – 2 электрона;  =1 (p-) – 6 электронов;
=1 (p-) – 6 электронов;  =2 (d-) – 10 электронов.
=2 (d-) – 10 электронов.
Принцип наименьшей энергии:  Правило Клечковского: 1)Первым заполняется тот подуровень – для которого сумма n+e меньше. Вопрос: Что сначала заполняется: 3d, или 4S? Решение: 3d: 3(n)+2(e)=5. 4s: 4(n)+0(e)=4. Ответ: сначала 4s, а затем 3d. 2)Если суммы n+e одинаковы, то первым заполняется тот подуровень – для которого n меньше. Что сначала заполняется: 5s, 3d, 4p? Решение: 5s: 5(n)+0(e)=5. 3d: 3(n)+2(e)=5. 4p:4(n)+1(e)=5. Ответ: сначала заполняется 3d, затем 4p, затем 5s.
Правило Клечковского: 1)Первым заполняется тот подуровень – для которого сумма n+e меньше. Вопрос: Что сначала заполняется: 3d, или 4S? Решение: 3d: 3(n)+2(e)=5. 4s: 4(n)+0(e)=4. Ответ: сначала 4s, а затем 3d. 2)Если суммы n+e одинаковы, то первым заполняется тот подуровень – для которого n меньше. Что сначала заполняется: 5s, 3d, 4p? Решение: 5s: 5(n)+0(e)=5. 3d: 3(n)+2(e)=5. 4p:4(n)+1(e)=5. Ответ: сначала заполняется 3d, затем 4p, затем 5s.
Правило Гунда:  Орбитали в пределах данного подуровня – заполняются сначала по одному электрону. Пример (похожее будет на зачёте): Охарактеризуйте четырьмя квантовыми числами – все восемь электронов:
Орбитали в пределах данного подуровня – заполняются сначала по одному электрону. Пример (похожее будет на зачёте): Охарактеризуйте четырьмя квантовыми числами – все восемь электронов: 
Порядок заполнения орбиталей электронами:  1s2|2s22p6|3s23p6|4s23d104p6|5s24d105p6|6s25d14f145d2-106p6|7s26d15f146d2-10…7p6|. Например: 25Mn 1s2|2s22p6|3s23p6|4s23d5| - тут числа которые сверху, над буквами слаживаются: 2+2+6+2+6+2+6=25. Потому какой подуровень заполняется последним электронами – различают: 1)s-элементы (красного цвета); p-элементы (оранжевого цвета); d-элементы (синего цвета); f-элементы (чёрного цвета) – эти цвета в таблице Менделеева справа-налево. 2)Перед s-, и p- элементами ставится: цифра=номер периода (N). Перед d-элементами ставится: номер периода(N)=-1. Перед f-элементами ставится: номер периода (N)=-2. Например: 42Mo 1s22s22p63s23p64s23d104p65s24d4 (это смотрится по таблице Менделеева).
1s2|2s22p6|3s23p6|4s23d104p6|5s24d105p6|6s25d14f145d2-106p6|7s26d15f146d2-10…7p6|. Например: 25Mn 1s2|2s22p6|3s23p6|4s23d5| - тут числа которые сверху, над буквами слаживаются: 2+2+6+2+6+2+6=25. Потому какой подуровень заполняется последним электронами – различают: 1)s-элементы (красного цвета); p-элементы (оранжевого цвета); d-элементы (синего цвета); f-элементы (чёрного цвета) – эти цвета в таблице Менделеева справа-налево. 2)Перед s-, и p- элементами ставится: цифра=номер периода (N). Перед d-элементами ставится: номер периода(N)=-1. Перед f-элементами ставится: номер периода (N)=-2. Например: 42Mo 1s22s22p63s23p64s23d104p65s24d4 (это смотрится по таблице Менделеева).
|
|
|
|
|
Дата добавления: 2015-04-24; Просмотров: 2309; Нарушение авторских прав?; Мы поможем в написании вашей работы!