
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Билет №12. Электролиз растворов и расплавов солей (на примере хлорида натрия).Практическое значение электролиза
|
|
|
|
Электролиз растворов и расплавов солей (на примере хлорида натрия).Практическое значение электролиза. Электролизом называются реакции в растворах или расплавах электролитов,происходящие под действием электрического тока. В расплавах или растворах происходит диссоциация электролита. Катионысмещаются к катоду, анионы — к аноду. Электролиз расплавов. На катоде происходит восстановление катионов, нааноде — окисление анионов.Электролиз расплава хлорида натрия. На катоде восстанавливаются катионы Na+ и выделяется металлический натрий, на аноде окисляются хлорид-ионы и выделяетсяхлор: 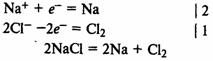 Электролиз водных растворов. В процессах на катоде и аноде могутучаствовать не только ионы электролита, но и молекулы воды.Будут ли на катоде восстанавливаться катионы металла или молекулы воды,зависит от положения металла в ряду напряжений металлов.
Электролиз водных растворов. В процессах на катоде и аноде могутучаствовать не только ионы электролита, но и молекулы воды.Будут ли на катоде восстанавливаться катионы металла или молекулы воды,зависит от положения металла в ряду напряжений металлов. 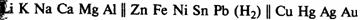 Если металл находится в ряду напряжений правее водорода, на катодевосстанавливаются катионы металла; если металл находится в ряду напряженийлевее водорода, на катоде восстанавливаются молекулы воды и выделяетсяводород. Наконец, в случае катионов металлов от цинка до свинца можетпроисходить либо выделение металла, либо выделение водорода, в зависимости отконцентрации раствора и других условий.На аноде также может происходить либо окисление анионов электролита, либоокисление молекул воды. При электролизе солей бескислородных кислот или самихкислот на аноде окисляются анионы (кроме F–.) В случаекислородсодержащих кислот на аноде окисляются молекулы воды и выделяетсякислород.Электролиз раствора хлорида натрия. На катоде восстанавливаются молекулы водыи выделяется водород, а на аноде окисляются хлорид-ионы и выделяется хлор:
Если металл находится в ряду напряжений правее водорода, на катодевосстанавливаются катионы металла; если металл находится в ряду напряженийлевее водорода, на катоде восстанавливаются молекулы воды и выделяетсяводород. Наконец, в случае катионов металлов от цинка до свинца можетпроисходить либо выделение металла, либо выделение водорода, в зависимости отконцентрации раствора и других условий.На аноде также может происходить либо окисление анионов электролита, либоокисление молекул воды. При электролизе солей бескислородных кислот или самихкислот на аноде окисляются анионы (кроме F–.) В случаекислородсодержащих кислот на аноде окисляются молекулы воды и выделяетсякислород.Электролиз раствора хлорида натрия. На катоде восстанавливаются молекулы водыи выделяется водород, а на аноде окисляются хлорид-ионы и выделяется хлор: 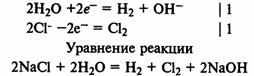 Электролиз раствора нитрата серебра. На катоде восстанавливаются катионы Ag+ и выделяется серебро, на аноде окисляются молекулы воды и выделяетсякислород:
Электролиз раствора нитрата серебра. На катоде восстанавливаются катионы Ag+ и выделяется серебро, на аноде окисляются молекулы воды и выделяетсякислород: 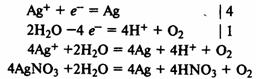 Применение. Электролиз расплавов используют для получения фтора, активныхметаллов (натрий, калий, магний, кальций, алюминий). Электролиз растворовиспользуют для получения хлора, щелочей, очистки металлов(электрорафинирование).
Применение. Электролиз расплавов используют для получения фтора, активныхметаллов (натрий, калий, магний, кальций, алюминий). Электролиз растворовиспользуют для получения хлора, щелочей, очистки металлов(электрорафинирование).
|
|
|
|
|
Дата добавления: 2015-04-24; Просмотров: 4699; Нарушение авторских прав?; Мы поможем в написании вашей работы!