
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Розпад гема
|
|
|
|
1. Розрив тетрапірольного кільця гему (у складі гемоглобіну) шляхом окислювального розщеплення метинового містка між І та II кільцями протопорфіринового циклу; в результаті реакції червоний пігмент еритроцитів гемоглобін перетворюється на зелений кров'яний пігмент вердоглобін (холеглобін). Реакція каталізується ферментом НАДФН-залежною гемоксигеназою і
супроводжується виділенням монооксиду вуглецю. Перетворення гемоглобіну на вердоглобін внаслідок окислення гему спричиняє послідовну зміну забарвлення в ділянках гематом, що утворюють "синці"
2. Розпад вердоглобіну з відщепленням білкової частини, вивільненням іона заліза та утворенням тетрапірольної молекули білівердину.
3. Перетворення білівердину на білірубін шляхом відновлення метинового зв'язку між піроламиIII, IV. Реакція каталізується ферментом НАДФН-залежною білівер- динредуктазою
4. Зазначені етапи утворення жовчних пігментів (1-3) відбуваються в клітинах ретикулоендотеліальної системи, з яких білірубін надходить у кров, де адсорбується молекулами сироваткового альбуміну. Комплекс "сироватковий альбумін - білірубін" транспортується в печінку, де пігмент поглинається гепатоцитами і підлягає подальшим перетворенням.
5. Білірубін є ліпідорозчинною речовиною і у високих концентраціях проявляє мембранотоксичність, особливо щодо клітин головного мозку. Детоксикація білірубіну, яка полягає в перетворенні пігменту у водорозчинну (і менш токсичну) форму - глю- куронід білірубіну, відбувається в мембранах ендоплазматичного ретикулуму гепатоцитів. У процесі взаємодії білірубіну з УДФ-глюкуроновою кислотою (УДФГК) утворюються моно- та диглюкуроніди білірубіну: Реакція каталізується УДФ-глюкуронілтрансферазою. Основна частина білірубіну екскретується в жовч у формі диглюкуронідів;
2. Паренхіматозна жовтяниця. Причини. Біохімічні показники
Печінкова {паренхіматозна) жовтяниця — розвивається внаслідок порушення
структури та ферментативних властивостей гепатоцитів в результаті дії пошкоджуючих
факторів вірусного, бактеріального, хімічного походження. значна гіпербілірубінемія
(збільшення концентрації загального білірубіну) Зростання в крові прямого білірубіну
3. Молекулярні механізми дії тиреоїдних гормонів.
Рецептори тиреоїдних гормонів локалізовані в ядрах клітин-мішеней. У взаємодії з гормонами беруть участь специфічні рецептори а-1 та Р-1, які є білками з м.м. 47 і 52 кДа, відповідно. Спорідненість цих рецепторів до Т3 значно більша, ніж до Т4. Молекули тиреоїдних рецепторів мають три структурних домени: N-термінальний домен; центральний ДНК-зв'язуючий домен з двома цинковими пальцями; С-термінальний домен, що сполучається з гормоном. Утворення комплексу гормон-рецептор призводить до конформаційних змін у молекулі рецептора; при цьому ДНК-зв'язуючий домен рецептора стає спроможним до взаємодії із специфічними сайтами на промоторах генів, які контролюють транскрипцію мРНК та синтез білків, що відповідають за прояви біологічних ефектів тиреоїдних гормонів.
4. Молекулярні механізми м’язового скорочення та розслаблення м’язів
м'язове скорочення, в основі якого лежить переміщення товстих і тонких філаментів, потребує участі АТФ; циклічне перетворення АТФ в АДФ є необхідною передумовою як скорочення, так і
розслаблення м'язів. Гідроліз АТФ до АДФ та Фн здійснюється завдяки АТФ-азній активності
глобулярних головок S1 міозину.
A. У м'язі, що перебуває в стані спокою, S1-головки міозину не сполучені з актиновими філамен-тами. Продукти гідролізу АТФ (АДФ та Фн) зв'язані з міозином.
B. При збудженні м'яза S1-головки зсуваються в напрямку тонких філаментів і сполучаються з
нитками актину (G-субодиницями). Фн вивільняється з комплексу з міозином.
C. Вивільнення АДФ з комплексу з міозином супроводжується конформаційним зсувом у
просторовому розташуванні головки S1, що зв'язана з актином (зміщенням кута між головкою і віссю міофібрили з 90° на 45°).
D. Взаємодія з актином молекули АТФ супроводжується розривом зв'язку між актином і міозином. S1-головка знову віддаляється від тонкого філамента.
E. АТФ, що вивільнився, гідролізується до АДФ та Фн, завдяки АТФ-азній активності вільних головок міозину. Продукти гідролізу знову сполучаються з міозином. Актинові та міозинові філамента готові до нового циклу взаємодії та пересування.
Головним біохімічним регулятором скорочення та розслаблення м'язів є зміни цитозольноїконцентрації іонів Са2+, яка у стані спокою (розслаблення) становить близько 10"8-10-7 моль/л. Поширення потенціалу дії з сарколеми на трубочки Т-системи, що контактують із мембранами саркоплазматичного ретикулуму, спричиняє вихід Са2+ з канальців СР, які відіграють роль депо Са2+ в міоцитах (у комплексі з білком секве-стрином). Внаслідок цих процесів концентрація Са2+ в саркоплазмі досягає 10~5 моль/л, що ініціює молекулярні процеси, які є м'язовим скороченням.
5. Нейромедіатори. Рецептори для нейромедіаторів та фізіологічно активних сполук
Нейромедіатори (нейротрансмітери) - біомолекули, які забезпечують передавання імпульсів (хімічних сигналів) у нервовій системі з одного нейрона на інший, а також з нейрона на ефекторний орган. За хімічною природою нейромедіатори поділяють на такі сполуки: ацетилхолін,
біогенні аміни (катехоламіни — норадреналін, дофамін, серотонін), амінокислоти та їх похідні (у-аміномасляна кислота - ГАМК, гліцин, глутамат, аспартат), пептиди - нейропептиди (ендорфіни, енкефаліни, сполука Р тощо). Медіаторні функції в нервовій системі можуть також виконувати пролін, таурин, (З-аланін, аденозин, простагландини. Рецептори нейромедіаторів - мембранні білки (здебільшого глікопротеїни), що локалізовані в постсинаптичних мембранах нейронів або плазматичних мембранах клітин ефекторних органів і здатні до зв'язування фізіологічних ефекторів (нейромедіаторів, різних ФАС, психотропних сполук) і передавання зовнішньоклітинного хімічного сигналу всередину нейрона. За принципами молекулярної організації та функціонування, рецептори нейромедіаторів - це здебільшого іонотропні рецептори (рецептори І класу), тобто такі, що контролюють відкриття іонних каналів на мембрані для Са2+, Na+ і К+; в ролі первинних ефекторів, що передають хімічний сигнал на нервову клітину, в цьому разі виступають компоненти іонних каналів (розділ 23). Крім того, у фізіологічних ефектах
деяких нейромедіаторів та нейромодуляторів (зокрема, нейропептидів головного мозку, ацетилхоліну та деяких біогенних амінів) беруть участь і метаботропні рецептори (рецептори II класу), які активують внутрішньоклітинні біохімічні системи шляхом утворення цАМФ або цГМФ, включенням фосфоінозитидної системи та/або збільшенням цитозольної концентрації іонів Са2+. Крім нейромедіаторів, із зазначеними типами рецепторів можуть взаємодіяти численні лікарські засоби, нейротоксини, що активують (агоністи), гальмують, блокують (антагоністи) або модулюють біохімічні, нейрофізіологічні та психологічні (поведінкові) ефекти, опосередковані
збудженням специфічних рецепторів певних зон головного мозку.
6. Білковосинтезуюча система. Особливості генетичного коду
Властивості генетичного коду:
(1) код є універсальним для всіх біологічних систем - вірусів, бактерій, вищих організмів;
(2) код є однонаправленим, тобто інформативним тільки в тому випадку, коли зчитується "зліва направо" (в напрямку 5'—»3');
(3) код є безперервним, тобто має лінійний безперервний порядок зчитування - між кодонами немає "розділових знаків";
(4) код є таким, що не перекривається - після зчитування інформації з одного триплета "рамка зчитування" переміщується вправо відразу на три нуклеотиди;
(5) код є "виродженим", тобто кожна амінокислота кодується не одним, а декількома кодонами.
що з 64 комбінацій нуклеотидів 61 кодон є змістовним, тобто таким, що визначає включення до складу білка певної амінокислоти, а 3 кодони - беззмістовними, тобто такими, що не кодують жодної з амінокислот. Ці нонсенс-кодони (UAA, UAG, UGA) виконують роль сигналів термінаціїтрансляції
генетичного (біологічного) коду, тобто сукупності знаків, символів та системи правил, алгоритмів,
'згідно з якими структурна інформація, що міститься в нуклеїнових кислотах, може бути трансформована у специфічну первинну структуру поліпептидів, яка, у свою чергу, визначає всі біологічні властивості білкових молекул.
Компонентами білоксинтезуючої системи, що реалізують процес трансляції в прокаріотичних та еукаріотичних клітинах, є:
рибосоми - рибонуклеопротеїдні структури з константами седиментації 70s та 80s у прокаріотів та еукаріотів (відповідно), що взаємодіють у процесі трансляції з іншими компонентами системи білкового синтезу; мРНК (іРНК) або інший матричний полірибонуклеотид, що програмує послідовність включення амінокислот у поліпептидний ланцюг згідно з інформацією, яка міститься в генетичній ДНК, тРНК, що виконують функцію адапторів у процесі
трансляції, взаємодіючи з кодонами мРНК та певними амінокислотами - близько 20 типів різнихтРНК, відповідно до кількості амінокислот, які вони акцептують, аміноацил-тРНК-синтетази (АРС-ази) - ферменти, що активують амінокислоти та сполучають амінокислотні залишки з З'-кінцями акцепторних гілок тРНК. АРС-ази є ферментами з високою специфічністю як відносно певної амінокислоти, так і тРНК, що їй відповідає; регуляторні білки - білкові фактори ініціації (IF), елонгації (EF) та термінації, або рилізинг-фактори (RF); білкові фактори еукаріотів мають позначення elF, eEF та eRF, відповідно; коферменти - ГТФ, АТФ.
Білет4.
1. Орнітиновий цикл сечоутворення.
Див.2-5
2. Обтураційна жовтяниця
Післяпечінкова (обтураційна) жовтяниця — спричиняється неможливістю надходження жовчі у дванадцятипалу кишку внаслідок закупорки жовчних шляхів. знебарвленням калових мас внаслідок відсутності в них стеркобіліногену та стеркобіліну ("ахолічний" кал) і цілковитою відсутністю уробіліну в сечі.
3. Білки плазми крові. Альбуміни. Глобуліни. Фібриноген.
Загальна концентрація білків плазми крові людини складає 65-85 г/л, ця величина може змінюватися в бік зменшення (гіпопротеїнемія) у людей старечого віку та за умов патологічних станів, що супроводжуються пригніченням білкового синтезу та активацією розпаду тканинних білків (голодування; виснажливі інфекційні хвороби; стан після тяжких травм, оперативних втручань; кахексія при злоякісних новоутвореннях). поділяються на п'ять фракцій: альбуміни
(сироваткові альбуміни), а1,-глобуліни, а2-глобуліни, в-глобуліни та, у-глобуліни.
Альбуміни (сироваткові альбуміни) - багатодисперсна фракція білків плазми, які характеризуються високою електрофоретичною рухомістю та легкою розчинністю у воді та сольових розчинах. Завдяки високій гідрофільності альбуміни зв'язують значну кількість води, і об'єм їх молекули при умовах гідратації збільшується вдвічі.
забезпечує до 70-80 % онкотичного тиску білків плазми крові, зменшення концентрації альбумінів сироватки, наприклад за умов порушення їх синтезу в гепатоцитах при печінковій недостатності, може спричиняти перехід води із судинного русла до тканин і розвиток онкотичних набряків. Транспортні білки
Глобуліни - гетерогенна фракція білків крові, що виконують транспортні
(а-глобуліни - транспорт ліпідів, тироксину, кортикостероїдних гормонів; а-глобуліни -
транспорт ліпідів, іонів міді; в-глобуліни - транспорт ліпідів, вільного та гемового заліза) та
захисні функції (участь в-глобулінів в імунних реакціях як антитоксинів; у-глобуліни як
фракція імуноглобулінів).
Фібриноген — безбарвний білок, розчинений в плазмі крові. При активації системи згортання крові фібриноген піддається ферментатівному розщеплюванню ферментом тромбіном із утворенням мономеру фібрину, який під дією активного XIII фактора згортання крові полімеризується і випадає в осад у вигляді білих ниток полімеру фібрину. Плазма крові без фібриногену називається сироваткою крові.
4. Біологічний ефект альдостерону.
альдостерон - мінералокортикоїд, фізіологічною функцією якого є стимуляція реабсорбції іонів натрію в дистальних сегментах ниркових канальців та збільшення виділення калію. Молекулярні механізми дії альдостерону полягають у стимуляції синтезу білків, які реалізують транспорт Na+ через мембрани чутливих клітин нефронів. Функціонування альдостеронового механізму тісно сполучене з ренін-ангіотензиновою системою;головний біохімічний ефект дії альдостерону полягає в стимуляції реабсорбції Na+(a разом з ним і СІ") у дистальній частині канальців нефронів.
5. Особливості метаболізму нервової тканини
Загальний хімічний склад головного мозку характеризється наявністю білків (близько 8 % загальної маси тканин), значною кількістю ліпідів (10-12 %), вуглеводів (близько 1 %), інших низькомолекулярних біомолекул, неорганічних солей і води (77-78 %). надзвичайно високому вмісті ліпідів різноманітної хімічної структури. Біоенергетика мозку характеризується значною залежністю від постачання киснем, який використовується переважно на аеробне окислення глюкози. Основним споживачем метаболічної енергії в головному мозку, що використовується у формі АТФ, є процес генерації нервового потенціалу на мембрані нейронів, який вимагає постійного функціонування натрієвого насоса - мембранної Na+, К+-АТФази. Головною особливістю енергетичного обміну головного мозку є значне переважання рівня використання глюкози над іншими субстратами енергетичного обміну. У тканині головного мозку в реакції гідролітичного дезамінування АМФ постійно утворюється вільний аміак, який знешкоджується шляхом взаємодії з глутаматом, утворюючи глутамін, що виходить у кров.
6. Значення обміну мінеральних солей.
Мінеральні солі – іони, створюють осмотичний тиск, що є основною рушійною силою в русі води в організмі. При накопиченні іонів натрію в організмі розвиваються набряки, при його надлишковому виведені – міжклітинна дегідратація.
Білет 5
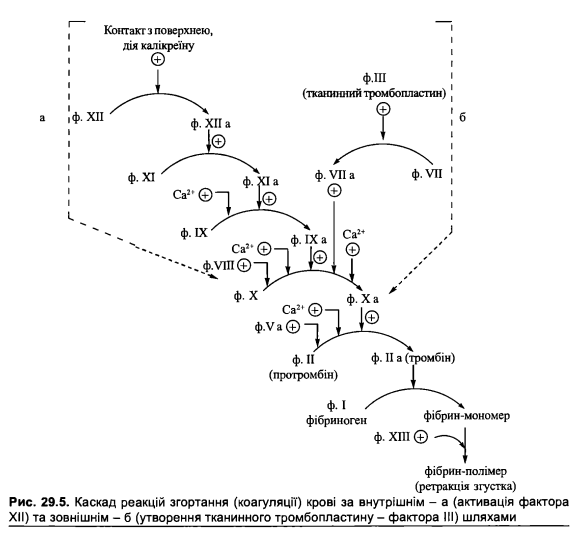
1. Механізм активації й функціонування каскадної системи згортання крові.
|
|
|
|
|
Дата добавления: 2015-05-08; Просмотров: 1073; Нарушение авторских прав?; Мы поможем в написании вашей работы!