
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Лабораторна робота №1 3 страница
|
|
|
|
СН3 - NH2 + H+Cl- ® [CH3-NH3]+Cl-
сіль
хлорид метиламонію
СН3 - NH2 + H+OH- ® [CH3 - NH3]+OH-
гидроксид метиламонію
Деякі аміни можуть вміщати в молекулі декілька аміногруп. Тоді назва такої сполуки складається за принципами міжнародної номенклатури: 1 2 3 4 5
CH2 - CH2 - CH - СH2 - CH3
ï ï
NH2 NH2 1,3 - диамінопентан
Відомі ароматичні аміни. Це похідні ароматичних вуглеводнів, де біля ароматичного кільця знаходяться аміногрупи (одна або декілька): 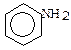 амінобензол (анілін). Ароматичні аміни також розглядають як первинні, вторинні, третинні. Властивості аналізуються за аміногрупою і за ароматичним циклом. Ароматичні аміни - слабкі основи. Послаблення основних властивостей викликає наявність ароматичного ядра. Треба звернути увагу на особливості властивостей первинних ароматичних амінів. За аміногрупою (-NH2) вони дають солі при взаємодії з кислотами. Вони здатні реагувати з азотистою кислотою з утворенням солей діазонію. Солі діазонію використовуються для одержання різних класів сполук і в тому числі азофарбників. Можна виділити такі стадії одержання азофарбника:
амінобензол (анілін). Ароматичні аміни також розглядають як первинні, вторинні, третинні. Властивості аналізуються за аміногрупою і за ароматичним циклом. Ароматичні аміни - слабкі основи. Послаблення основних властивостей викликає наявність ароматичного ядра. Треба звернути увагу на особливості властивостей первинних ароматичних амінів. За аміногрупою (-NH2) вони дають солі при взаємодії з кислотами. Вони здатні реагувати з азотистою кислотою з утворенням солей діазонію. Солі діазонію використовуються для одержання різних класів сполук і в тому числі азофарбників. Можна виділити такі стадії одержання азофарбника:
а) одержання солі:
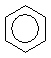 -NH2 + Н+С1- ® [
-NH2 + Н+С1- ® [  -NH3]+С1
-NH3]+С1
анілін хлорид феніламонію (сіль)
б) реакція діазотування (взаємодія солі з азотистою кислотою). Одержання солі діазонію:
[  -NH3]+С1-
-NH3]+С1- 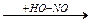 [
[  -NºN]С1-
-NºN]С1-
сіль діазонію
в) реакція азосполучення - це взаємодія солей діазонію з окси- або амінопохідними ароматичних сполук. Сіль діазонію називають діазоскладаючою, а окси- або амінопохідні називають азоскладаючою. Сполучення діазоскладаючої з азоскладаючою проходить за рахунок відщеплення водню в пара- або орто-положенні азоскладаючої:
[ 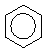 -NºN]С1- +Н
-NºN]С1- +Н  -ОН
-ОН 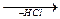
 -N=N-
-N=N-  -OH
-OH
оксіазосполука -N=N- - азогрупа.
Тема: Амінокислоти
Амінокислотами називають похідні органічних кислот, де в радикалі може бути одна або декілька аміногруп. По положенню аміногрупи амінокислоти розподіляють на a, b, g...Амінокислоти називають, беручи за основу назву кислоти з додатком -аміно. Багато амінокислот називають за тривіальною номенклатурою.
CH2 - CООH;
ï
NH2 амінооцтова кислота, гліцин
a b
CH3 - CH - CООH; СH2 - CH2 - CООH;
ï ï
NH2 NH2
a-амінопропіонова кислота, аланін b-амінопропіонова кислота
Амінокислоти містять дві функціональні групи за протилежними властивостями (кислотні і основні). Тому вони проявляють амфотерні властивості, реагуючи з кислотами і основами, утворюючи солі:
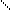

|
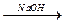 CH2 - C = О
CH2 - C = О
ï ОН ï O-Na
NH2 NH2
|

 CH2 - C = О ¾¾® [ CH2 - C = О ] +Cl-
CH2 - C = О ¾¾® [ CH2 - C = О ] +Cl-
ï О-Н ï OH
:NH2 NH3 сіль
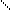 Амінокислоти проявляють типові властивості по карбоксильній групі (-C = О) та по аміногрупі (-NH2; -NH-; -N-).
Амінокислоти проявляють типові властивості по карбоксильній групі (-C = О) та по аміногрупі (-NH2; -NH-; -N-).
 ОН
ОН
Велике значення a-амінокислот, так як з них збудовані молекули білків.
Прикладами a- амінокислот є:
CH2 - CООH; CH3 - CH - CООH; CH2 - CH - CООH;
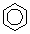 ï ï ï ï
ï ï ï ï
NH2 NH2 NH2
гліцин аланін фенілаланін
CООH; CООH;
ï ï
NH2-C-H NH2-C-H
ï ï
(CH2)3 CH2
ï ï
CH2 CH2
ï ï
NH2 S
ï
лізин CH3 метіонін
a-амінокислоти при певних умовах можуть реагувати між собою, утворюючи сполуки з пептидними зв’язками:


 CH2-C=О + CH3-CН-С=О + CH2-C=О...
CH2-C=О + CH3-CН-С=О + CH2-C=О... 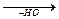
ï О-Н ï OH ï OH
NH2 NH2 NH2
О О
úç úç
 ®CH2-C-NH-CH-C-NH-CH2-C=О -C-NH- пептидний зв’язок.
®CH2-C-NH-CH-C-NH-CH2-C=О -C-NH- пептидний зв’язок.
ï ï OH úç
NH2 NH2 О
Тема: Білки
Природні високомолекулярні сполуки синтезовані з a-амінокислот. Білки виконують різні функції. Це ферменти, гормони, антибіотики. Вони входять до складу тваринних і рослинних організмів. Білкові речовини - найважливіша складова частина їжі людини і тварини. Білки містять вуглець, водень, кисень, сірку, фосфор і азот. По кількості визначеного азоту можна зробити висновок про кількість білку у цьому зразку.
Численні досліди встановили, що в молекулах білків залишки амінокислот зв’язані пептидними зв’язками -С - NH -.
úç
О
У будові молекул білків виділяють чотири структури. Деякі білки характеризуються трьома структурами. Первинна структура - певний порядок сполучення залишків a -амінокислот. Основний міжатомний тип зв’язку - пептидний. Вторинна структура - розміщення поліпептидного ланцюга в просторі у вигляді спіралі. Міжатомний тип зв’язку - водневий.
-C-NH-
úç
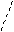 O
O
-NH-C-
úç
O
Третинна структура - утворення певної форми білкової молекули за рахунок взаємодії певних функціональних груп амінокислот між собою. Можна умовно виділити глобулярну і фібрилярну форму білкової молекули. Четвертинна структура - об’єднання кількох структур, які мають первинну, вторинну і третинну будову в більш складні молекули.
Білки мають специфічні фізичні і хімічні властивості. Слід звернути увагу на відношення білків до розчинників, на зворотне і незворотне осадження, на денатурацію білків, гідроліз, кольорові реакції, амфотерний характер, ізоелектричний стан, ізоелектричну точку, методи розділу суміші білків і їх очищення.
Для формування системи знань слід звернути увагу на класифікацію білків, на групи білків-протеїнів і протеїдів.
Правила техніки безпеки у лабораторії органічної хімії та надання першої допомоги (загальні правила)
1. Робота у лабораторії органічної хімії повинна вестись з точним дотриманням усіх правил і запобіжних заходів, зазначених у прописах дослідів і синтезів.
2. Приступаючи до виконання роботи, варто ознайомитись з властивостями застосовуваних речовин(токсичність, вогненебезпечність).
3. Перед тим, як зважити або відміряти речовину для синтезу, треба уважно прочитати напис на етикетці.
4. Органічні речовини не можна брати руками, тому що внаслідок усмоктування їх шкірою можливо отруєння. Багато органічних речовин викликають сильне подразнення шкіри.
5. Прилади для проведення реакцій нагрівання розчинів і перегонки ні в якому разі не можна збирати наглухо закритими, щоб уникнути вибуху.
6. Не можна близько нахилятися до приладу, у якому йде реакція, нагрівання або перемішування якоїсь речовини.
7. При нагріванні речовин у пробірці не можна тримати її отвором до себе або вбік стоячого поруч товариша.
8. Треба обережно, остерігаючись поранень, працювати зі скляним посудом. Вставляючи скляні трубки в канали пробок, необхідно попередньо оплавити їх кінці і змазати канали пробок гліцерином; вставляти скляну трубку треба поступально-обертальним рухом. При вставлені пробок у колбу варто тримати її пальцями за горло й уникати надмірного зусилля, що може призвести до поломки скла.
9. При роботі у лабораторії слід особливо берегти очі:
а) при визначенні температури плавлення в приладі із сірчаною кислотою;
б) при тих роботах, коли є небезпека розбризкування і розкидання їдких речовин (перемішування кислот і лугів, роздрібнення твердого лугу, цинку хлориду, сплавлення і т.д.);
в) при перегонці у вакуумі;
г) при роботах із металевим натрієм;
д) при виготовленні скляних капілярів.
10. Варто дотримуватись великої обережності при роботі з вогненебезпечними розчинниками (етиловий ефір, бензол, петролейний ефір, бензин, сірковуглець, спирт, ацетон та ін.). Роботу з ними необхідно вести тільки вдалині від вогню, користуючись водяними електричними банями. При перегонці необхідно застосовувати холодильник із водяним охолодженням.
11. Робота з отруйними речовинами, що подразнюють органи дихання, сильно пахнуть, повинна проводитись тільки у витяжній шафі та із застосуванням гумових рукавичок.
12. При роботі з бромом не можна вдихати його пари; при цьому особливо потрібно берегти очі.
13. Концентровані сульфатну й нітратну кислоти варто переливати тільки у витяжній шафі. При розведенні кислоти необхідно обережно невеличкими порціями при перемішуванні додавати кислоту до води.
14. Категорично забороняється затягувати ротом у піпетки органічні речовини та їх розчини.
15. Обов’язок кожного працюючого в лабораторії – берегти й акуратно поводитись із посудом, приладами і предметами обладнання.
16. Не можна переносити з однієї лабораторії в другу прилади і реактиви без дозволу лаборанта або викладача.
17. Категорично забороняється виливати в раковини концентровані розчини кислот і лугів, органічні розчинники, що сильно пахнуть і вогненебезпечні речовини. Всі ці залишки зливають у спеціальні пляшки.
18. Закінчивши роботу, перевірте, чи виключена вода, газ, електрика. Здайте лаборанту посуд і реактиви. Поставте металеві штативи на місце, приведіть усе в порядок.
Перша допомога при опіках та отруєннях
1. При термічних опіках відразу роблять примочки етиловим спиртом, або розчином KMnO4.
2. При опіках кислотами необхідно негайно промити уражене місце великою кількістю води, а потім розчином NaOH і знову великою кількістю води.
3. При опіках їдкими лугами необхідно добре промити уражене місце проточною водою, потім слабким розчином оцтової кислоти а потім знову великою кількістю води.
4. При попаданні кислоти або лугу в очі слід відразу ж промити їх водою. Для цього спрямовують невеликий струмінь води то в одне, то в друге око протягом 3-5 хвилин. Потім очі необхідно промити або розчином NaOH (у випадку ураження кислотою), або розчином H3BO3 (у випадку ураження лугом) а потім великою кількістю води. Після цього необхідно терміново звернутися до лікаря.
5. При опіках фенолом уражене місце обробляється спиртом.
6. При опіках шкіри бромом його змивають спиртом або розведеним розчином лугу і промивають великою кількістю води. Після того уражене місце обробляють маззю від опіків. При вдиханні парів брому необхідно глибоко подихати над спиртом а потім випити молоко і вийти на свіже повітря.
7. Шкіру, уражену сильно діючою органічною речовиною, слід швидко промити великою кількістю розчинника і доставити потерпілого у медпункт.
Гасіння місцевої пожежі та одягу що горить
1. При виявленні пожежі терміново відключити газ та електроприлади в усій лабораторії. Швидко забрати всі горючі речовини подальше від вогню, а полум’я гасити вогнегасником, піском або протипожежною ковдрою. Не слід заливати полум’я водою. У багатьох випадках це призводить до більшого розширення полум’я та розширення зони пожежі.
2. Якщо на тому, хто працює, загорівся одяг, необхідно його повалити на підлогу і швидко накрити протипожежною ковдрою. У жодному разі не можна бігти, від цього полум’я тільки посилиться. Можна погасити на собі одяг обливанням водою або швидким перекочуванням по підлозі.
ВИДІЛЕННЯ ТА ОЧИЩЕННЯ ОРГАНІЧНИХ СПОЛУК, ВИЗНАЧЕННЯ ФІЗИЧНИХ КОНСТАНТ, ЯКІСНИЙ АНАЛІЗ
1. Перекристалізація
Цей метод використовується для поділу суміші твердих речовин. Очищення буде проведене успішно, якщо розчинність речовини різко залежить від температури, якщо розчинність речовини, що має бути очищеною в даному розчиннику різко відрізняється від розчинності домішок, якщо розчинник індиферентний стосовно речовини, що очищується.
При кристалізації речовини треба дослідним шляхом підібрати відповідний розчинник із малою кількістю проби. Температура кипіння розчинника повинна бути нижче температури плавлення речовини на 10-150С.
Перекристалізація з води
Реактиви: кристалічні бензойна або щавлева кислоти, забруднені вугіллям.
У колбу ємністю 200-500 мл помістити 2 г бензойної кислоти або таку ж вагу щавлевої кислоти й у випадку з бензойною кислотою прилити 100 мл води, а в випадку з щавлевою - 5 мл води. Вміст пробірки нагріти до початку кипіння. Гарячий розчин відфільтрувати через паперовий фільтр і остудити. Речовини, що очищаються виділяються у вигляді кристалів. Відфільтрувати кристали шляхом відсмоктування рідини. Для цього застосовують лійку Бюхнера. Підібрати фільтр і вкласти його в лійку, змочити водою і щільно притиснути до дна лійки. При включеному вакуумі вилити в лійку розчин з отриманими кристалами. Не припиняючи відсмоктування, віджимають кристали плоскою скляною пробкою. Припинивши відсмоктування, промивають осад водою, знову відсмоктують, переносять кристали на фільтрувальний папір і віджимають насухо. Отримані кристали бензойної або щавлевої кислоти можна використовувати для визначення температури плавлення.
2. Сублімація (возгонка)
При сублімації тверда речовина, минаючи рідкий стан, переходить у пароподібний стан, а пари при охолодженні переходять у твердий. Не всі речовини можуть піддаватися очищенню цим методом. Цей метод можна використовувати при очищенні хінонів, багатоядерних сполук, органічних кислот.
Реактиви: забруднені нафталін або хінон.
На дно стакана тонким шаром помістити 2-3 г забрудненого нафталіну або хінону. Нагріти стакан повільно і невеличким полум'ям, попередньо опустити в стакан скляну лійку. З'являються пари і при охолодженні дають звільнені від домішок кристали, що осідають на охолоджених стінках лійки.
Сублімацію можна проводити в порцеляновій чашці, покритій конічною лійкою. Якщо сублімації піддаються невеличкі кількості речовин, то її проводять на годинниковому склі, поверх прикритим іншим годинниковим склом. Годинникові стекла поміщають у порцелянову чашу, наповнену піском і нагрівають.
3. Екстракція (витяг)
Екстракцію застосовують для виділення речовини з твердої суміші або розчинів визначеним розчинником. На практиці речовину з водяного розчину частіше усього витягають органічним розчинником. Розчинник повинний задовольняти таким вимогам: розчинник не повинний змішуватися з водяною фазою, мати невисоку температуру кипіння. Крім того, розчинність речовини, що екстрагується повинна бути значно вищою, ніж у вихідному розчині; різна густина речовин.
Екстрагування рідин частіше усього проводять у ділильній лійці. Для екстрагування органічних сполук з водних розчинів застосовують бензин, бензол, хлороформ, діетиловий етер і ін.
Перед початком роботи верхню пробку і нижній край ділильної лійки змащують тонким прошарком вазеліну. Потім у неї наливають розчин, що підлягає екстрагуванню і добавляють розчинник, з огляду на те, що загальний обсяг рідини в лійці не перевищував 2/3 її об’єму. Ділильну лійку закривають пробкою й обережно струшують, плавно перевертаючи догори-вниз на протязі 5-10 хвилин, притримуючи пробку і край руками. При струшуванні підвищується тиск усередині лійки. Для його зменшення, ділильну лійку повертають пробкою униз і відкривають кран. Пари розчинника виходять і тиск зрівнюється з атмосферним. Після цього ділильну лійку закріплюють у штативі і лишають до повного поділу прошарків. Знявши пробку з лійки, випускають нижній прошарок через кран, а верхній прошарок зливають через верхній отвір. Для більш повного витягу речовини екстрагування повторюють декілька разів підряд, підливаючи щоразу нові порції розчинника.
Щоб визначити закінчення екстрагування, декілька крапель останньої порції екстракту випаровують на годинниковому склі досуха. Якщо проба випаровується без залишку, то екстрагування закінчене.
Реактиви та посуд: розчин йоду, CCl4, ділильна лійка, колбочки.
У ділильну лійку ємністю до 100 мл помістити приблизно 10 мл розчину йоду та 20 мл CCl4. Зробити екстракцію йоду по вище викладеній методиці.
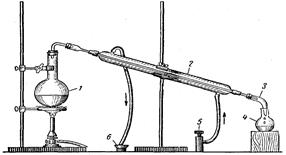
4. Фракційна (дробна) перегонка
Реактиви та посуд: Суміші: а) чотирьоххлористий вуглець і ксилол;
б) ксилол і хлороформ;
в) хлороформ і скипидар, прилад для перегонки
|
|
|
|
|
Дата добавления: 2015-05-24; Просмотров: 552; Нарушение авторских прав?; Мы поможем в написании вашей работы!