
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Самостійна робота учнів. 1. назвати речовину згідно міжнародній систематичній номенклатурі
|
|
|
|
1. назвати речовину згідно міжнародній систематичній номенклатурі




 СН3 СН3 С2Н5 ОН СН3
СН3 СН3 С2Н5 ОН СН3





 О = С – СН – СН2 – СН – СН3 СН3 – СН – С – СН2 – СН2 – СН2 – С = О СН3 – С – СН – СН – СН3
О = С – СН – СН2 – СН – СН3 СН3 – СН – С – СН2 – СН2 – СН2 – С = О СН3 – С – СН – СН – СН3
Н СІ СН3 Н СН3 СН3
2.за назвою напишіть напівструктурну формулу речовин
А) 2,3,3-трихлоробутаналь Б) 2,3-дибромо-4-метилпентаналь
В) 2,5-диметилфенол Г)2,3,5-триметилгексан-1,4-диол
3. напишіть формули трьох можливих ізомерів гексаналю
4. здійсніть перетворення
СН4→СН3СІ→С2Н6→С2Н2→СН3СНО→СН3СООН
5.Визначте об’єм водню,що може приєднатися до 120 грам пентаналю
6.. Масова частка Карбону у сполуці 76,6%,
Гідрогену – 6,38 %, Оксигену – 17,02 %. Густина парів сполуки за вуглекислим газом 2,136. Зайдіть формулу сполуки
Тема 2: Оксигеновмісні органічні сполуки
Заняття 4 карбонові кислоти
Мета: ознайомитися з особливостями будови карбонових кислот на прикладі оцтової кислоти. Навчитись складати напівструктурні формули та називати кислоти за міжнародною систематичною номенклатурою, вивчити будову карбоксильної групи та пов’язані з нею властивостями кислот,познайомити учнів з основними галузями застосування карбонових кислот
Навчальні питання:
1.Карбонові кислоти, склад, будова молекули, фізичні властивості.
2.Ізомерія та номенклатурні назви карбонових кислот.
3.Хімічні властивості кислот, якісні реакції на карбоксильну групу.
4. Добування та застосування карбонових кислот
Навчальна література:
Л-3 с.129-136
Л-4 с. 121-122
Л- 6 с.113-122
І. Карбонові кислоти
| Визначення | Функціо- нальні групи | Загальна формула | Номенк- латурна назва | Види ізомерії | Будова | Застосування | Добування | Фізичні і Хімічні властивості |
| Карбоно-ві кислоти – органічні речовини в молекуло яких є одна або кілька карбоксильних груп |  С = О
ОН
Карбок-сильна група, складає скла з гідроксогрупи і карбонільної групи С = О
ОН
Карбок-сильна група, складає скла з гідроксогрупи і карбонільної групи
|  R – С = О
ОН
СnН2nО2 R – С = О
ОН
СnН2nО2
| Нумерація ланцюга відбувається від карбоксильної групи, закінчення –ова кислота | 1.ізомерія карбонового ланцюга 2.міжкласова ізомерія з естерами | Оксисен в карбонільній групі більш електро- негативний, тому до нього зсувається електронна густина і виникає частковий мінусовий заряд, на гідрогені гідроксо групи виникає частковий додатній заряд. | Оцтова кислота:синтез барвників, пластмас, ліків,штучних волокон,негорючої кіноплівки,ба барвник тканин, пестицидів,естерів, в харчовій промисловості Мурашина кислота:хімічна промисловість-відновник, харчова-як консервант та дезінфікуючий засіб, виробництво каучуку | 1.окиснення спиртів С2Н5ОН +[О]→СН3СООН 2.промисловий спосіб одержання оцтової кислоти 1)крекінг метану СН4→С2Н2+3Н2 2)р-ція Кучерова С2Н2+Н2О→ СН3СНО 3)окиснення оцтового альдегіду киснем повітря СН3СНО+[О]→ СН3СООН 3.окиснення бутану (новий промисловий метод) 2С4Н10+5О2→ 4СН3СООН+2Н2О | 1.дія на індикатор СН3СООН↔СН3СОО-+Н+ 2.взаємодіяз металами 2СН3СООН+Са→(СН3СОО)2Са+Н2 3.взаємодія з оксидами металів 2СН3СООН+СаО→(СН3СОО)2Са+Н2О 4.взаємодія з основами СН3СООН+КОН→СН3СООК+Н2О 5.взаємодія з солями 2СН3СООН+Nа2СО3→2СН3СООNа+Н2О+СО2 6.горіння СН3СООН+2О2→2СО2+2Н2О 7.реакція етерифікації СН3СООН+С2Н5ОН→СН3СООС2Н5 +Н2О 8.взаємодія з галогенами по вуглеводневому радикалу. СН3СООН+СІ2→СН2СІСООН+НСІ |
| Наслідок з будови 1. Між молекулами кислот виникають водневі зв’язки, тому вони рідини 2.водневі зв’язки виникають між молекулами кислоти і води, тому вони добре розчинні. 3.внаслідок сильного відтягування електронної густини від атома Гідрогену, він стає рухливим, може легко заміщуватись на інші атоми тому ці речовини мають сильні кислотні властивості і змінюють забарвлення індикаторів. |
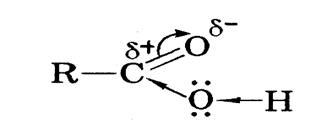
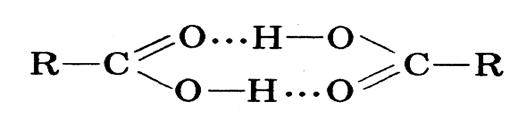
Схема зсуву електронної густини у карбонових кислотах схема утворення водневих зв’язків між молекулами
карбонових кислот
Приклади назви карбонової кислоти згідно міжнародній систематичній номенклатурі


 СН3 СН3 СН3
СН3 СН3 СН3

 С6Н3 – С5Н – С4 – С3Н – С2Н2 – С1 = О 3,4,4,5-тетраметилгексанова кислота
С6Н3 – С5Н – С4 – С3Н – С2Н2 – С1 = О 3,4,4,5-тетраметилгексанова кислота
СН 3 ОН
|
|
|
|
|
Дата добавления: 2015-05-24; Просмотров: 726; Нарушение авторских прав?; Мы поможем в написании вашей работы!