
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Теоретичний вступ. Води світового океану, атмосфери, річок, озер, а також підземні води – об’єднують загальним поняттям – гідросфера
|
|
|
|
ЛАБОРАТОРНА РОБОТА № 10
ЯКІСНЕ ДОСЛІДЖЕННЯ ПРИРОДНОЇ ВОДИ
Води світового океану, атмосфери, річок, озер, а також підземні води – об’єднують загальним поняттям – гідросфера.
Вода, внаслідок полярності її молекул, є добрим розчинником для багатьох речовин. Вона відіграє винятково важливу роль в геохімічних і гідрогеологічних процесах земної кулі. Природні води беруть активну участь в утворенні і руйнуванні різних мінералів. При взаємодії з твердими тілами і газами вода перетворюється в розчин. За своїм складом природні води – це складні фізико-хімічні системи, які містять розчинені речовини у вигляді йонів і молекул, а також мінеральні і органічні речовини у формі колоїдів, суспензій та емульсій. Усі прісні води (з вмістом сухого залишку від 1 г/л та менше), а також мінералізовані води (залишок більше1 г/л), є природними розчинами. Це води річок, озер, морів, океанів, ґрунтові води тощо.
Речовини, що містяться у воді, умовно поділяють за О.Алєкіним на п’ять груп:
1. Головні йони
В природних водах встановлена присутність більше 80 хімічних елементів, але найбільш поширені аніони: НСО3-, SO42-, Cl-, CO32-, HSiO3- і катіони: Na+, Ca2+, Mg2+, K+. Вміст головних йонів у прісних водах складає 90-95% від загального солевмісту.
2. Розчинені гази
У воді найчастіше розчинені такі гази: кисень О2, азот N2, вуглекислий газ СО2; рідше – сірководень Н2S, метан СН4.
Кисень та азот у поверхневі водойми надходять з повітря. Основним джерелом надходження карбон диоксиду є біохімічні процеси розпаду органічних речовин; крім того, він потрапляє у поверхневі водойми з підземними водами, а також поглинається з повітря. Сірководень утворюється в результаті розчинення сульфідних мінералів під дією карбонатної кислоти, а також при відсутності кисню у біохімічному розкладі органічних сполук, що містять Сульфур.
3. Біогенні речовини
До цієї групи належать сполуки, які необхідні для життєдіяльності водних організмів, а також утворені ними в процесі обміну речовин. Це, в першу чергу, є мінеральні і органічні сполуки Нітрогену. Органічні форми Нітрогену представлені білками та продуктами їх розпаду. Неорганічні сполуки Нітрогену (NH3, NO2-, NO3-) можуть утворюватись при розкладанні нітрогенвмісних органічних сполук або надходити в поверхневі води з атмосферними опадами, при вимиванні добрив з ґрунту.
Важливим біогенним елементом є Фосфор. Концентрація сполук Фосфору в чистих водоймах є незначною. Це є мінеральні (дигідроген- та гідрогенфосфати) та органічні сполуки.
Сполуки Феруму(ІІ) містяться тільки в підземних водах, в поверхневих водах концентрація сполук Феруму(ІІІ) незначна внаслідок повного гідролізу солей. Органічна форма вмісту Феруму у воді – це складні комплекси з гуміновими кислотами, які мають буре забарвлення.
Сполуки Силіцію бувають у природних водах у формі різних мінеральних сполук (силікатна кислота та її солі, алюмосилікати) та органічних сполук.
4. Мікроелементи
До цієї групи належать елементи, сполуки яких зустрічаються в природних водах у дуже малих концентраціях – менше за 1 мг/л.
О.О.Алєкін виділяє такі групи мікроелементів:
4.1. Типові катіони (Li+, Rb+, Cs+, Ba2+, Sr2+ тощо);
4.2. Йони важких металів (Cu2+, Ag+, Ni2+, Cd2+ тощо);
4.3. Амфотерні комплексоутворювачі (Co, Mo, V тощо);
4.4. Типові аніони (I-, Br-, F- тощо);
4.5. Радіоактивні елементи.
5. Органічні сполуки
Основну частину органічних речовин природних вод складають гумусові сполуки, що утворюються при розкладанні рослинних решток, а також мікроорганізми і продукти їх взаємодії з навколишнім середовищем.
Вміст органічних сполук у воді характеризується величиною окиснюваності – кількістю кисню, який витрачається на окиснення домішок сильними окисниками (KMnO4, K2Cr2O7). В чистих водах окиснюваність складає від 1 до 4 мг О2 /л.
Першоджерела мінерального складу природних вод на земній кулі – це, по-перше, гази, що виділяються з надр Землі в процесі дегазації мантії, і, по-друге, продукти хімічної взаємодії води з кристалічними породами, які складають земну кору.
Походження аніонів пов’язане, в основному, з газами, які виділились при дегазації мантії. В атмосферу, як в минулому, так і тепер, надходять водневі сполуки Хлору - HCl, Нітрогену – NH3, Сульфуру – H2S, Брому - HBr, Карбону – CH4 та кисневі сполуки Карбону - CO і CO2.
Початковий склад атмосфери Землі дуже відрізнявся від теперішнього. У ньому не було газів сучасної атмосфери (N2, O2), спостерігався інший вміст CO2. Склад атмосфери за 4,5 млрд. років існування Землі змінився під впливом таких процесів:
1. Фотохімічні реакції розкладу молекул газів під впливом космічного випромінювання:

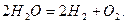
2. Фотосинтетична діяльність організмів, внаслідок якої виділявся кисень і зв’язувався Карбон з карбон(IV) оксиду.
3. Окиснення газів (після виникнення кисню):

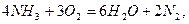
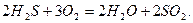
З виникненням в атмосфері постійного вмісту кисню з’явилась окиснювальна атмосфера. Зникли NH3, CH4, H2S. У воді з’явились сульфатні, нітратні йони та аніони інших оксигеновмісних кислот.
Походження катіонів природних вод пов’язане з виверженими кристалічними породами. Розкладання вивержених порід відбувалось під впливом кислих продуктів, які надходили з надр Землі. За хімічним складом ці кристалічні породи переважно належали до алюмосилікатів. За мінералогічним складом вони належали, в основному, до польових шпатів. З часом вивержені породи розкладались – вивітрювались. Спочатку відбувалось фізичне вивітрювання, тобто подрібнення породи під дією коливань температури, замерзання води тощо. Одночасно відбувалось хімічне вивітрювання. Дуже поширений мінерал ортоклаз – польовий шпат вивітрюється за схемою:

При наявності аніонів кислот (карбонатної, сульфатної) утворюється не гідрогенсилікат, а солі відповідних кислот, при дисоціації яких в розчині з’являються йони Na+, K+, Mg2+, Ca2+.
Природні води різного походження дуже відрізняються за кількістю і складом домішок та розчинених речовин. Дослідження фізичних і хімічних показників води дозволяє зробити висновки про якість води та придатність її для пиття, зрошення, а також для різних виробничих потреб.
Грубодисперсні домішки утворюють з водою кінетично нестійкі системи. В стані спокою для таких систем є характерним утворення осаду або спливання в залежності від їх густини. Даний фізико-хімічний процес визначає такі методи очищення вод від домішок:
- відстоювання,
- фільтрування,
- центрифугування.
Найважливіші показники придатності води для пиття – це санітарний стан, який характеризується вмістом нітрогенвмісних сполук (NH3, NO2-, NO3-), сірководню H2S, йона Cl-, а також величиною окиснюваності, що визначається концентрацією органічних сполук у воді.
Аналізом водної витяжки можна дуже точно і швидко визначити ступінь засолення ґрунтів, необхідність промивання, а аналізом природних вод – можливість використання їх для зрошення. Засоленими вважаються ґрунти, які містять розчинені у воді солі більше за 0,2%. Найчастіше серед цих солей у засолених ґрунтах зустрічаються NaCl, Na2SO4, NaHCO3, CaSO4, CaCl2, MgSO4, MgCl2. Вміст водорозчинних солей у більшості ґрунтів коливається від сотих до десятих часток відсотка. В засолених ґрунтах (наприклад, у солончаках) кількість водорозчинних речовин може досягати кількох відсотків.
При визначенні засоленості ґрунтів у водній витяжці визначають сухий залишок – загальну суму водорозчинних речовин, склад аніонів (CO32-, НСО3-, SO42-, Cl-) і катіонів (Ca2+, Mg2+, Na+, K+). При скороченому аналізі визначають сухий залишок, катіони Ca2+ і Mg2+, аніони НСО3-, Cl- та SO42-.
Негативно впливають на рослини не всі, а тільки токсичні солі, до яких належать Na2CO3, MgCO3, NaHCO3, Mg(HCO3)2, Na2SO4, MgSO4, NaCl і CaCl2.
Присутність йонів CO32- у водній витяжці пов’язана тільки з токсичними солями. Наявність йонів НСО3- у водній витяжці може бути зумовлена присутністю токсичних солей NaHCO3, Mg(HCO3)2 та нетоксичної солі Ca(HCO3)2. У тому випадку, коли йонів Ca2+ у водній витяжці більше, ніж НСО3-, то усі йони НСО3- відносять до нетоксичних. Наявність йонів SO42- може бути зумовлена присутністю в ґрунті токсичних (Na2SO4,, MgSO4) і нетоксичних (CaSO4) солей.
Йони Cl- відносять до токсичних, оскільки всі солі, що їх містять, є токсичними.
|
|
|
|
|
Дата добавления: 2015-05-24; Просмотров: 430; Нарушение авторских прав?; Мы поможем в написании вашей работы!