
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Експериментальна частина. До 100 мл досліджуваної води, відміряної мірною колбою в конічну колбу на 250 мл, додати 2-3 краплі розчину фенолфталеїну
|
|
|
|
До 100 мл досліджуваної води, відміряної мірною колбою в конічну колбу на 250 мл, додати 2-3 краплі розчину фенолфталеїну. Якщо з’явиться рожеве забарвлення, то воду слід титрувати 0,1н. розчином хлоридної кислоти до знебарвлення. Потім у ту ж пробу додати 2-3 краплі розчину метилоранжу і продовжувати титрування 0,1н. розчином хлоридної кислоти до переходу забарвлення з жовтого в рожеве. Записати об’єм 0,1н. розчину хлоридної кислоти, який витрачений на титрування за фенолфталеїном і загальний об’єм 0,1н. розчину хлоридної кислоти, який витрачений на все титрування.
Загальну лужність (ЛЗ) води (ммоль-екв/л) розраховують за формулою:
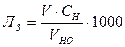 (ммоль-екв/л),
(ммоль-екв/л),
де V – загальний об’єм розчину хлоридної кислоти, витрачений на титрування взятого об’єму досліджуваної води, мл; 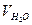 - об’єм води, взятої для дослідження, мл; СН – молярна концентрація еквівалента розчину хлоридної кислоти.
- об’єм води, взятої для дослідження, мл; СН – молярна концентрація еквівалента розчину хлоридної кислоти.
Для розрахунку карбонатної твердості визначають лужність досліджуваної води за фенолфталеїном (ЛФ), яку розраховують за формулою:
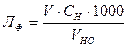 (ммоль-екв/л),
(ммоль-екв/л),
де V – об’єм розчину хлоридної кислоти, витраченої на титрування за фенолфталеїном, мл.
Тоді ТКАРБ. = ЛЗ – ЛФ. Якщо лужність за фенолфталеїном дорівнює нулю, то можна вважати, що загальна лужність води дорівнює її карбонатній твердості.
Титрування повторюють три рази. Розходження в об’ємі кислоти, витраченої на титрування, не повинно перевищувати 0,05 мл. В зазначену формулу підставляють середні значення. Результати дослідів представляють у вигляді таблиці 18:
Таблиця 18
Результати визначення ЛЗ, ЛФ і ТКАРБ.
| № з.п. | 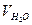 ,
мл ,
мл
| СН НС1 , моль-екв./л | VH Cl ф-фт, мл | ЛФ, ммоль-екв./л | VH Cl ф-фт + м-ор, мл | ЛЗ, ммоль-екв./л | ТКАРБ ., ммоль-екв./л |
| Сер. |
Контрольні завдання
1. Розрахувати постійну твердість води, якщо для видалення кальцій-катіонів, які містились в 50 л цієї води, витрачено 21,6 г безводної бури.
2. Яку масу Са(ОН)2 необхідно додати до 1000 л води, щоб усунути тимчасову твердість 2,86 ммекв/л?
3. Розрахувати тимчасову твердість води, знаючи, що на реакцію з гідрогенкарбонатом, який міститься в 50 мл цієї води, витрачено 2,5 мл 0,1н. розчину НС1.
4. Розрахуйте загальну твердість води, якщо в 0,15 л води міститься 16,20 мг кальцій гідрогенкарбонату, 2,92 мг магній гідрогенкарбонату, 11,10 мг кальцій хлориду і 9,50 мг магній хлориду.
5. Знайдіть тимчасову твердість води, якщо на титрування 0,1 л зразку води, яка містить магній гідрогенкарбонат, витрачено 7,2 . 10-3 л 0,14 н. НС1.
6. Для усунення загальної твердості вапняно-содовим методом до 50 л води було додано 7,4 г Са(ОН)2 і 5,3 г Na2CO3. Розрахувати тимчасову і постійну твердість води.
7. Чому дорівнює постійна твердість води, якщо для її усунення до 25 л води було додано 21,6 г бури Na2B4O7 . 10H2О?
8. Некарбонатна твердість води дорівнює 3,18 ммекв/л. Яку масу Na3PO4 треба взяти, щоб пом’якшити 1м3 води?
9. Загальна твердість Рівненської водопровідної води дорівнює 8,52 ммекв/л, а тимчасова 6,95 ммекв/л. Яку масу Са(ОН)2 і Na2CO3 треба взяти, щоб усунути твердість 5 л води?
10. Твердість деякого зразку води обумовлена тільки кальцій нітратом. При обробці 0,25 л зразку води натрій карбонатом в осад випало 37,8 мг СаСО3. Чому дорівнює твердість води?
11. Для пом’якшення 100 л води витратили 12,72 г Na2CO3. Чому дорівнює твердість води?
12. Яку масу гашеного вапна треба додати до 2,5 л води, щоб усунути її тимчасову твердість 4,43 ммекв/л?
13. При визначенні тимчасової твердості на титрування 0,1 л води витрачено 5,25 . 10-3 л 0,101н. НС1. Чому дорівнює твердість води?
14. Твердість деякого зразку води обумовлена тільки ферум(ІІ) гідрогенкарбонатом. При кип’ятінні 0,25 л води в осад випадає 4 мг FeCO3. Чому дорівнює твердість води?
15. Яка тимчасова твердість води, в 1 л якої міститься 0,146 г магній гідрогенкарбонату?
16. Визначити загальну твердість води, якщо в 1 л цієї води міститься 120 мг Са2+ і 24 мг Mg2+. Чи можна цю воду застосовувати для зрошення?
17. Твердість води, що містить кальцій гідрогенкарбонат, дорівнює 3 ммоль-екв/л. Визначити масу гідрогенкарбонату в 1 л такої води.
18. Яку масу натрій карбонату необхідно додати до 2 л води, щоб усунути загальну твердість, що дорівнює 6,2 ммоль-екв/л.
19. Визначити тимчасову твердість води, якщо на реакцію з гідрогенкарбонатом, що міститься в 100 мл цієї води, використано 6 мл 0,1н розчину НС1.
20.Яку масу натрій карбонату потрібно додати до 5л води, щоб усунути загальну твердість води, що дорівнює 4,6 ммоль-екв/л?
|
|
|
|
|
Дата добавления: 2015-05-24; Просмотров: 632; Нарушение авторских прав?; Мы поможем в написании вашей работы!