
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Замечания и предложения будут приняты по адресу: anesthesiolog@tut.by 2 страница
|
|
|
|
H+ + HbO2 ↔ HbH+ + O2
Соответственно, увеличение концентрации ионов водорода вызывает смещение реакции вправо, снижая связывание кислорода с гемоглобином и облегчая его отдачу в тканях – эффект Бора (Bohr effect). При развитии ацидоза эффект Бора компенсирует дефицит кислорода в тканях путём увеличением его отдачи. Таким образом, буферная и транспортная функции гемоглобина находятся в тесной взаимосвязи (см. рис. 1).
В венозных капиллярах физически растворённый CO2 поступает в эритроциты из плазмы, где под действием фермента карбоангидразы (CAZ) вступает в связь с водой и образует угольную кислоту – H2CO3. Угольная кислота диссоциирует на бикарбонат и ион водорода. В эритроцитах бикарбонат соединяется с калием, образуя бикарбонатную соль:
HCO3- + K+ → KHCO3
При снижении концентрации бикарбоната в плазме процесс носит обратный характер, высвобождая HCO3-. Бикарбонат диффундирует обратно в плазму, а для поддержания электронейтральности и компенсации утечки анионов в эритроциты из плазмы поступают ионы Cl-. В легочных капиллярах все происходит наоборот - ионы бикарбоната поступают в эритроциты, обмениваясь на Cl-.. Процесс обеспечивается работой протеинового обменника, обозначенного на рисунке 1 кругом. Обменное перемещение ионов хлора в эритроците называется хлоридным сдвигом Гамбургера. Вошедшие в эритроциты ионы хлора соединяются с калием, образуя – KCl, сохраняя электронейтральное состояние клетки.
В легочных капиллярах поступивший в эритроциты бикарбонат соединяется с H+, образуя H2CO3. Образовавшийся в результате CO2 диффундирует в альвеолы, элиминируясь из организма с выдыхаемым воздухом.
Следует обратить внимание, что эффект Бора быстрее проявляется при респираторном ацидозе. Ион водорода и бикарбонат проникают через клеточные мембраны медленно, требуя несколько часов для полной диффузии и наступления равновесия в системе внеклеточная/внутриклеточная жидкость. Углекислый газ, напротив, диффундирует гораздо быстрее, приводя к внутриклеточному ацидозу.
Как упоминалось выше, восстановленный (дезоксигенированный) гемоглобин ведет себя подобно основанию, присоединяя ионы водорода. Теоретически, чем ниже сатурация гемоглобина венозной крови кислородом, тем больше в ней восстановленного гемоглобина, и, следовательно, концентрация бикарбоната и BE (см. «терминология анализов КЩС и ABG») будет увеличена по сравнению со значениями артериальной крови. На самом деле в таком случае в венозной крови будут находятся кислые продукты метаболизма, в том числе и анаэробного (молочная кислота) и уровень бикарбоната будет снижаться эквипотенциально ликвидирующей ацидоз работе буфера.
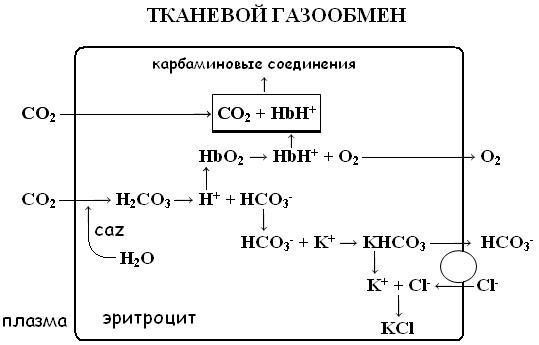

Рис. 1 Взаимосвязь транспортной и буферной функций гемоглобина. Представлены основные физиологические механизмы газообмена и работы буферной системы гемоглобина. Объяснение в тексте.
Физико-химические свойства гемоглобина после отдачи кислорода меняются – сродство восстановленного гемоглобина к CO2 увеличивается в 3,5 раза по сравнению с оксигемоглобином. Данное свойство называется эффектом Кристиансена-Дугласа-Холдейна, или кратко эффектом Холдейна (Haldane effect), обозначенным на рисунке 1 прямоугольным контуром. Эффект Холдейна обусловлен реакцией CO2 с аминогруппами, приводящей к образованию карбаминовых соединений (карбаминогемоглобина):
R-NH2 + CO2 → RNH-CO2- + H+
Упрощая вышеописанные процессы,
работу гемоглобинового буфера можно описать следующим образом:
· H+ + KHb ↔ HbH+ + K+ для нейтрализации нелетучих кислот;
· H2CO3 + KHb ↔ HbH+ + HCO3- + K+ для нейтрализации летучих кислот.
2.3 ФОСФАТНЫЙ БУФЕР
Фосфатный буфер играет главную роль в буферировании мочи и внутриклеточной жидкости.
Основные элементы фосфатного буфера – H2PO4 и HPO4-.
Механизм действия фосфатного буфера аналогичен работе бикарбонатной буферной системы: поступивший ион водорода от сильной кислоты соединяется с HPO4- образуя H2PO4. При добавлении в систему щелочи происходит обратная реакция с образованием HPO4- и H2O из H2PO4 и OH-.
Роль фосфатного буфера заключается в конверсии сильных щелочей и кислот в более слабые соединения.
pK фосфатного буфера равна 6,8, что ближе к среднему значению pH по сравнению с pK бикарбонатного буфера. Несмотря на то, что сила фосфатного буфера выше, чем у бикарбонатного, его роль в буферировании во внеклеточной жидкости невелика, так как общая концентрация фосфатов в крови составляет около 8% от концентрации бикарбоната.
В почках фосфатный буфер особенно важен, так как, во-первых, количество фосфатов в моче достаточно велико, а во вторых, pH канальцевой жидкости ниже, чем pH плазмы, приближаясь к pK фосфатной буферной системы.
Во внутриклеточной жидкости концентрация фосфатов выше, чем во внеклеточной, а pH внутри клетки несколько ниже, чем снаружи, что обеспечивает эффективность фосфатного буфера как внутриклеточного.
3. Компенсаторные механизмы
Компенсаторные механизмы при нарушениях КЩС включаются последовательно в зависимости от мощности и эффективности буферной системы. Выделяют три основные физиологические системы, регулирующие баланс ионов водорода:
· непосредственно буферные системы жидкостного компартмента организма;
· дыхательная система (респираторный центр);
· мочевыделительная система (почки).
Практически немедленно развивается действие бикарбонатного буфера в плазме, затем – в интерстициальной жидкости. Для полного развития действия внутриклеточных буферов необходимо несколько часов.
Время реагирования механизмов компенсации нарушений КЩС различно:
1. Внеклеточное буферирование: 10-15 минут. Осуществляется с помощью бикарбонатного буфера.
2. Внутриклеточное буферирование: 2-4 часа. Осуществляется преимущественно за счет гемоглобинового буфера.
3. Респираторная компенсация: 3-5 часов (максимальная – 12-24 часа).
4. Почечная компенсация: 6-8 часов начало (максимум – 5-7 дней).
3.1 РЕСПИРАТОРНАЯ КОМПЕНСАЦИЯ
Регуляция дыхания происходит двумя путями:
· по «отклонению» (центральная регуляция) - управляется количеством ионов водорода в цереброспинальной жидкости;
· по «возмущению» - (периферическая регуляция) - контролируется периферическими хеморецепторами, располагающимися в каротидных тельцах общих сонных артерий, связана с колебаниями PaO2 в плазме.
Дыхание в норме регулируется центральными хеморецепторами, располагающимися в продолговатом мозге на дне IV желудочка (см. «Респираторный алкалоз»). Непосредственно хеморецепторы продолговатого мозга реагируют на изменения концентрации ионов водорода в цереброспинальной жидкости (ЦСЖ), но так как водород практически не проникает через ГЭБ, то основную регуляторную роль оказывает физически растворённый в плазме CO2 (PaCO2). Нормальные значения PaCO2 находятся в пределах 35–45 mmHg. Уровню PaCO2 40 mmHg соответствует 1,2 моль/л физически растворенного CO2.
Количественное изменение pH находится в определённой зависимости от уровня альвеолярной вентиляции. Так, увеличение альвеолярной вентиляции в два раза вызывает изменение pH на 0,23. Если нормальное значение pH равно 7,40, то двукратное увеличение альвеолярной вентиляции «поднимет» pH до 7,63. Напротив, снижение альвеолярной вентиляции на ¼ часть от нормы «понизит» pH на 0,45. То есть если нормальное значение pH 7,40, то уменьшение нормальной альвеолярной вентиляции на четверть вызовет снижение pH до 6,95. Частота вентиляции может увеличиваться в 15 раз сверх нормы, что теоретически делает респираторную компенсацию весьма эффективной в коррекции изменений КЩС, однако на практике эффект респираторной компенсации органичен (см. далее).
Альвеолярная вентиляция влияет на количество ионов водорода посредством элиминации CO2, но и изменение количества H+ также вызывает изменение альвеолярной вентиляции. Так, метаболический ацидоз с pH 7,0 увеличивает альвеолярную вентиляцию в 4-5 раз.
Проникая через ГЭБ, CO2 сдвигает реакцию диссоциации угольной кислоты вправо:
CO2 + H2O ↔ H2CO3 ↔H+ + HCO3-
| Бикарбонатный буфер является единственным буфером цереброспинальной жидкости, в основном благодаря тому, что ГЭБ является непроницаемым для подавляющего большинства веществ. К тому же в тканях головного мозга происходят интенсивные метаболические процессы, продукт местного аэробного метаболизма CO2 в большом количестве поступает непосредственно в ЦСЖ, влияя на респираторную регуляцию. Количество растворенного в ЦСЖ углекислого газа на 10 мм. рт. ст. выше, чем в плазме и составляет в среднем 50 мм. рт. ст. Перемещение CO2 из плазмы в ЦСЖ происходит за 60 секунд, если же изменение pH плазмы не связано с PaCO2, то для изменений pH ЦСЖ требуется более длительное время. |
Образовавшийся в результате диссоциации угольной кислоты водород активирует хеморецепторы, увеличивая альвеолярную вентиляцию. Так, при повышении PaCO2 в крови на 1 мм. рт. ст. минутный объем дыхания возрастает на 1-4 л/мин сверх нормы.
Находящиеся в плазме ионы водорода также диффундируют в цереброспинальную жидкость, но значительно медленнее, чем CO2. Следовательно, ацидоз вызывает накопление ионов водорода в ЦСЖ как быстрым прямым проникновением CO2 через ГЭБ, так и более медленным переходом ионов водорода из плазмы. Конечное повышение H+ в ЦСЖ вызывает стимуляцию дыхательного центра, увеличивая тем самым альвеолярную вентиляцию и снижая в итоге PaCO2.
Ионы бикарбоната не проникают через гематоэнцефалический барьер, однако, при развитии алкалоза снижение протонов водорода оказывает депрессивное действие на дыхательный центр. Величина PaCO2 (именно - H+) при которой вентиляция равна нулю, называется порогом апноэ. На практике врачи чаще всего сталкиваются с ним при выходе больного из анестезии, во время которой проводилась гипервентиляция. Отсутствие спонтанных дыхательных попыток больного зачастую принимается за остаточное действие релаксантов либо анестетиков. Гипокапния, обусловленная гипервентиляцией, также препятствует эффективному отучению больных от ИВЛ (weaning).
Если же снижение альвеолярной вентиляции происходит в результате компенсации метаболического алкалоза, то увеличение PaCO2 направленно на коррекцию pH до нормальных величин. Однако такая компенсаторная реакция не совершенна, так как при достижении определенного порога CO2 включаются активированные вследствие гиповентиляции и гипоксии защитные механизмы периферических хеморецепторов, реагирующих на отклонения PaO2 от нормы.
Таким образом, респираторная компенсация эффективна для коррекции метаболического ацидоза, но не алкалоза. Для метаболического ацидоза эффективность дыхательной компенсации составляет 50-75%. Это значит, что при сильном снижении pH респираторная система не в состоянии полностью компенсировать расстройство КЩС. Например, если в результате попадания сильной кислоты во внеклеточную жидкость pH снизится с 7,4 до 7,0, то респираторная система сможет вернуть pH только до 7,2 – 7,3.
Если центральная регуляция является основной физиологической регуляцией в условиях покоя, то периферические хеморецепторы представляют собой группу «быстрого реагирования», включающуюся в условиях острой гипоксии. Активность периферических рецепторов существенно не меняется, пока PaO2 не упадет ниже 50 мм. рт. ст. Однако как только PaCO2 станет превышать 65 мм. рт. ст., то PaO2 может являться основным стимулом дыхательной активности уже и при значениях менее 80 мм. рт. ст. У больных ХОБЛ при нарушении функции внешнего дыхания и развитии хронической гипоксии и гиперкарбии центральные хеморецепторы становится менее чувствительным к постоянно повышенному PaCO2, переключая регуляцию дыхания на регуляцию по «возмущению». В таком случае дыхательная активность всецело зависит от колебаний PaO2 в крови. Если такому больному с целью коррекции гипоксии дать кислород, то «возмущенный» дыхательный центр успокоится, что немедленно проявится угнетением дыхания. Не совсем понятно значение данного синдрома в клинике – многие врачи категорически против применения кислорода у таких больных, однако не будет ли гипоксия при угнетении дыхания нарастать вновь, снова стимулируя дыхательный центр? По-видимому, главное неблагоприятное значение такого срыва вентиляторной компенсации заключается не в усугублении гипоксии, а в замедлении выведения CO2.
Однако в современных исследованиях было показано, что у больных ХОБЛ с имеющейся хронической гиперкапнией после подачи кислорода содержание PaCO2 увеличивалось, но минутный объем вентиляции оставался неизменным [20]. Это значит, что кислородотерапия у таких больных не меняет легочные объемы и не действует угнетающе на дыхательный центр.
Поэтому главным неблагоприятным эффектом кислородотерапии является изменение вентиляционно-перфузионных отношений. Этот феномен объясняется увеличением шунтирования крови через невентилируемые участки легких. При гипоксии в зонах легких, где есть альвеолярная гиповентиляция, включается рефлекс Эйлера-Лилиестранда, который заключается в вазоконстрикции мелких сосудов легких - таким способом организм пытается уменьшить объем шунта (не оксигенирующейся крови). Этот рефлекс действует и в нормальных физиологических условиях для поддержания адекватного вентиляционно-перфузионного отношения, так как в нижних отделах легких кровоток преобладает над вентиляцией, а в верхних – наоборот. Рефлекс Эйлера-Лилиестранда (гипоксическая легочная вазоконстрикция) в определенной степени уравновешивает неравномерности распределения вентиляция/кровоток в зонах West. У больных ХОБЛ с одной стороны гипоксическая вазоконстрикция предотвращает выраженную гипоксемию, направляя кровоток в наиболее вентилируемые зоны легких; с другой стороны, спазм сосудов легких вызывает повышение легочного сосудистого сопротивления, провоцируя развитие легочного сердца и правожелудочковой недостаточности. Оксигенотерапия снимает вазоконстрикцию, вызывая «обвал» сосудистой регуляции.
Об увеличение шунтирования свидетельствует отмеченное в исследованиях увеличение PaCO2 без изменения легочных объемов. Как изменяется артериальное PaO2 не совсем ясно, так как с одной стороны увеличение альвеолярного напряжения кислорода увеличивает диффузию оного через альвеолярно-капиллярную мембрану, с другой стороны – увеличение шунта эффективно «разбавляет» повышенное PaO2 в крови конечных легочных капилляров. Да и если гипоксемия вновь достигнет критических величин, не запуститься ли вазоконстрикция вновь? Неблагоприятные последствия кислородотерапии – абсорбционные ателектазы – могут привести к усугублению неравномерности вентиляционно-перфузионных соотношений.
Дабы не углубляться в софизм, следует добавить, что подход к больным с ХОБЛ должен быть сугубо индивидуальным, при проведении оксигенотерапии нужно внимательно следить за функцией внешнего дыхания у пациента, не забывая о возможной депрессии дыхательного центра и усилении гипоксии вследствие угнетения легочной вазоконстрикции.
В отдельных случаях депрессию дыхательного центра может вызывать и острый респираторный ацидоз, обусловливая при очень высоких цифрах PaCO2 развитие синдрома углекислого наркоза (carbon-dioxide narcosis). Углекислый наркоз возникает, вероятно, в результате нарастания интранейронального ацидоза и увеличения внутричерепного давления.
3.2 ПОЧЕЧНАЯ КОМПЕНСАЦИЯ
Почечный механизм компенсации более медленный, чем респираторный. Полноценная почечная компенсация развивается только через несколько дней после изменения pH.
Существует несколько механизмов почечной компенсации:
1. реабсорбция или экскреция бикарбоната;
2. регенерация (образование) бикарбоната;
3. экскреция H+ в виде титруемых кислот и ионов аммония.
Почечная компенсация при ацидозе
При ацидозе механизмы почечной компенсации включаются последовательно и состоят из трех этапов:
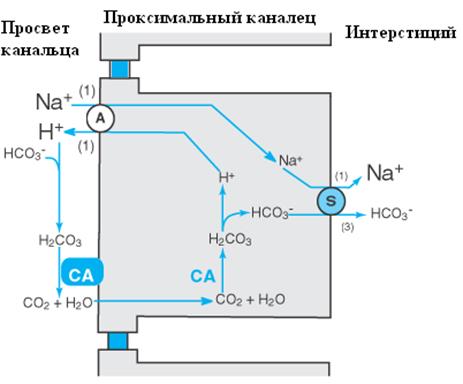
Рис. 2. Реабсорбция бикарбоната в проксимальном канальце нефрона.
A – антипортер, S – симпортер, СА – карбоангидраза, цифрами в скобках обозначены пропорции обмениваемых ионов.
· увеличение реабсорбции HCO3-
· увеличение экскреции титруемых кислот
· увеличение выработки аммиака (аммониогенез)
Увеличение реабсорбции HCO3- (см. рис. 2).
В клетках проксимальных почечных канальцев под влиянием Na+/H+-обменника (антипортера) ион натрия поступает из мочи в клетку в обмен на протон водорода. Далее, часть натрия при помощи Na+/K+-АТФазы удаляется в кровь, а протон в моче связывает профильтровавшийся ион бикарбоната и образует молекулу угольной кислоты (Н2СО3). Работа Na+/K+-АТФазы создает концентрационный градиент для ионов натрия между тубулярной жидкостью и клетками проксимальных почечных канальцев. Градиент движения Na+ обеспечивает энергией движение H+ в противоположном направлении.
Угольная кислота под влиянием карбоангидразы IV, которая лежит на поверхности мембраны клеток канальца, распадается на СО2 и Н2О. Далее углекислый газ путем пассивной диффузии и, возможно, через аквапориновые каналы типа 1, поступает в клетки канальца, где за счет работы цитоплазматической фракции карбоангидразы II вновь превращается в угольную кислоту. Угольная кислота подвергается диссоциации до протона и бикарбоната. Протон снова включается в Na+/H+-обмен, а ионы бикарбоната переносятся в кровь. Транспорт HCO3- через базолатеральную мембрану осуществляется при помощи двух механизмов:
1. Na+/HCO3- симпортер (рис. 2);
2. Cl-/HCO3- обменник (рис. 5).
Таким образом возвращаются в кровь 80-85% бикарбоната, оставшиеся 10-20% подвергаются реабсорбции в дистальных канальцах.
Работа протонной помпы проксимальных канальцев сопряжена с реабсорбцией натрия: чем больше натрия реабсорбируется, тем больше выводится протонов водорода, следовательно, увеличивается количество связанного в моче бикарбоната, обеспечивая его возврат в сосудистое русло.
Каждый день почки фильтруют порядка 4320 мэкв бикарбоната (180л/день × 24 мэкв/л), который в обычных условия практически полностью реабсорбируется обратно, сохраняя бикарбонатную буферную систему в целостности. Так как реабсорбция бикарбоната сопряжена с экскрецией водорода, то для полноценной его реабсорбции почкам необходимо секретировать 4320 мэкв водорода в сутки. Дополнительно организму необходимо вывести 80 мэкв водорода, чтобы избавиться от нелетучих кислот, синтезируемых ежедневно. Итого дневная секреция H+ составляет 4400 мэкв/сутки. Практически весь водород секретируется в проксимальных канальцах, и только около 5% H+ секретируются в дистальных канальцах и собирательных трубочках. В проксимальной части нефрона концентрация ионов водорода может быть увеличена только в 3 или 4 раза, тогда как в дистальных отделах количество секретируемого H+ может увеличиваться в 900 раз. Поэтому в проксимальных канальцах pH может быть снижен только до 6,7, а в дистальных канальцах и собирательных трубочках – до 4,5.
Когда практически весь бикарбонат уже реабсорбировался и ионы водорода, которые секретирует Na+/H+-обменник, уже не способны нейтрализоваться бикарбонатом, возникает закисление мочи. Как упоминалось выше, вследствие синтеза нелетучих кислот суточная экскреция водорода превышает фильтрацию бикарбоната на 80 мэкв. Водород способен самостоятельно элиминироваться с мочой в ионизированный форме в виде H+. Таким образом выводиться только небольшое количество H+. Минимальное значение pH мочи составляет 4,5, что соответствует концентрации H+ 10-4.5 мэкв/л или 0,03 мэкв/л. Таким образом, каждый литр мочи может вывести максимум 0,03 мэкв ионизированного (свободного) водорода. Чтобы экскретировать 80 мэкв нелетучих кислот ежедневно почкам необходимо было бы выделить 2667 литров мочи. Буферирование ионов водорода существенно облегчает процессы его элиминации. Наиболее мощными буферными системами мочи являются фосфатная и аммониевая. Существующие другие слабые буферные системы мочи (уратная и цитратная) не играют существенной роли в коррекции pH.
Увеличение экскреции титруемых кислот (буферирование) (см. рис.3)
Выведение H+ осуществляется при помощи монофосфата, (HPO42-). В результате образуется H2PO4-, обладающий отрицательным зарядом, препятствующим его канальцевой реабсорбции. H2PO4- существует в моче в виде натриевой соли - NaH2PO4.
В результате работы фосфатного буфера возникает не только титрование ионов водорода, но и сохранение бикарбоната. В этом случае наработанный бикарбонат в клетках почечных канальцах поступает непосредственно в кровь, восполняя его потери во внеклеточной жидкости при ацидозе. Таким образом, если H+ связывается с другими буферами, нежели бикарбонатный, чистым дополнительным эффектом будет являться добавление HCO3- во внеклеточную жидкость.
Фосфатный буфер (H2PO4-/HPO42-) с pK 6,8 является идеальным буфером для мочи. В обычных условиях фосфатный буфер может «связать» только около 30-40 мэкв H+ в день. При нарастании ацидоза и дальнейшем закислении мочи резервы фосфатного буфера исчерпываются, передавая основную роль аммониевой буферной системе.
Увеличение выработки аммиака (аммониогенез) (см. рис. 4)
При истощении запасов монофосфата наиболее важным буфером мочи становится пара аммиак/аммоний - NH3/NH4+. Константа диссоциации для пары аммиак/аммоний равна 9,2, что не совсем подходит для pH канальцевой жидкости. Несмотря на это аммониогенез является спасительным механизмом компенсации возросшей кислотной нагрузки, что объясняется следующим. Аммиак образуется в результате дезаминирования глутаминовой кислоты в митохондриях эпителия почечных канальцев. Эту реакцию ускоряют ацидоз и гипокалиемия.
Одна молекула глутамина метаболизируется до двух молекул аммиака и двух молекул бикарбоната[3]. NH3 легко диффундирует через люминальную мембрану, попадает в просвет канальца и взаимодействует с водородом, образуя ион аммония (аммониогенез). NH4+ является ионизированным соединением, не способным проникнуть через клеточную мембрану, свободно элиминируется с мочой в комплексе с ионом хлора. Бикарбонат через базолатеральную мембрану поступает в интерстициальную жидкость и затем в кровь. Чем больше ацидоз, тем больше увеличивается выработка NH3. Таким образом, чистый эффект аммониогенеза заключается не только в выведении ионов водорода, но и в образовании бикарбоната, восполняя его потери во внеклеточной жидкости.
В нормальных условиях количество H+, элиминировавшегося при помощи фосфатного буфера, составляет 50% от всего экскретируемого почками водорода, равно как и количество образованного в почках бикарбоната (в процентном соотношении). Однако при хроническом ацидозе посредством аммониевого буфера почки способны выделять гораздо больше кислот – до 500 мэкв/сутки. Соответственно, увеличивается и образование бикарбоната на 500 мэкв/сутки. Этот механизм играет основную роль в компенсации хронического ацидоза, что будет подробно рассмотрено в главе, посвященной ренальному канальцевому ацидозу. Когда количество ионов водорода во внеклеточной жидкости снижается (алкалоз), почки теряют способность реабсорбировать бикарбонат. Снижение количества бикарбоната вследствие повышенной секреции равносильно расходу его на титрование кислот. Поэтому удаление бикарбоната из организма вызывает увеличение концентрации H+ во внеклеточной жидкости. Чем больше выражен алкалоз, тем больше угнетена реабсорбция НСО3-.
Почки обладают значительными возможностями в коррекции метаболического алкалоза, но также могут являться и непосредственной причиной его развития.
Функциональная роль почечных канальцев такова, что при определённых условиях образование или реабсорбция бикарбоната может резко увеличиваться.
Например, дефицит натрия активирует его реабсорбцию в проксимальных канальцах (см. рис.2). Вследствие увеличения реабсорбции натрия происходит увеличение экскреции водорода (см. рис. 2, работа Na+/H+ антипортера), что в конечном итоге способствует образованию НСО3-. Образование НСО3- в таком случае происходит даже на фоне уже имеющегося метаболического алкалоза Избыток минералокортикоидов может также вызвать метаболический алкалоз. Действуя в дистальных отделах почечных канальцев и в области корковых отделов собирательных трубочек, альдостерон увеличивает реабсорбцию натрия путем облегчения его диффузии через ионные каналы из просвета канальца и повышения активности Na+/K+-АТФазы в базальной мембране (см. рис. 5). Поскольку транспорт натрия не сопряжен с другими ионами, он приводит к перемещению положительного заряда в клетку и наружная цитоплазматическая мембрана приобретает более отрицательный заряд, чем внутренняя, обращенная в сторону кровеносного сосуда(60 мВ против 75 мВ).

Рис. 3. Работа фосфатного буфера при экскреции кислот. A – антипортер, S – симпортер, СА – карбоангидраза
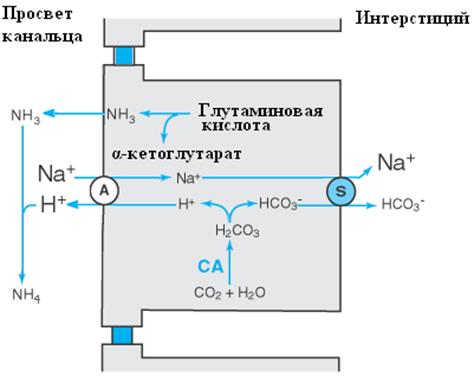
Рис. 4. Увеличение выработки аммиака и экскреция аммония с мочой. A – антипортер, S – симпортер, СА – карбоангидраза
Почечная компенсация при алкалозе
.
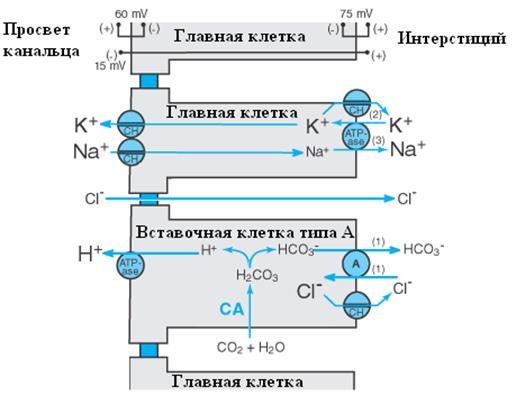
Рис. 5. Поздние дистальные отделы и собирательные трубочки.
Механизм опосредованного альдостероном метаболического алкалоза. Объяснение в тексте. A – антипортер, Ch – ионный канал (ion channel), ATP-ase – АТФ-аза, СА – карбоангидраза.
Компенсировать разность электрохимического потенциала (составляющую на примере около 15 мВ) можно путем увеличения транспорта отрицательно заряженных ионов в интерстиций либо экскрецией положительно заряженных частиц в просвет канальца. В почечных канальцах присутствуют оба механизма – возникающий отрицательный заряд при переносе ионов натрия способствует пассивной диффузии ионов хлора по электрохимическому градиенту через межклеточные соединения и секреции протонов водорода Н+-АТФазой вставочных клеток типа А. Так как секреция Н+ сопряжена с образованием бикарбоната (см. рис.5), то при повышении альдостерон-индуцируемой реабсорбции натрия развивается метаболический алкалоз, причем гиперальдостеронизм (Conn’s syndrome) может являться причиной метаболического алкалоза даже при отсутствии дефицита натрия.
Далее приведем основные причины, влияющие на увеличение или снижение секреции водорода и реабсорбцию бикарбоната (табл. 2).
Таблица 2. Факторы, влияющие на увеличение или снижение секреции H+ и реабсорбции HCO3- в почечных канальцах. Arthur C. Guyton, M.D., John E. Hall, Ph.D. Textbook of Medical Physiology 11th ed. 2006.
| Увеличение секреции H+ и реабсорбции HCO3- | Снижение секреции H+ и реабсорбции HCO3- |
| ↑ PaCO2 | ↓PaCO2 |
| ↑H+ ↓HCO3- | ↓H+, ↑HCO3- |
| ↓ОЦК | ↑ОЦК |
| ↑Ангиотензин II | ↓Ангиотензин II |
| ↑Альдостерон | ↓Альдостерон |
| Гипокалиемия | Гиперкалиемия |
|
|
|
|
|
Дата добавления: 2015-05-09; Просмотров: 1235; Нарушение авторских прав?; Мы поможем в написании вашей работы!