
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Опухоли мочевой собирательной системы 1 страница
|
|
|
|
Опухоли почки
Рак почки. Рак почки (аденокарцинома почки — устаревшее название «гипернефрома») составляет 85% всех случаев первичных опухолей почки. Ежегодно в США раком почки заболевают до 18000 человек и около 8000 умирают от этого заболевания. Наиболее часто рак почки отмечают у людей в возрасте 55—60 лет. Причем чаще (в 2 раза) болеют мужчины. К факторам риска, связанным с окружающей средой, относят сигаретный дым и кадмий. Существуют генетически передаваемые формы рака, характеризующиеся многоочаговым и двусторонним поражением почек. Чаще эту форму рака диагностируют у лиц с болезнью Гиппеля—Линдау (проявляющейся гемангиомами сетчатки и центральной нервной системы, наследуемыми по аутосомно-доминантному типу). В некоторых семьях, пораженных семейным раком почки, был обнаружен маркер хромосомных транслокаций между хромосомами 3 и 8 и 3 и 11. У находящихся на хроническом диализе больных с терминальной стадией почечной недостаточности может развиться кистозное поражение почки и как следствие рак почки. При помощи электронной микроскопии и иммунологических методик было установлено, что раковые клетки развиваются из эпителия извитых проксимальных канальцев почки. Применять термин «гипернефрома» для обозначения рака не следует, поскольку он отражает ранее существовавшее мнение о происхождении этой опухоли из клеток коркового вещества надпочечников.
Клинические признаки. Рак почки был назван «терапевтической опухолью», поскольку это заболевание часто диагностируют даже при отсутствии метастазов по системным, а не по урологическим проявлениям. Хотя триада, состоящая из выраженной гематурии, болей в боку и пальпируемого образования в области живота, считается классической совокупностью признаков для постановки клинического диагноза рака почки, все эти признаки одновременно встречаются менее чем у 10% больных. Приблизительно у 30% больных будет наблюдаться по меньшей мере один из указанных признаков. Самым распространенным считают гематурию, которая наблюдается у 60% больных. Хотя микрогематурию, выявляемую при исследовании осадка мочи, рассматривают как стойкий патологический признак, кровотечение обычно не бывает обильным, позволяя опухоли увеличиться до значительных размеров без клинических проявлений, прежде чем возникнут боли в боку и станет очевидным наличие образования в области живота. Опухоль обычно распространяется в направлении почечной капсулы, околопочечной жировой клетчатки, лимфатических узлов, почечной вены, нижней полой вены и надпочечника, расположенного на той же стороне, что и пораженная почка. Метастазы чаще наблюдают в легких, средостении, костях, центральной нервной системе, щитовидной железе и печени.
Приблизительно у 50% больных отмечают быструю утомляемость, потерю массы тела и кахексию, иногда перемежающуюся лихорадку, не связанную с инфекционным заболеванием (причем она может быть единственным симптомом). В начале заболевания приблизительно у 50% больных развивается анемия. Примерно у 5% больных наблюдают эритроцитоз, обусловленный выработкой эритропоэтинов. Возможны также эозинофилия, лейкемоидные реакции, тромбоцитоз и повышенная скорость оседания эритроцитов. Раковые опухоли почки могут продуцировать гормоны или гормоноподобные вещества, включая паратгормоны или простагландины (что может вызвать гиперкальциемию), пролактин (галакторея), ренин (гипертензия), гонадотропины (феминизация и маскулинизация) и глюкокортикоиды (синдром Кушинга). Внутрипочечные артериовенозные свищи, образующиеся при сосудистых опухолях, могут предрасполагать к развитию застойной сердечной недостаточности. Инвазия опухоли в почечную вену и в нижнюю полую вену может привести к внезапному появлению бессимптомного варикоцеле и отеку нижней конечности соответственно. Окклюзия опухолью почечной вены (с обструкцией или без обструкции полой вены) может вызвать развитие гепатоспленомегалии и асцита. Иногда нарушения функции печени обнаруживают у тех больных, у которых нет метастазов в печень. После удаления первичной опухоли эти нарушения часто исчезают.
Диагностика (рис. 231-1). Подозрение на рак почки могут вызвать такие признаки, как внутрипочечные кальцификаты и/или изменения контуров почек, наблюдаемые на обзорных рентгенограммах брюшной полости. Однако основным методом исследования, при помощи которого выявляют и оценивают большинство образований в почках, служит внутривенная урография (ВВУ) в сочетании с нефротомографией. Необходимо отдифференцировать кистозное поражение почек от опухолей почек. При выявлении деформированной, расширенной или не поддающейся визуализации собирательной системы почек и неровных их контуров можно предположить рак. Нефротомография дает возможность получить четкие очертания контуров почек и помогает отличить кистозные поражения от плотных образований. Ультразвуковая эхография поможет отличить выявленные эхографически простые кисты от опухолей почек. С учетом данных нефротомографии точность диагностирования доброкачественной кисты с помощью ультразвуковой эхографии приблизительно равна 97%. Если кистозное поражение, наблюдаемое при проведении ВВУ, аналогично имеющим доброкачественный вид кистозным поражениям, выявляемым при ультразвуковой эхографии, обнаруживается у больного, у которого нет каких-либо симптомов и гематурии, то, вероятно, нет необходимости в проведении пункции кисты. В таком случае следует периодически повторять ВВУ или ультразвуковое исследование.
Если требуется точность диагностики свыше 97% или если при повторных ВВУ или ультразвуковых исследованиях выявляются какие-либо изменения, можно выполнить пункцию кисты с аспирацией содержимого и последующей его цитологической оценкой. Нисходящая цистография, проведенная после аспирации, может дать дополнительную ценную информацию. Иногда, хотя и очень редко, рак почки может диагностироваться одновременно с простой кистой, локализуясь в ее пределах.

Рис. 231-1. Диагностическое исследование для выявления различных образований в области почек.
Если выявленное с помощью ВВУ или ультразвукового исследования новообразование не соответствует критериям, принятым для определения доброкачественной простой кисты, применяют компьютерную томографию (КТ). По информативности КТ сравнима с селективной артериографией почки, а возможно, даже превосходит ее по эффективности диагностики рака почки, а также установления стадии его развития. Кроме того, КТ равноценна селективной артериографии почки в отношении определения поражения почечной вены и превосходит ее по возможности выявления увеличения регионарных лимфатических узлов (вызванного или наличием опухолевых клеток, или гиперплазией) и/или поражения печени. КТ является предпочтительным методом исследования для диагностики рака почки и определения стадии развития процесса. Однако если результаты КТ допускают неоднозначное толкование или если требуется провести дополнительное исследование сосудистого русла, то КТ следует дополнить артериографией почки.
Другие исследования. Цитологическое исследование мочи не помогает диагностике рака почки. Полезным дополнительным исследованием, позволяющим контрастировать те участки собирательной системы почек, которые не заполняются контрастным веществом при проведении стандартной ВВУ, может быть ретроградная пиелография. Она может дать основание предположить диагноз переходноклеточного рака почечной лоханки. У больных с гематируей и увеличением почек цистоскопия является важным вспомогательным методом ис следования, предназначенным для того, чтобы исключить одновременное существование какой-либо опухоли, развивающейся из эпителия мочевых путей, такой как рак мочевого пузыря.
Если диагноз рака почки считается вероятным, то в дополнение к КТ брюшной полости больному следует провести рентгенологические исследования грудной клетки и костей, а также исследовать функцию печени для выявления потенциально возможных отдаленных метастазов.
Стадии болезни, основное лечение и прогноз. Если в ходе предоперационного обследования не выявлены метастазы, то показана радикальная нефрэктомия. Кроме удаления почки и окружающей ее фасции Героты, многие урологи-хирурги считают целесообразным выполнение регионарной лимфаденэктомии для уточнения прогноза. Предоперационная эмболизация основной почечной артерии упрощает операционный подход в случае обширного поражения тканей. Проводить пред- или послеоперационную локальную лучевую терапию нецелесообразно.
После проведения операции и выполнения гистологического исследования определяют стадию развития рака почки, руководствуясь следующим: стадия I — опухоль расположена в пределах почечной капсулы; стадия II — опухоль проросла за пределы почечной капсулы, но ограничена пределами фасции Героты; стадия III — поражены регионарные лимфатические узлы, почечная вена, расположенная на той же стороне туловища, или полая вена; стадия IV— отдаленные метастазы. Срок жизни после определения стадии I рака почки исчисляется пятью годами для 60—75% больных; при стадии II — для 47— 65%; при стадии III без поражения регионарных лимфатических узлов—для 25—50%, а в случае поражения этих узлов—для 5—15%; при стадии IV— менее 5%.
Системная терапия при метастаза х. При лечении больных с метастатическим раком почки стандартного подхода при назначении химиотерапевтических, гормональных или иммунных препаратов не существует. Хотя ранее и сообщалось о благоприятном действии гестагенных и андрогенных средств, все же гормональная терапия, по-видимому, играет очень незначительную роль в лечении больных раком почки. Обычно проводимая химиотерапия предусматривает применение винбластина сульфата в сочетании с нитрозомочевиной или без нее. Недостаточно эффективен и интерферон. Системное ведение больных раком почки еще находится в стадии исследования.
Селективное хирургическое ведение больных с мета-стазами. Опрометчиво надеяться на то, что после удаления почки у больного, находящегося в стадии IV рака, протекающего в остальных отношениях бессимптомно, произойдет самопроизвольная регрессия метастазов. Однако если при первичном поражении наблюдаются боли, кровотечение или другие паранеопластические нарушения, то иногда бывает целесообразно удалить первичную опухоль или рассмотреть возможность выполнения ангиоинфаркта в целях локального купирования процесса, несмотря на наличие метастазов. У больных, в анамнезе у которых имелся рак почки, в результате чего возник изолированный метастаз в легких или в центральной нервной системе, часто бывает целесообразно провести резекцию этих метастазов. У больных, которым назначено хирургическое удаление изолированных метастазов, по меньшей мере в течение 1 года с момента постановки первичного диагноза до развития метастазов не отмечают никаких проявлений заболевания, а опухоли у них были медленно растущими.
Разнообразные опухоли почки. У детей самым распространенным видом рака почки является опухоль Вильмса (нефробластома). При этих опухолях эффективна многоформная терапия, включающая хирургическое вмешательство, лучевую терапию и сочетанную химиотерапию с использованием актиномицина D и винкристина. Метастазы в почках обычно наблюдают у больных раком легкого, молочной железы и меланомой. Поражение почки возможно и при злокачественной лимфоме; однако обычно не бывает функциональных почечных нарушений в результате поражения паренхимы.
Встречаются и доброкачественные опухоли почек. Обычно их обнаруживают случайно при патологоанатомическом исследовании. Наиболее распространенная доброкачественная опухоль почки у новорожденных и младенцев — это мезобластическая нефрома (гамартома плода); таких больных успешно лечат путем простой нефрэктомии.
Вся мочевая собирательная система, начиная от почечной лоханки до мочеиспускательного канала выстлана переходно-клеточным эпителием, или «уротелием». Данный эпителий легко подвергается канцерогенным воздействиям. Этим и объясняется множественность уротелиальных опухолей. Чаще встречается рак мочевого пузыря, несколько реже — опухоли почечной лоханки. Рак мочеточника, как и рак мочеиспускательного канала, встречается редко.
Рак мочевого пузыря. В США рак мочевого пузыря ежегодно диагностируют приблизительно у 40 000 человек; из этого числа 11 000 больных в год умирают. Мужчины болеют в 3 раза чаще, чем женщины. Чаще заболевают люди в возрасте старше 40 лет. Причем замечено, что развитие переходно-клеточного рака преобладает у лиц, подвергающихся воздействию ароматических аминов, особенно 2-нафталамина. Этим, вероятно, можно объяснить высокую частоту появления различных видов уротелиального рака среди курильщиков сигарет и рабочих химических заводов, а также заводов, выпускающих красители и определенные виды резины. Плоскоклеточным раком чаще заболевают лица, у которых выявлена хроническая инвазия Schistosoma haematolium. Возникновение уротелиальных опухолей связывают с длительным введением противоракового алкилирующего средства — циклофосфана, который метаболизируется до активных веществ — акролеина и фосфорамида иприта.
Клинические признаки. Чаще всего больные предъявляют жалобы на макро- и микрогематурию, у них отмечают также дизурию, частое мочеиспускание или недержание мочи. Иногда эти симптомы могут быть единственным проявлением рака мочевого пузыря, и стойкое присутствие их у ранее внешне здорового человека заслуживает внимания. Другие проявления, такие как обструкция мочеточника, боли в области таза или симптомы, связанные с висцеральными или костными метастазами, выявляют при обследовании у небольшого числа больных.
Диагностика и определение стадии процесса. Основными методами диагностики рака мочевого пузыря являются цитологическое исследование мочи, полученной при промывании мочевого пузыря, посредством катетеризации или после мочеиспускания, ВВУ и цистоскопическое исследование с взятием биоптатов из опухоли и выборочно с участков слизистой оболочки, так же как и бимануальное исследование, проводимое под анестезией. К числу выявленных при ВВУ факторов, заставляющих предположить рак мочевого пузыря, относятся односторонняя или двусторонняя обструкция мочеточников с гидронефрозом, дефект наполнения или отсутствие растяжимости мочевого пузыря. Дополнительную информацию относительно стадии процесса можно получить с помощью выполнения КТ брюшной полости или полости малого таза. После эндоскопической резекции опухоли мочевого пузыря оценивают глубину проникновения ее в стенку пузыря. Если дополнительные исследования, направленные на определение стадии заболевания, включая физикальное обследование, рентгеноскопию грудной клетки и биохимический анализ крови, дадут нормальные результаты, то на основании данных биопсии делают заключение относительно того, является ли клиническая стадия заболевания поверхностной или инвазивной. Дополнительную информацию относительно околопузырного распространения опухоли или наличия метастазов в лимфатических узлах можно получить при цистэктомии, которая и укажет истинную патологическую стадию заболевания. У значительного числа больных, стадия заболевания которых отнесена по данным эндоскопии к мышечно-инвазивной, возможны скрытые метастазы в лимфатические узлы или в отдаленные участки тела, если стадию заболевания определяли во время проведения цистэктомии. Такие скрытые микрометастазы указывают на системное поражение, и они ответственны за увеличение числа больных, у которых в конечном итоге возникнут отдаленные метастазы, несмотря на лечение при первичном поражении мочевого пузыря.
Лечение. Рак мочевого пузыря можно подразделить на поверхностный, инвазивный и метастатический. К числу лиц, страдающих поверхностным раком мочевого пузыря, относятся больные с карциномой in situ, с поражением слизистой оболочки (стадия О) или подслизистых слоев (стадия А). Таким больным обычно проводят эндоскопическую резекцию и выборочно берут биоптаты из стенки мочевого пузыря. Через каждые 3—6 мес цистоскопические исследования повторяют. Приблизительно у 50—70% таких больных в течение 3 лет после постановки первоначального диагноза возникает поверхностный рецидив заболевания (поражение слизистой оболочки или подслизистых слоев). Таким больным делают цистоскопическую резекцию и внутрь мочевого пузыря вводят N, N', N''-триэтилентиофосфамид (тиотепа), доксорубицина гидрохлорид, митомицин С или бациллу Кальметта—Герена (БЦЖ).
Еще у 12% больных с начальным поверхностным поражением в конечном итоге разовьется прогрессирующий рак с распространением опухоли в мышцы мочевого пузыря (стадия Б), околопузырную клетчатку (стадия В) или метастазами в лимфатические узлы (стадия Г1), кости или другие внутренние органы (стадия Г2). У некоторых больных первичным может быть инвазивное или метастатическое поражение.
Инвазивное поражение. У больных с инвазивным поражением опухоль проросла в мышцы и/или в околопузырную жировую клетчатку. Традиционными методами лечения считают цистэктомию (радикальная или простая), лучевую терапию или предоперационную лучевую терапию с последующей цистэктомией. При такой схеме лечения приблизительно 45% больных могут прожить еще 5 лет. Причиной летального исхода для большинства таких больных (несмотря на проведение радикальной хирургической операции или лучевую терапию) будут отдаленные метастазы, а не рецидивы местного поражения.
Метастатическое поражение. Из числа больных с отдаленными метастазами в лимфатических узлах, внутренних органах или костях только у 30—70% эффективна системная химиотерапия; но, как правило, улучшение длится не более 6 мес. Большинство больных после появления метастазов живут около 2 лет. Применяемые в настоящее время активные химиотерапевтические средства, такие как цисплатин, метотрексат, доксорубицина гидрохлорид, циклофосфан и винбластин, а также различные сочетания этих средств, обеспечили обнадеживающие долговременные ремиссии. Одна из современных стратегий лечения больных с инвазивным поражением заключается в проведении химиотерапии, а затем осуществлении местного лечения мочевого пузыря (хирургическое или облучение). Целью такой программы является уничтожение микрометастазов, которые обычно имеются у больных с инвазивным поражением.
Переходно-клеточный рак почечной лоханки. Опухоли почечной лоханки составляют приблизительно 10% всех случаев первичного рака почки. Почти 90% из них представляют собой переходно-клеточный рак. Помимо этиологических факторов, вызывающих рак мочевого пузыря, развитию опухолей почечной лоханки способствует нефропатия, вызванная злоупотреблением анальгетиками. Эту форму рака обычно наблюдают у женщин среднего возраста, в анамнезе которых имеются психические заболевания или хронические головные боли и которые в течение нескольких лет приняли большое количество анальгетиков (более 3 кг). Точное количество и вид анальгетиков, вызывающих переходно-клеточный рак, неизвестны, хотя в эксперименте рак этого вида могут индуцировать аспирин и/или фенацетин. Эндемическая балканская нефропатия (см. также гл. 226) связана с высокой частотой случаев развития опухолей почечной лоханки и мочеточников, особенно у женщин.
У большинства больных с переходно-клеточным раком почечной лоханки отмечают безболезненную макрогематурию. Обструкция мочеточника и вызванные тромбами боли встречаются редко. Диагностика основана на результатах ВВУ, с помощью которой выявляют закупоренную, плохо функционирующую или невизуализирующуюся почку или дефект наполнения в визуализируемой почке, и положительных результатах цитологического исследования мочи. Установить природу и локализацию опухоли почечной лоханки или мочеточника позволяют цистоскопия и ретроградная пиелография со взятием биоптата. Консервативное лечение с локальным иссечением пораженного участка и сохранением паренхимы почки на ранних стадиях развития небольших злокачественных опухолей дает благоприятные результаты. После проведенной операции больные живут до 5 лет. При обширных поражениях и на поздних стадиях заболевания лечение заключается в радикальной нефроуретерэктомии и удалении участка мочевого пузыря вместе с мочеточником, идущим от пораженной почки и его устьем. Указанный оперативный подход необходим, чтобы избежать рецидива рака в культе мочеточника и его устье. Кроме того, в дальнейшем обязательно проведение цистоскопического контроля и цитологических исследований мочи чтобы не пропустить возможное впоследствии развитие рака мочевого пузыря и/или опухоли мочеточника или почечной лоханки, расположенных на противоположной стороне. Из числа подобных больных в течение 5 лет выживет 10— 50%. Химиотерапию, разработанную для лечения больных раком мочевого пузыря, применяли и для лечения больных с метастатическим переходно-клеточным раком почечной лоханки, но результаты такого лечения оказались менее успешными.
РАЗДЕЛ 3. ОПУХОЛЕВЫЕ БОЛЕЗНИ
ГЛАВА 293. Т-ЛИМФОТРОПНЫЕ ВИРУСЫ ЧЕЛОВЕКА
Роберт К. Галло, Антоны С. Фаучи (Robert С. Gallo, Anthony S. Fauci)
Биология ретровирусов. Впервые ретровирусы были выделены от цыплят в начале этого века. Позднее, в 50-х годах, от мышей, больных лейкозом, был выделен ретровирус млекопитающего. В настоящее время уже хорошо известно, что эти вирусы связаны с возникновением у многих видов животных как злокачественных, так и незлокачественных заболеваний. Ретровирусы в зависимости от вызываемых ими форм заболеваний могут быть разделены на злокачественные, незлокачественные, одновременно злокачественные и незлокачественные и непатогенные. Непатогенные вирусы часто наследуются как нормальные генетические менделевские элементы. Этот путь их наследования уникален, эти вирусы получили название эндогенных. Примером вируса, обладающего одновременно как злокачественными, так и незлокачественными свойствами, служит вирус, который может вызвать лейкоз у кошек. Он вызывает Т-лейкоз, однако чаще бывает ответствен за нарушения, напоминающие синдром приобретенного иммунодефицита человека (см. гл. 257). Ретровирусы, вызывающие незлокачественные заболевания, например энцефалит и другие неврологические болезни, артриты, болезни легких, относятся к медленно действующим и обозначаются как лентивирусы. Их выделяют от копытных животных, человека (Т-лимфотропный вирус, человека III типа, или HTLV-III) и нечеловекообразных обезьян (обезьяний Т-лимфотропный вирус III типа, или STLV-III).
Ретровирусы имеют внешнюю оболочку, отпочкованную от клеточной мембраны, и содержат электронно-плотную сердцевину, окружающую вирусный геном. Sine qua поп ретровируса представляет собой ДНК-полимеразу, которую называют обратной транскриптазой и которая вместе с РНК входит в состав сердцевины. Обратная транскриптаза катализирует перевод генетической информации из РНК-в ДНК-форму (провирус). Провирус затем обычно мигрирует из цитоплазмы к ядру и после перехода в кольцевую двуспиральную форму интегрируется с ДНК клетки-хозяина, в которой и остается на протяжении всей жизни клетки (рис. 293-1). Поскольку провирус в процессе S-фазы клеточного цикла удваивается вместе с собственно клеточной ДНК, то и дочерние клетки наследуют вирусный геном. Таким образом, организм инфицируется как бы в течение всей жизни. При экспрессии вируса его РНК и белки можно обнаружить в цитоплазме клетки, а также в связи с внутренней поверхностью клеточной мембраны, в которой отпочковывание и высвобождение вируса завершают его жизненный цикл. Иногда происходят делеции провируса, в результате чего формируемый вирус приобретает некоторые свойства, отличающие его от оригинального варианта.
Молекулярные механизмы повреждения клетки вирусом обусловлены структурными особенностями его генома. Наиболее показательны в этом плане вирусы хронических лейкозов, содержащие всего три гена, ответственных за вирусную репликацию: gag, pol и env (рис. 293-2; см. гл. 59). Первый (gag) кодирует синтез внутренних структурных белков, pol — обратной транскриптазы, а env — гликопротеинов оболочки. Свойства оболочки вируса имеют решающее значение в выборе типов клеток, которые он может инфицировать, исходя из чего можно понять требования, предъявляемые к новым антивирусным вакцинам, которые должны способствовать выработке антител, действие которых направлено на оболочку вируса. Вирусная генная цепочка на обоих концах ограничена нуклеотидной последовательностью, которую называют длинным концевым повтором (ДКП) и которая содержит регуляторные элементы, влияющие на экспрессию вирусных генов, а иногда и на вблизи расположенные гены клетки-хозяина. Длинный концевой повтор содержит сигналы, определяющие интеграцию провируса в ДНК клетки-хозяина и образует участки окончания считывания интегрированной провирусной последовательности нуклеотидов. Примерами вирусов, вызывающих хронические лейкозы, могут служить FeLV, вирус лейкоза мышей, вирус лейкоза птиц. До индукции лейкоза эти вирусы интенсивно реплицируются в клетках хозяина. Доказано, что эти вирусы вызывают лейкоз путем интеграции в специфический участок хромосомы, таким образом, ассоциированные ДКП стимулируют постоянную экспрессию клеточных генов, участвующих в процессах роста клетки. Наиболее демонстративным примером этого механизма действия служит развитие у цыплят лейкоза, обусловленного вирусом лейкоза птиц. Его длинный концевой повтор стимулирует экспрессию клеточного онкогена, что, по-видимому, служит первой ступенью в индукции лейкоза. Интеграция вируса носит случайный характер, однако высокая скорость репликации благоприятствует интеграции вируса именно в те участки хромосомы, которые расположены достаточно близко к клеточному онкогену, и, таким образом, ДКП получает возможность его активации. Все это позволяет объяснить совершенно очевидную необходимость длительного размножения вируса до начала развития злокачественного процесса.

Рис. 293-1. Жизненный цикл ретровируса.
Интактные вирионы проникают в клетку после адсорбции на специфических клеточных рецепторах. Одноцепочечная вирусная РНК лишается оболочки, а обратная транскриптаза синтезирует двуспиральную вирусную ДНК, проникающую в ядро и интегрирующуюся в геной клетки-хозяина. При определенных условиях ДНК провируса не экспрессируется. В других случаях она транскрибируется с образованием РНК, кодирующей вирусные белки, и геномной РНК. Затем происходит сборка вириона из вирусных белков и геномной РНК с последующим его отпочковыванием от клеточной мембраны.
Ретровирус, в результате генетических рекомбинаций приобретающий в своем геноме ген клетки-хозяина, который быстро трансформирует клетки и индуцирует острые злокачественные процессы, часто называют вирусом острого лейкоза или саркомы, а ген обозначают как вирусный onc-ген (см. рис. 293-2; см. гл. 58 и 59).
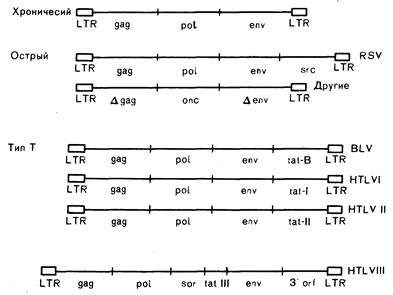
Рис. 293-2. Генная структура и предлагаемая классификация ретровирусов. Синтез внутренних структурных белков кодирует gag, синтез обратной транскриптазы — ро1, гликопротеинов оболочки — env; LTR — длинный концевой повтор; Dgag, Denv — неполные гены; sre — один из онкогенов; BLV — вирус коровьего лейкоза; tat — транскрипционный трансактиватор; sor — короткая открытая рамка считывания; 3'orf—3' — открытая рамка считывания. Функции последних двух генов у HTLV-III не известны.
Вирусы, содержащие onc-ген, немногочисленны и у человека не обнаружены. Они представляют скорее интерес для изучения механизмов неопластической трансформации, чем как этиологический фактор естественного развития опухолей. Каждая клетка, инфицированная этими вирусами, может трансформироваться (развивается поликлональная опухоль), так как продукт вирусного onc-гена оказывает непосредственное трансформирующее действие. Таким образом, для развития опухоли не требуется интеграции вируса в какой-либо определенный участок хромосомы клетки-хозяина.
Общие свойства ретровирусов человека. Третья категория ретровирусов (трансактивационные ретровирусы) представлена хорошо известными вирусами человека: Т-лимфотропными вирусами типов I и II (HTLV-I и HTLV-II) и вирусом коровьего лейкоза (BLV). Третий известный ретровирус человека HTLV-III, или лимфаденопатический вирус, выделен в особую категорию. Геномы всех этих вирусов обладают следующими свойствами: 1) помимо генов вирусной репродукции, они содержат один добавочный ген или более; 2) добавочный ген (гены) негомологичен гену (генам) клеток млекопитающего, т. е. не представляет собой onc-ген; 3) по крайней мере один из добавочных генов кодирует синтез протеина, который участвует в активации экспрессии других вирусных генов и, возможно, некоторых генов клетки (преимущественно за счет связывания с регуляторными усиливающими элементами в клетке, которые сходны с вирусными ДКП). Биологический эффект этих вирусов опосредован именно этим геном, который обозначается как транскрипционный трансактиватор (tat). С учетом того, что tat кодирует синтез протеина ядра, который может активировать другие гены, становится ясно, что для индукции заболевания этому вирусу совсем не требуется интегрироваться в какую-то особую область хромосомы. Следовательно, для развития опухолевого процесса нет необходимости в продолжительной репликации вируса в организме. Сходный феномен отмечается и при развитии лимфомы у коров, вызываемой вирусом BLV. Вирус HTLV-III содержит не только три гена вирусной репликации и ген tat, но еще по крайней мере два других гена, функции которых остаются невыясненными.
|
|
|
|
|
Дата добавления: 2017-01-14; Просмотров: 197; Нарушение авторских прав?; Мы поможем в написании вашей работы!