
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Спектральная идентификация углеводов
|
|
|
|
Идентификация моносахаров с применением ИК-спектроскопии является довольно трудной задачей. Причина этому – сложность строения сахаров и одновременное наличие различных функциональных групп и таутомерных форм. Чаще всего, ИК-спектры применяют для установления идентичности двух образцов сахаров, при этом исследуемый и известный (стандартный) образцы должны быть приготовлены одинаковым способом и находиться в одном и том же агрегатном состоянии. Необходимость этого обусловлена сильной зависимостью положения сигналов в сахарах от агрегатного состоянии вещества. Например, для аморфного и кристаллического образца исследуемого сахара, смещение отдельных полос может достигать 20 см-1.
Деформационным колебаниям С–Н связи при аномерном центре в пиранозах соответствует полоса поглощения при 844±8 см-1, если водородный атом расположен экваториально, и полоса при 891±7 см-1, если этот атом расположен аксиально. Эта закономерность широко используется для определения конфигурации у С1 и может быть использована для определения конформации пиранозного кольца в моносахаридах или их производных с известной конфигурацией при С1. Аналогичным образом может применяться закономерность, наблюдаемая для ИК-спектров полных ацетатов пираноз: в этих соединениях колебаниям С–О-связи у аномерного центра отвечает полоса при 1160 см-1, если ацетоксильная группа расположена аксиально, и при 1128 см-1, если эта группа экваториальна.
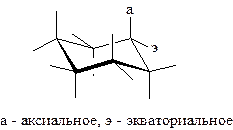
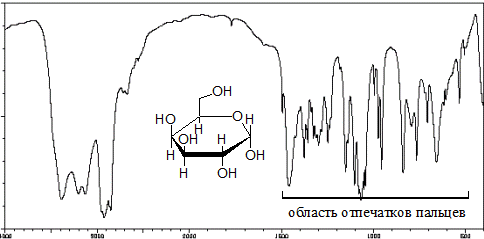
Рис. 3. ИК-спектр D -галактопиранозы
Однако, сравнивая ИК-спектры двух углеводов D -галактопиранозы (рис.) и 1,2,3,4,5,6-циклогексангексанола (рис..) можно понять, что делать серьезные выводы по одному внешнему виду спектров невозможно, поскольку они очень похожи. Требуется тщательный анализ области «отпечатков пальцев» и применение дополнительных спектральных методов исследования молекул для установления их структуры.
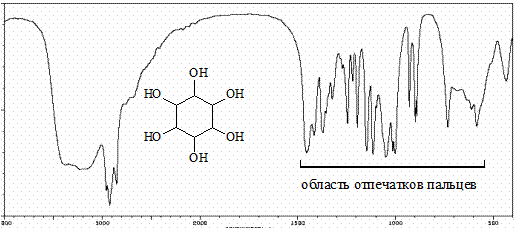
Рис. 4. ИК-спектр1,2,3,4,5,6-циклогексангексанола
Наиболее приемлема ИК-спектроскопия для установления взаимного положения гидроксильных групп в сахарах. Для такого исследования готовят разбавленные (0,005 М) растворы сахаров в четыреххлористом углероде, что позволяет избежать образования межмолекулярных ассоциатов. Если гидроксильная группа в сахарах участвует в образовании внутримолекулярной водородной связи ее сигнал смещается в длинноволновую область. Образование пятичленного цикла с участием гидроксигруппы сдвигает ее сигнал на 30 см-1, а для шестичленных циклов этот сдвиг достигает 80 см-1. Интенсивность сигнала позволяет судить о количестве гидроксильной группы данного типа в равновесной смеси.
Изомер А 5-окси-2-фенил-1,3-диоксана имеет одну полосу поглощения ν(ОН) при 3593 см-1, это связано с фиксацией гидроксигруппы за счет образования водородных связей и возможно лишь при цис -конфигурации изомера. Эта конформация приобретает устойчивость за счет экваториально расположенного ароматического кольца и водородных связей между гидроксигруппой и атомами кислорода шестичленного кольца. Для изомеров В и С существуют две полосы поглощения при 3633 и 3593 см-1, что объясняется возможностью существования равновесия двух конформаций в растворе, одна из которых стабилизирована двумя экваториальными заместителями, а вторая – водородной связью.
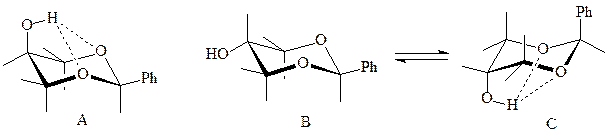
Например, для дезоксисахара с разветвленной цепью углеродных атомов возможны две структуры А и В.
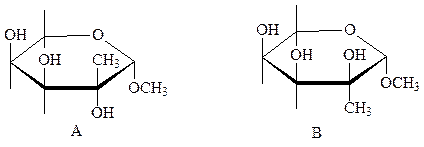
В ИК-спектре этого сахара присутствует полоса поглощения при 3512 см-1, характерная для шестичленного цикла типа С. Образование такой системы связей возможно только при образовании конформации типа D. Из этого можно сделать вывод, что образец исследуемого вещества представляет собой В -изомер.
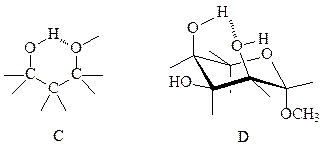
ИК-спектры позволяют различать g[*]- и d-лактоны альдоновых кислот, так как в g-лактонах полоса поглощения валентных колебаний С=О лежит в интервале 1760-1800 см-1, а в d-лактонах – при 1725-1750 см-1.
Для валентных колебаний N-H-связи характерно поглощение в интервале 3100-3500 см-1. 5-Ацетамидо-5-дезокси-L-арабиноза может существовать в двух изомерных формах А и В. Поскольку в ИК-спектре арабинозы присутствует полоса поглощения при 3450 см-1, соответствующая NH-группе, можно сказать, что она существует в форме изомера А.
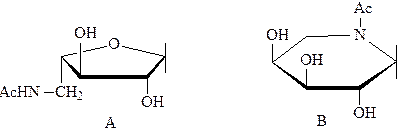
Моносахариды и их производные имеют ряд особенностей, которые можно использовать при установлении их строения, используя спектры ЯМР 1Н. Например, протоны (А и B), связанные с ацетальным атомом углерода резонируют в самом слабом поле - 5.27 и 4.59 м.д., соответственно. Впрочем, если более электроакцепторные группы присоединяются к другим атомам углерода, то очередность резонирования протонов в силовом поле может измениться.
Аксиальный (ориентированный вдоль оси, направленной перпендикулярно к основной плоскости молекулы) атом водорода (В) пиранозного кольца резонирует в более сильном электромагнитном поле, чем экваториальный (ориентированный перпендикулярно к этой оси) (А) (см. рис. 5).
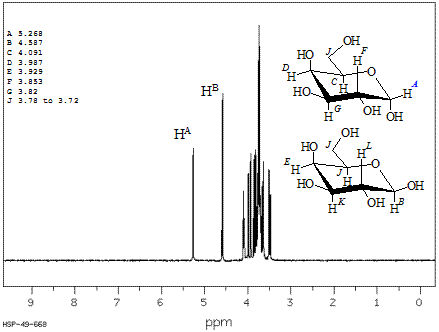
Рис. 5. Спектр ЯМР 1Н D -галактопиранозы
Использование масс-спектрометрии для исследования строения сахаров осложняется тем, что для получения спектров необходимо перевести вещество в газообразное состояние, что сделать с кристаллическими тугоплавкими сахарами очень трудно. Поэтому часто получают различные производные сахаров, например эфиры, обладающие значительно более низкой температурой возгонки.
Распад циклических сахаров под действием электронного удара происходит с разрывом связей, находящихся вблизи от гликозидного центра между атомами С1-С2, С1-Огликозида и С1-Окольца. Специфично протекает фрагментация для пиранозных и фуранозных циклов.
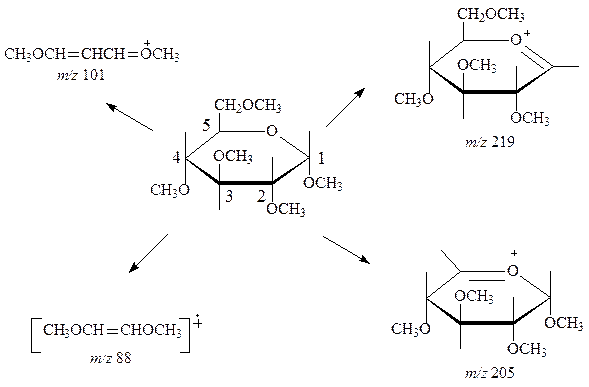
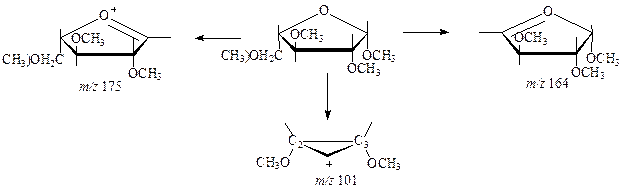
Используя масс-спектрометрию можно определить ациклический или циклический характер моносахаридов, а также количество циклов в молекуле углевода. Наиболее предсказуем распад ациклических производных. Масс-спектр линейного пентаацетата арабината содержит четыре характерных фрагмента с m / z 73, 145, 217 и 289 [ Ошибка! Закладка не определена. ], образующихся по нижеприведенной схеме:
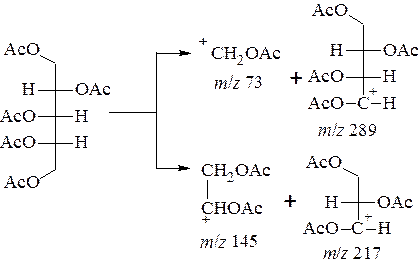
Масс-спектр циклического тетраацетил-метил-a-глюкопиранозида, являющегося структурным изомером ациклического пентаацетата арабината, содержит не все описанные выше характерные фрагменты распада молекулярного иона ациклического моносахарида (см. рис. 6, табл. 7).
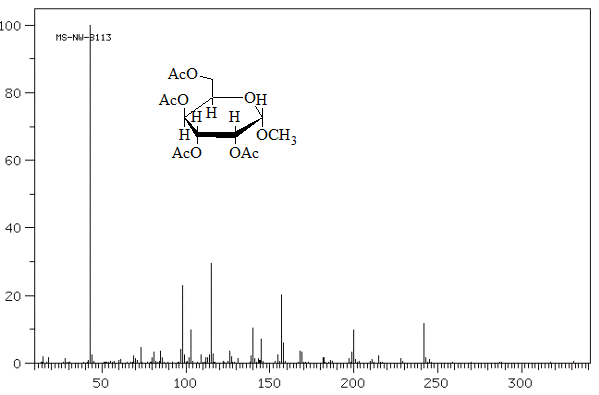
Рис. 6. Масс-спектр тетраацетата метил-a-глюкопиранозида
Таблица 7
Пики ионов в масс-спектре тетраацетата метил-a-глюкопиранозида
| Ион, m/z | Интенсивность сигнала, I | Ион, m/z | Интенсивность сигнала, I | Ион, m/z | Интенсивность сигнала, I |
| 15.0 | 1 | 102.0 | 1 | 155.0 | 2 |
| 18.0 | 1 | 103.0 | 9 | 157.0 | 20 |
| 42.0 | 0 | 109.0 | 2 | 158.0 | 5 |
| 43.0 | 100 | 112.0 | 1 | 168.0 | 3 |
| 44.0 | 2 | 113.0 | 1 | 169.0 | 3 |
| 61.0 | 1 | 114.0 | 2 | 182.0 | 1 |
| 69.0 | 2 | 115.0 | 29 | 197.0 | 1 |
| 70.0 | 1 | 116.0 | 2 | 199.0 | 3 |
| 73.0 | 4 | 126.0 | 3 | 200.0 | 9 |
| 80.0 | 1 | 127.0 | 2 | 201.0 | 1 |
| 81.0 | 3 | 131.0 | 1 | 211.0 | 1 |
| 85.0 | 3 | 139.0 | 2 | 215.0 | 2 |
| 86.0 | 1 | 140.0 | 10 | 228.0 | 1 |
| 97.0 | 4 | 141.0 | 1 | 242.0 | 11 |
| 98.0 | 22 | 143.0 | 1 | 243.0 | 1 |
| 99.0 | 2 | 145.0 | 7 | 245.0 | 1 |
Масс-спектр a-D-маннопиранозы (рис. 7) содержит характерные для углеводов фрагменты распада молекулярного иона, это ионы с m / z 73 (максимальная интенсивность) и 31 (I 89%) (табл. 8).
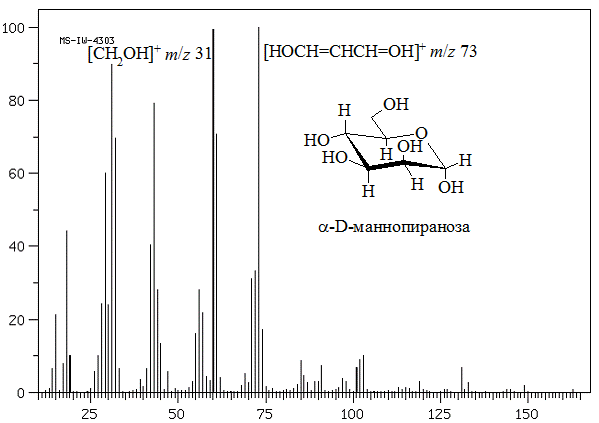
Рис. 7. Масс-спектр a-D-маннопиранозы
Таблица 8
Пики ионов в масс-спектре a-D-маннопиранозы
| Ион, m/z | Интенсивность сигнала, I | Ион, m/z | Интенсивность сигнала, I | Ион, m/z | Интенсивность сигнала, I | Ион, m/z | Интенсивность сигнала, I |
| 13.0 | 1 | 40.0 | 1 | 61.0 | 70 | 89.0 | 2 |
| 14.0 | 6 | 41.0 | 6 | 62.0 | 4 | 90.0 | 3 |
| 15.0 | 21 | 42.0 | 40 | 68.0 | 2 | 91.0 | 7 |
| 17.0 | 7 | 43.0 | 79 | 69.0 | 5 | 96.0 | 1 |
| 18.0 | 44 | 44.0 | 28 | 70.0 | 2 | 97.0 | 3 |
| 19.0 | 10 | 45.0 | 13 | 71.0 | 31 | 98.0 | 3 |
| 25.0 | 1 | 47.0 | 5 | 72.0 | 33 | 101.0 | 6 |
| 26.0 | 5 | 49.0 | 1 | 73.0 | 100 | 102.0 | 8 |
| 27.0 | 10 | 53.0 | 1 | 74.0 | 17 | 103.0 | 10 |
| 28.0 | 24 | 54.0 | 3 | 75.0 | 1 | 113.0 | 1 |
| 29.0 | 60 | 55.0 | 16 | 77.0 | 1 | 115.0 | 1 |
| 30.0 | 23 | 56.0 | 28 | 83.0 | 1 | 116.0 | 1 |
| 31.0 | 89 | 57.0 | 21 | 84.0 | 2 | 119.0 | 2 |
| 32.0 | 69 | 58.0 | 4 | 85.0 | 8 | 131.0 | 6 |
| 33.0 | 6 | 59.0 | 3 | 86.0 | 4 | 133.0 | 2 |
| 39.0 | 3 | 60.0 | 99 | 87.0 | 2 | 149.0 |
|
|
|
|
|
Дата добавления: 2015-07-13; Просмотров: 3478; Нарушение авторских прав?; Мы поможем в написании вашей работы!