
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Определение количества углеводов 1 страница
|
|
|
|
Определение общего содержания сахаров химическими методами
Химические методы определения сахаров основаны на их редуцирующих свойствах, т. е. на их способности легко окисляться в щелочных растворах относительно слабыми окислителями. Это обусловливается наличием в сахарах карбонильной группы.
Редуцирующими свойствами обладают все простые сахара (моносахариды) и некоторые дисахариды: мальтоза, лактоза и целлобиоза. Поскольку в растительных продуктах содержатся как простые, так и сложные углеводы (крахмал, клетчатка и др.), то для определения общего их содержания предварительно необходимо провести гидролиз сложных углеводов и превратить их в простые редуцирующие сахара.
Окислителями при количественном определении сахаров являются фелинговая жидкость, йод, красная кровяная соль. Чаще других используют различные модификации метода, основанного на окисляющем действии фелинговой жидкости. Фелинговая жидкость представляет собой смесь двух растворов, первый из которых содержит раствор сернокислой меди (CuSO4•5Н2О), второй - раствор сегнетовой соли (калия-натрия виннокислого) и едкого натра. Концентрация этих растворов в зависимости от способа определения бывает различная. Растворы хранят отдельно, так как в смеси они неустойчивы. Смешивают их в равных количествах по объёму в момент проведения анализа.
При смешивании растворов сернокислая медь сначала реагирует со щелочью, образуя голубой осадок гидрата окиси меди:
CuSO4 + 2NaOH = Na2SO4 + Сu(ОН)2,
который с сегнетовой солью образует темно-синий раствор комплексного соединения:
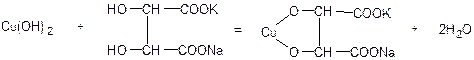
Следовательно, в фелинговой жидкости медь находится в виде комплексной соли. Эта соль легко растворима в воде, причём в водных растворах она содержит ион:
|
|
|

и поскольку этим исключено наличие иона меди, медь не осаждается щелочами. Таким образом, введение в раствор сегнетовой соли имеет целью исключительно растворению осадка гидрата окиси меди, образующегося при взаимодействии CuSO4 и 2NaOH.
Комплексное соединение при кипячении реагирует с редуцирующими веществами, при этом освобождается окись меди, которая в момент выделения отдает кислород на окисление сахаров и восстанавливается до закиси меди Cu2O, представляющую собой осадок красного цвета, нерастворимый в воде. По количеству Cu2O можно судить о содержании сахаров в растворе.
В частности, реакцию комплексной соли меди с глюкозой можно выразить уравнением:

Значительное влияние на реакцию оказывает воздух. В одинаковых условиях опыта Cu2O получается тем меньше, чем больше была поверхность соприкосновения кипящей смеси с воздухом.
Потеря меди объясняется тем, что одновременно с её восстановлением на поверхности жидкости идёт процесс окисления меди кислородом воздуха.
Немалую роль в образовании осадка играет также продолжительность нагревания, причём после 20-минутного нагревания увеличение идёт незначительно. Так, Кьельдаль нашёл, что нагревание в течение 5-10 минут даёт разницу на каждую минуту в 1 мг, тогда как при нагревании в течение 20-30 минут увеличение осадка составляло только 0,24 мг в минуту.
Определение количества образовавшейся закиси меди можно проводить весовыми и колориметрическими методами. Однако наиболее распространены следующие объемно-аналитические методы определения степени восстановления фелинговой жидкости: а) методы прямого титрования испытуемым раствором сахара точно измеренного количества фелинговой жидкости установленного типа. Конец реакции определяют при помощи различных индикаторов (метиленовой сини, красной кровяной соли и т. д.); б) метод перманганатометрического титрования, основанный на отделении осадка закиси меди, последующем окислении ее окисной солью железа и определения образующейся закиси железа перманганатометрическим титрованием. Это наиболее точный метод (одним из его вариантов является метод Бертрана); в) методы йодометрического титрования, основанные на непосредственном йодометрическом определении закиси меди или на предварительном ее окислении до окиси.
|
|
|
Подготовка образца продукта к испытанию. Непосредственному определению сахаров предшествует тщательное приготовление водной вытяжки из анализируемого продукта. Водная вытяжка не должна содержать дубильные, красящие и белковые вещества, которые могут исказить результаты. Удаляют их путем осаждения уксуснокислым свинцом в точно нейтральной среде, так как щелочная реакция способствует образованию свинцовых сахаров, а слабокислая может вызвать частичный гидролиз дисахаридов.
Навеску или точно измеренный объем исследуемого продукта берут так, чтобы получить в конечном фильтрате оптимальную для данного метода концентрацию сахара от 0,4 до 0,8%. Так, при 10%-ном содержании сахаров масса должна быть около 50 г, при меньшей сахаристости навеску продукта увеличивают, а при большей соответственно уменьшают. Навеску взвешивают с точностью до 0,01 г, переносят в мерную колбу вместимостью 500 мл, смывая стаканчик несколько раз дистиллированной водой в количестве не более 250 мл.
Органические кислоты, содержащиеся в навеске, нейтрализуют 15% – ным раствором углекислого натрия до рН = 7,0. Для определения рН применяют универсальную индикаторную бумагу. Для этого на фарфоровую пластинку или плоскодонную фарфоровую чашечку помещают с помощью тонко оттянутых пипеток или тоненьких стеклянных палочек 1 каплю индикатора и 1 каплю испытуемого раствора. Другой стеклянной палочкой смешивают эти капли и по образующейся окраске, пользуясь цветовой шкалой, приложенной к индикаторной бумаге, определяют рН испытуемого раствора.
После нейтрализации колбу с содержимым нагревают 15 мин на водяной бане при 80°С при частом взбалтывании, затем охлаждают до комнатной температуры и прибавляют 7 мл 30%-ного раствора нейтрального уксуснокислого свинца (раствор 2)*, хорошо перемешивают и отстаивают 5 мин. Осаждение, считают законченным после того, как жидкость над осадком станет прозрачной. В противном случае прибавляют дополнительно раствор уксуснокислого свинца. Только после появления над осадком прозрачного раствора в колбу добавляют 18 – 20 мл насыщенного раствора двузамещенного фосфорнокислого натрия или сернокислого натрия для осаждения избытка уксуснокислого свинца. Содержимое колбы взбалтывают и дают осадку отстояться (достаточно 10 мин). При осаждении сернокислым натрием, при мутном фильтрате жидкость отстаивают 24 ч. Полноту осаждения проверяют осторожным приливанием по стенке колбы нескольких капель раствора фосфорнокислого или сернокислого натрия. При помутнении раствора добавляют еще 8 – 10 мл одного из указанных выше растворов солей натрия, затем содержимое колбы взбалтывают, дают осадку отстояться и снова повторяют определение полноты осаждения избытка уксуснокислого свинца. При отсутствии помутнения в месте соприкосновения жидкостей колбу доливают дистиллированной водой до метки, содержимое тщательно перемешивают и через 1 – 2 мин фильтруют через сухой складчатый фильтр в сухой стакан. Получают фильтрат А для определения в нем инвертного сахара.
|
|
|
В навесках продуктов, содержащих нередуцирующие углеводы, проводят инверсию. Для этого пипеткой отбирают 50 мл фильтрата А в мерную колбу вместимостью 100 мл, прибавляют 5 мл концентрированной соляной кислоты (плотностью 1,19 г/см3). Полученный раствор нагревают на водяной бане 8 мин при температуре 68 – 70°С.
После инверсии охлажденный раствор осторожно нейтрализуют, приливая по капле 20%-ный раствор NaOH, а к концу нейтрализации 0,1 н раствор NaOH (раствор 1 в). Конец нейтрализации проверяют по лакмусовой бумажке, опущенной в колбу, по универсальному индикатору или приливанием метилового оранжевого до появления желто-оранжевой краски. Далее раствор охлаждают и доводят дистиллированной водой до объема 100 мл. Желательно в отдельной колбе заранее определить количество 20%-ного и 0,1 н растворов NaOH, необходимое для нейтрализации 5 мл концентрированной соляной кислоты.
|
|
|
Перманганатный метод по Бертрану
Ход определения. В сухую коническую колбу вместимостью 150 – 200 мл отмеряют пипеткой 20 мл нейтральной или слабокислой по лакмусу вытяжки после инверсии и последовательно вносят по 20 мл первого (раствор 3 б) и второго (раствор 4 а) растворов Фелинга. Смесь нагревают до кипения и кипятят ровно 3 мин, применяя песочные часы. Затем колбу снимают с огня, ставят в наклонном положении в фарфоровую чашечку для лучшего оседания выпавшего осадка закиси меди и фильтруют прозрачную горячую жидкость через стеклянный фильтр в колбу Бунзена, создавая вакуум при помощи водоструйного насоса или насоса Комовского. Фильтрат должен иметь синюю окраску. Бледная окраска фильтрата указывает на недопустимо высокое содержание сахара в испытуемом растворе. Осадок закиси промывают в конической колбе 3 – 4 раза небольшим количеством горячей дистиллированной воды, каждый раз дают воде отстояться и фильтруют через тот же фильтр, стараясь не переносить на него осадок. Осадок должен все время находиться под тонким слоем воды, чтобы не соприкасаться с воздухом. Промывание заканчивают, когда исчезнет голубоватый оттенок промывной воды.
Фильтрат из колбы Бунзена выливают, тщательно ополаскивают ее дистиллированной водой и вновь закрывают пробкой с фильтр-воронкой и стеклянным фильтром. Промытый осадок в конической колбе заливают небольшими порциями раствором сернокислого окисного железа (раствор 19) или раствором железоаммонийных квасцов (раствор 20 а) до полного его растворения. Общее количество раствора сернокислого окисного железа не должно превышать 20 мл. Закись меди окисляется вследствие перехода окисной формы железа в закисную:
Cu2O + Fe2(SO4)3 + H2SO4 = 2CuSO4 + 2FeSO4 + H2O
При этом образуется прозрачная светло-зеленая жидкость, которую фильтруют через тот же стеклянный фильтр в колбу Бунзена под вакуумом. В случае попадания на поверхность фильтра осадка закиси меди его при помощи перемешивания стеклянной палочкой растворяют в растворе. Затем коническую колбу и фильтр 3 – 4 раза промывают небольшими порциями горячей дистиллированной воды, собирая промывные воды в колбу Бунзена под вакуумом.
Фильтрат, содержащий закисное сернокислое железо FeSO4 в количестве, эквивалентном бывшей раньше в осадке закиси меди, оттитровывают 0,1 н раствором перманганата калия (раствор 5 а) до появления устойчивой розовой окраски. Перманганат калия в кислой среде окисляет железо в окисное:
2KMnO4 + 10FeSO4 + 8H2SO4 = 5Fe2(SO4)3 + 2MnSO4 + K2SO4 + 8H2O
Умножая число израсходованных мл перманганата калия на его титр по меди, определяют количество мг меди. Если раствор перманганата точно 0,1 н, то 1 мл KMnO4 соответствует 6,36 мг меди и количество осажденной меди, мг, будет равно Х = 6,36 × а, где а – количество 0,1 н раствора KMnO4, пошедшее на титрование исследуемого раствора, мл.
По установленному количеству меди находят по таблица 1 соответствующее количество сахара. Учитывая разведение, содержание сахара (X, %) определяют по формуле:
Х = g×V1×V2×100/(G×V×V3×1000),
где G – навеска продукта, г; g – количество инвертного сахара, найденное по табл. 8, мг; V1 – объем вытяжки, приготовленный из навески (фильтрат А), мл; V2 – объем, до которого раствор доведен после инверсии, мл; V – объем испытуемого раствора (фильтрата А), взятый для инверсии, мл; V3 – объем раствора после инверсии, взятый для определения сахара, мл
Вычисление производят с точностью до 0,1%. Конечным результатом считают среднее арифметическое двух параллельных определений, расхождение между которыми не должно превышать 0,5%. Перманганатный метод по Макс-Мюллеру. Эта модификация перманганатного метода отличается от вышеописанной приготовлением, концентрацией и объемом растворов реактивов.
Ход определения. В сухую коническую колбу последовательно вносят пипеткой по 25 мл растворов Фелинга I (раствор 3 а) и Фелинга II (раствор 4 б). Смесь быстро нагревают до кипения и сразу приливают 50 мл раствора, полученного после инверсии. Содержимое колбы доводят до кипения и кипятят ровно 2 мин. По окончании нагревания выпавшему осадку закиси меди дают отстояться. Раствор над осадком должен быть синим от избытка ионов меди. Если раствор над осадком обесцвечивается, то определение повторяют с меньшим, точно измеренным количеством фильтрата А с добавлением в коническую колбу дистиллированной воды в таком объеме, который составил бы вместе со взятым количеством испытуемого раствора 50 мл. Затем прозрачную жидкость над выпавшим осадком закиси меди фильтруют через стеклянный фильтр в колбу Бунзена при слабом разрежении, избегая по возможности перенесения осадка на фильтр. Осадок промывают 3 – 4 раза небольшими порциями горячей дистиллированной воды, давая ему каждый раз осесть на дно колбы и оставляя его покрытым жидкостью во избежание окисления закиси меди. После этого приступают к растворению осадка в 30 – 50 мл раствора железо-аммонийных квасцов (раствор 20 б), описанному в методе Бертрана. Полученный фильтрат тотчас же титруют раствором перманганата калия (раствор 5 б) до неисчезающей слабо-розовой окраски. Для определения меди (в мг) количество мл марганцево-кислого калия, пошедшее на титрование, умножают на 10 и на поправочный коэффициент К раствора перманганата калия. После этого по таблица 2 находят соответствующее количество инвертного сахара во взятом объеме раствора после инверсии. Учитывая разведение, общее содержание сахара вычисляют по формуле, указанной в описании метода Бертрана.
Прямое титрование фелинговой жидкости сахарным раствором в присутствии метиленовой сини. Метод также основан на реакции окисления редуцирующих сахаров фелинговой жидкостью, которая титруется непосредственно испытуемым сахарным раствором до полного восстановления окисной меди до закисной. Конец реакции устанавливают по индикатору метиленовому голубому, являющемуся прекрасным акцептором водорода. В кипящем щелочном растворе, как только вся окись меди восстановится до закисной, первая капля сахарного раствора начнет реагировать с метиленовой синью и восстановит ее. При этом синяя окраска раствора перейдет в красновато-оранжевую, поэтому конец реакции установить легко.
Ход определения. В коническую колбу вместимостью 100 мл приливают разными пипетками по 5 мл Фелинг I (раствор 3 а) и Фелинг II (раствор 4 б) и смесь доводят до кипения за 2 мин. Затем из бюретки с боковым краном и хорошо притертой пробкой, не прекращая кипения жидкости в колбе, приливают испытуемый раствор сахаров (фильтрат А или раствор после инверсии) до тех пор, пока синий цвет кипящей смеси не изменится на красновато-оранжевый. После этого добавляют 5 капель 1%-ного раствора метиленового голубого (раствор 21) и продолжают, не прерывая умеренное кипячение, прибавлять из бюретки небольшими порциями испытуемый раствор, пока не исчезнет синяя окраска и взмучиваемый при кипячении осадок меди не окрасит всю смесь в красновато-оранжевый цвет. На все титрование должно уходить не более 4 мин. Объем израсходованного на титрование испытуемого раствора регистрируют и считают ориентировочным. Для получения более точных данных определение повторяют. При этом в колбу с 10 мл фелинговой жидкости приливают из вновь заполненной бюретки испытуемый раствор в количестве на 1 мл меньше, чем было затрачено при первом опыте. Далее смесь доводят до кипения также за 2 мин, прибавляют 5 капель метиленовой сини и в течение 1 мин дотитровывают при кипячении испытуемым раствором до исчезновения синего окрашивания. Для расчета принимают данные повторного опыта как более достоверные. Количество инвертного сахара в 100 мл испытуемого раствора находят по табл. 10.
Таблица 1
Данные для расчета сахара по количеству меди по методу Бертрана
| Количество меди, мг | Содержание инвертного сахара по методу Бертрана (мг) | |||||||||
| Количество меди, 0,1 мг | ||||||||||
| 0,0 | 0,1 | 0,2 | 0,3 | 0,4 | 0,5 | 0,6 | 0,7 | 0,8 | 0,9 | |
| 0,5 | 0,54 | 0,59 | 0,63 | 0,68 | 0,72 | 0,77 | 0,81 | 0,83 | ||
| 0,90 | 0,95 | 1,00 | 1,04 | 1,09 | 1,1З | 1,18 | 1,22 | 1,27 | 1,31 | |
| 1,36 | 1,40 | 1,45 | 1,50 | 1,54 | 1,59 | 1,63 | 1,68 | 1,72 | 1,77 | |
| 1,81 | 1,83 | 1,90 | 1,95 | 2,0 | 2,04 | 2,09 | 2,13 | 2,18 | 2,22 | |
| 2,27 | 2,31 | 2,36 | 2,40 | 2,45 | 2,50 | 2,55 | 2,60 | 2,65 | 2,70 | |
| 2,75 | 2,80 | 2,85 | 2,90 | 2,95 | 3,0 | 3,05 | 3,10 | 3,15 | 3,20 | |
| 3,25 | 3,30 | 3,35 | 3,40 | 3,45 | 3,50 | 3,55 | 3,60 | 3,65 | 3,70 | |
| 3,75 | 3,80 | 3,85 | 3,90 | 3,95 | 4,00 | 4,05 | 4,10 | 4,15 | 4,20 | |
| 4,25 | 4,30 | 4,35 | 4,40 | 4,45 | 4,50 | 4,55 | 4,60 | 4,65 | 4,70 | |
| 4,75 | 4,80 | 4,85 | 4,90 | 4,95 | 5,00 | 5,05 | 5,10 | 5,15 | 5,20 | |
| 5,25 | 5,30 | 5,35 | 5,40 | 5,45 | 5,50 | 5,55 | 5,60 | 5,65 | 5,70 | |
| 5,75 | 5,80 | 5,85 | 5,90 | 5,95 | 6,00 | 6,05 | 6,10 | 6,15 | 6,20 | |
| 6,25 | 6,30 | 6,35 | 6,40 | 6,45 | 6,50 | 6,55 | 6,60 | 6,65 | 6,70 | |
| 6,75 | 6,80 | 6,95 | 6,90 | 6,95 | 7,00 | 7,05 | 7,10 | 7,15 | 7,20 | |
| 7,25 | 7,30 | 7,35 | 7,40 | 7,45 | 7,50 | 7,55 | 7,60 | 7,65 | 7,70 | |
| 7,75 | 7,80 | 7,85 | 7,90 | 7,95 | 8,00 | 8,05 | 8,10 | 8,15 | 8,20 | |
| 8,25 | 8,30 | 8,35 | 8,40 | 8,45 | 8,50 | 8,55 | 8,60 | 8,65 | 8,70 | |
| 8,75 | 8,80 | 8,85 | 8,90 | 8,95 | 9,00 | 9,05 | 9,10 | 9,15 | 9,20 | |
| 9,25 | 9,30 | 9,35 | 9,40 | 9,45 | 9,50 | 9,54 | 9,58 | 9,62 | 9,66 | |
| 9,70 | 9,75 | 9,80 | 9,85 | 9,90 | 9,95 | 10,00 | 10,05 | 10,00 | 10,15 | |
| 10,20 | 10,25 | 10,30 | 10,35 | 10,40 | 10,45 | 10,50 | 10,55 | 10,60 | 10,65 | |
| 10,70 | 10,75 | 10,80 | 10,85 | 10,90 | 10,95 | 11,00 | 11,05 | 11,10 | 11,15 | |
| 11,20 | 11,25 | 11,30 | 11,35 | 11,40 | 11,45 | 11,50 | 11,50 | 11,60 | 11,65 | |
| 11,70 | 11,75 | 11,80 | 11,85 | 11,90 | 11,95 | 12,00 | 12,05 | 12,10 | 12,15 | |
| 12,21 | 12,26 | 12,31 | 12,36 | 12,42 | 12,47 | 12,52 | 12,57 | 12,63 | 12,68 | |
| 12,73 | 12,78 | 12,84 | 12,89 | 12,94 | 13,00 | 13,05 | 13,10 | 13,15 | 13,20 | |
| 13,25 | 13,30 | 13,35 | 13,40 | 13,45 | 13,50 | 13,55 | 13,60 | 13,65 | 13,70 | |
| 13,75 | 13,80 | 13,85 | 13,90 | 13,95 | 14,00 | 14,05 | 14,10 | 14,15 | 14,20 | |
| 14,25 | 14,30 | 14,35 | 14,40 | 14,45 | 14,50 | 14,55 | 14,60 | 14,65 | 14,70 | |
| 14,75 | 14,80 | 14,85 | 14,90 | 14,95 | 15,00 | 15,05 | 15,10 | 15,15 | 15,20 | |
| 15,25 | 15,30 | 15,35 | 15,40 | 15,45 | 15,50 | 15,55 | 15,60 | 15,65 | 15,70 | |
| 15,75 | 15,80 | 15,85 | 15,90 | 15,95 | 16,00 | 16,05 | 16,10 | 16,15 | 16,20 | |
| 16,25 | 16,30 | 16,35 | 16,40 | 16,45 | 16,50 | 16,55 | 16,60 | 16,65 | 16,70 | |
| 16,75 | 16,80 | 16,85 | 16,90 | 16,95 | 17,00 | 17,05 | 17,10 | 17,15 | 17,21 | |
| 17,26 | 17,31 | 17,36 | 17,42 | 17,47 | 17,52 | 17,57 | 17,63 | 17,68 | 17,73 | |
| 17,78 | 17,84 | 17,89 | 17,94 | 18,00 | 18,05 | 18,20 | 18,15 | 18,20 | 18,25 | |
| 18,30 | 18,35 | 18,40 | 18,45 | 18,50 | 18,55 | 18,60 | 18,65 | 18,70 | 18,75 | |
| 18,80 | 18,85 | 18,90 | 18,95 | 19,00 | 19,05 | 19,10 | 19,15 | 19,20 | 19,25 | |
| 19,30 | 19,35 | 19,40 | 19,45 | 19,50 | 19,55 | 19,60 | 19,65 | 19,70 | 19,75 | |
| 19,80 | 19,85 | 19,90 | 19,95 | 20,00 | 20,05 | 20,10 | 20,15 | 20,21 | 20,26 | |
| 41' | 20,31 | 20,36 | 20,42 | 20,47 | 20,52 | 20,57 | 20,63 | 20,68 | 20,73 | 20,78 |
| 20,84 | 20,89 | 20,94 | 21,00 | 21,05 | 21,10 | 21,15 | 21,21 | 21,26 | 21,31 | |
| 21,36 | 21,42 | 21,47 | 21,52 | 21,57 | 21,63 | 21,38 | 21,73 | 21,78 | 21,84 | |
| 21,89 | 21,94 | 22,00 | 22,05 | 22,10 | 22,15 | 22,21 | 22,26 | 22,31 | 22,36 | |
| 22,42 | 22,47 | 22,52 | 22,57 | 22,63 | 22,68 | 22,73 | 22,78 | 22,84 | 22,89 | |
| 22,94 | 23,00 | 23,05 | 23,10 | 23,15 | 23,21 | 23,26 | 23,31 | 23,36 | 23,42 | |
| 23,47 | 23,52 | 23,57 | 23,63 | 23,68 | 23,73 | 23,78 | 23,84 | 23,89 | 23,94 | |
| 24,00 | 24,05 | 24,11 | 24,16 | 24,22 | 24,27 | 24,33 | 24,38 | 24,44 | 24,50 | |
| 24,55 | 24,61 | 24,66 | 24,72 | 24,77 | 24,83 | 24,88 | 24,94 | 25,00 | 25,05 | |
| 25,10 | 25,15 | 25,21 | 25,26 | 25,31 | 25,36 | 25,42 | 25,47 | 25,52 | 25,57 | |
| 25,63 | 25,68 | 25,73 | 25,78 | 25,84 | 25,89 | 25,94 | 26,00 | 26,05 | 26,10 | |
| 26,15 | 26,21 | 26,26 | 26,31 | 26,36 | 26,42 | 26,47 | 26,52 | 26,57 | 26,63 | |
| 26,68 | 26,73 | 26,78 | 26,84 | 26,89 | 26,94 | 27,00 | 27,05 | 27,10 | 27,15 | |
| 27,21 | 27,26 | 27,31 | 27,36 | 27,42 | 27,47 | 27,52 | 27,57 | 27,63 | 27,68 | |
| 27,73 | 27,78 | 27,84 | 27,89 | 27,94 | 28,00 | 28,05 | 28,10 | 28,15 | 28,21 | |
| 28,26 | 28,31 | 28,36 | 28,42 | 28,47 | 28,52 | 28,57 | 28,63 | 28,68 | 28,73 | |
| 28,78 | 28,84 | 28,89 | 28,94 | 29,00 | 29,05 | 29,10 | 29,15 | 29,21 | 29,26 | |
| 29,31 | 29,36 | 29,42 | 29,47 | 29,52 | 29,57 | 29,63 | 29,68 | 29,73 | 29,78 | |
| 29,84 | 29,89 | 29,94 | 30,00 | 30,05 | 30,11 | 30,16 | 30,22 | 30,27 | 30,33 | |
| 30,68 | 30,44 | 30,50 | 30,55 | 30,61 | 30,66 | 30,72 | 30,77 | 30,83 | 30,88 | |
| 30,94 | 31,00 | 31,05 | 31,10 | 31,15 | 31,21 | 31,26 | 31,31 | 31,36 | 31,42 | |
| 31,47 | 31,52 | 31,57 | 31,63 | 31,68 | 31,73 | 31,78 | 31,84 | 31,89 | 31,94 | |
| 32,00 | 32,05 | 32,11 | 32,16 | 32,22 | 32,27 | 32,33 | 32,38 | 32,44 | 32,50 | |
| 32,55 | 32,61 | 32,66 | 32,72 | 32,77 | 32,83 | 32,88 | 32,94 | 33,00 | 33,05 | |
| 33,10 | 33,15 | 33,21 | 33,26 | 33,31 | 33,36 | 33,42 | 33,47 | 33,52 | 33,57 | |
| 33,63 | 33,68 | 33,73 | 33,78 | 33,84 | 33,89 | 33,94 | 34,00 | 34,05 | 34,11 | |
| 34,16 | 34,72 | 34,27 | 34,33 | 34,38 | 34,44 | 34,50 | 34,55 | 34,61 | 34,66 | |
| 34,72 | 34,77 | 34,83 | 34,88 | 34,94 | 35,00 | 35,05 | 35,11 | 35,16 | 35,22 | |
| 35,27 | 35,33 | 35,38 | 35,44 | 35,50 | 35,55 | 35,61 | 35,66 | 35,72 | 35,77 | |
| 35,83 | 35,88 | 35,94 | 36,00 | 36,05 | 36,10 | 36,15 | 36,21 | 36,26 | 36,31 | |
| 36,36 | 36,42 | 36,47 | 36,52 | 36,57 | 36,63 | 36,68 | 36,43 | 36,78 | 36,84 | |
| 36,89 | 36,94 | 37,00 | 37,05 | 37,11 | 37,16 | 37,22 | 37,27 | 37,33 | 37,38 | |
| 37,44 | 37,50 | 37,55 | 37,61 | 37,66 | 37,72 | 37,77 | 37,83 | 37,88 | 37,94 | |
| 38,00 | 38,05 | 38,10 | 38,15 | 38,21 | 38,26 | 38,31 | 38,36 | 38,42 | 38,47 | |
| 38,52 | 38,57 | 38,63 | 38,68 | 38,73 | 38,78 | 38,84 | 38,89 | 38,94 | 39,00 | |
| 39,05 | 39,11 | 39,16 | 39,22 | 39,27 | 39,33 | 39,38 | 39,44 | 39,50 | 39,55 | |
| 39,61 | 39,66 | 39,72 | 39,77 | 39,83 | 39,88 | 39,94 | 40,00 | 40,05 | 40,11 | |
| 40,16 | 40,22 | 40,27 | 40,33 | 40,38 | 40,44 | 40,50 | 40,55 | 40,61 | 40,66 | |
| 40,72 | 40,77 | 40,83 | 40,88 | 40,94 | 41,00 | 41,05 | 41, 11. | 41,17 | 41,23 | |
| 41,29 | 41,35 | 41,41 | 41,47 | 41,52 | 41,58 | 41,64 | 41,70 | 41,70 | 41,82 | |
| 41,88 | 41,94 | 42,00 | 42,05 | 42,11 | 42,16 | 42,22 | 42,27 | 42,33 | 42,38 | |
| 42,44 | 42,50 | 42,55 | 42,61 | 42,66 | 42,72 | 42,77 | 42,83 | 42,88 | 42,94 | |
| 43,00 | 43,05 | 43,11 | 43,16 | 43,22 | 43,27 | 43,33 | 43,38 | 43,44 | 43,50 | |
| 43,50 | 43,61 | 43,66 | 43,72 | 43,77 | 43,83 | 43,88 | 43,94 | 44,00 | 44,05 | |
| 44,11 | 44,16 | 44,23 | 44,29 | 44,35 | 44,41 | 44,47 | 44,52 | 44,58 | 44,64 | |
| 44,70 | 44,76 | 44,82 | 44,88 | 44,94 | 45,00 | 45,05 | 45,11 | 45,16 | 45,22 | |
| 45,27 | 45,33 | 45,38 | 45,44 | 45,50 | 45,55 | 45,61 | 45,66 | 45,72 | 45,77 | |
| 45,83 | 45,88 | 45,94 | 46,00 | 46,05 | 46,11 | 46,16 | 46,22 | 46,27 | 46,33 | |
| 46,38 | 46,44 | 46,50 | 46,55 | 46,61 | 46,66 | 46,72 | 46,77 | 46,83 | 46,88 | |
| 46,94 | 47,00 | 47,05 | 47,11 | 47,16 | 47,22 | 47,27 | 47,33 | 47,38 | 47,44 | |
| 47,50 | 47,55 | 47,61 | 47,66 | 47,72 | 47,77 | 47,83 | 47,88 | 47,94 | 48,00 | |
| 48,05 | 48,11 | 48,17 | 48,23 | 48,29 | 48,35 | 48,41 | 48,47 | 48,52 | 48,58 | |
| 48,94 | 48,70 | 48,76 | 48,82 | 48,88 | 48,94 | 49,00 | 49,05 | 49,11 | 49,16 | |
| 49,32 | 49,27 | 49,33 | 49,38 | 49,44 | 49,50 | 49,55 | 49,61 | 49,66 | 49,72 | |
| 49,77 | 49,83 | 49,88 | 49,94 | 50,00 | 50,05 | 50,11 | 50,17 | 50,23 | 50,29 | |
| 50,35 | 50,41 | 50,47 | 50,52 | 50,58 | 50,64 | 50,70 | 50,76 | 50,82 | 50,88 | |
| 50,94 | 51,00 | 51,05 | 51,11 | 51,17 | 51,23 | 51,28 | 51,35 | 51,41 | 51,47 | |
| 51,52 | 51,58 | 51,64 | 51,70 | 51,76 | 51,82 | 51,88 | 51,94 | 52,00 | 52,05 | |
| 52,11 | 52,16 | 52,22 | 52,27 | 52,33 | 52,38 | 52,44 | 52,50 | 52,55 | 52,61 | |
| 52,66 | 52,72 | 52,77 | 52,83 | 52,88 | 52,94 | 53,00 | 53,05 | 53,11 | 53,17 | |
| 53,23 | 53,29 | 53,35 | 53,41 | 53,47 | 53,52 | 53,58 | 53,64 | 53,70 | 53,76 | |
| 53,83 | 53,88 | 53,94 | 54,00 | 54,05 | 54,11 | 54,17 | 54,23 | 54,29 | 54,35 | |
| 54,41 | 54,47 | 54,52 | 54,58 | 54,64 | 54,70 | 54,76 | 54,82 | 54,88 | 54,94 | |
| 55,00 | 55,05 | 55,11 | 55,17 | 55,23 | 55,29 | 55,35 | 55,41 | 55,47 | 55,52 | |
| 55,58 | 55,64 | 55,70 | 55,76 | 55,82 | 55,88 | 55,94 | 56,00 | 56,05 | 56,11 | |
| 56,17 | 56,23 | 56,29 | 56,35 | 56,41 | 56,47 | 56,52 | 56,58 | 56,64 | 56,70 | |
| 56,76 | 56,82 | 56,88 | 56,94 | 57,00 | 57,05 | 57,11 | 57,16 | 57,22 | 57,27 | |
| 57,33 | 57,38 | 57,44 | 57,50 | 57,55 | 57,61 | 57,66 | 57,72 | 57,77 | 57,83 | |
| 57,88 | 57,94 | 58,00 | 58,05 | 58,11 | 58,17 | 58,23 | 58,29 | 58,35 | 58,41 | |
| ПО | 58,47 | 58,52 | 58,58 | 58,64 | 58,70 | 58,76 | 58,82 | 58,88 | 58,94 | 59,00 |
| 59,05 | 59,11 | 59,17 | 59,23 | 59,29 | 59,35 | 59,41 | 59,47 | 59,52 | 59,58 | |
| 59,64 | 59,70 | 59,76 | 59,82 | 59,88 | 59,94 | 60,00 | 60,05 | 60,11 | 60,17 | |
| ИЗ | 60,23 | 60,29 | 60,35 | 60,41 | 60,47 | 60,52 | 60,58 | 60,64 | 60,70 | 60,76 |
| 60,82 | 60,88 | 60,94 | 61,00 | 61,06 | 61,12 | 61,18 | 61,25 | 61,31 | 61,37 | |
| 61,43 | 61,50 | 61,56 | 61,62 | 61,68 | 61,75 | 61,81 | 61,87 | 61,93 | 62,00 | |
| 62,05 | 62,11 | 62,17 | 62,23 | 62,29 | 62,35 | 62,41 | 62,47 | 62,52 | 62,58 | |
| 62,64 | 62,70 | 62,76 | 62,82 | 62,88 | 62,94 | 63,00 | 63,06 | 63,12 | 63,18 | |
| 63,25 | 63,31 | 63,37 | 63,43 | 63,50 | 63,56 | 63,52 | 63,68 | 63,75 | 63,81 | |
| 63,87 | 63,93 | 64,00 | 64,05 | 64,11 | 64,17 | 64,23 | 64,29 | 64,35 | 64,41 | |
| 64,47 | 64,52 | 64,58 | 64,64 | 64,70 | 64,76 | 64,82 | 64,88 | 64,94 | 65,00 | |
| 65,05 | 65,11 | 65,17 | 65,23 | 65,29 | 65,35 | 65,41 | 65,47 | 65,52 | 65,58 | |
| 65,64 | 65,70 | 65,76 | 65,82 | 65,88 | 65,94 | 66,00 | 66,06 | 66,12 | 66,18 | |
| 66,25 | 66,31 | 66,67 | 66,43 | 66,50 | 66,56 | 66,62 | 66,68 | 66,75 | 66,81 | |
| 66,87 | 66,93 | 67,00 | 67,05 | 67,11 | 67,17 | 67,23 | 67,29 | 67,35 | 67,41 | |
| 67,47 | 67,52 | 67,58 | 67,64 | 67,70 | 67,76 | 67,82 | 67,88 | 67,94 | 68,00 |
Таблица 2
|
|
|
|
|
Дата добавления: 2015-07-13; Просмотров: 799; Нарушение авторских прав?; Мы поможем в написании вашей работы!