
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Стандартные электродные потенциалы в водных растворах при 250С
|
|
|
|
Величины коэффициентов Mn для вычисления стандартного изменения энергии Гиббса по методу Темкина и Шварцмана
| Т, К | М0 | М1 ·10–3 | М2 ·10–6 | М-2 ·105 |
| 0,0000 0,0392 0,1133 0,1962 0,2794 0,3597 0,4361 0,5088 0,5765 0,6410 0,7019 0,7595 0,8141 0,8665 0,9162 0,9635 1,009 1,0525 1,094 1,134 1,173 1,210 1,246 1,280 1,314 1,346 1,3775 1,408 | 0,0000 0,0130 0,0407 0,0759 0,1153 0,1574 0,2012 0,2463 0,2922 0,3389 0,3860 0,4336 0,4814 0,5296 0,5780 0,6265 0,6752 0,7240 0,7730 0,8220 0,8711 0,9203 0,9696 1,0189 1,0683 1,1177 1,1672 1,2166 | 0,0000 0,0043 0,0140 0,0303 0,0498 0,0733 0,1004 0,1310 0,1652 0,2029 0,2440 0,2886 0,3362 0,3877 0,4424 0,5005 0,5619 0,6265 0,6948 0,7662 0,8411 0,9192 1,0008 1,0856 1,1738 1,2654 1,3603 1,4585 | 0,0000 0,0364 0,0916 0,1423 0,1853 0,2213 0,2521 0,2783 0,2988 0,3176 0,3340 0,34835 0,3610 0,3723 0,3824 0,3915 0,3998 0,4072 0,4140 0,4203 0,4260 0,4314 0,4363 0,4408 0,44505 0,4490 0,4527 0,4562 |
Таблица 7.4
| Электрод | Реакция | φо, В | |
| Электроды, обратимые относительно катиона | |||
| Li+, Li | Li+ + e → Li | –3,045 | |
| Аl3+, Аl | Аl3+ + 3 e → Аl | –1,662 | |
| Zn2+, Zn | Zn2+,+2 e → Zn | –0,763 | |
| Fe2+, Fe | Fe2+ + 2 e → Fe | –0,440 | |
| Cd2+, Cd | Cd2+ + 2 e → Cd | –0,403 | |
| Ni2+, Ni | Ni2+ + 2 e → Ni | –0,250 | |
| Sn2+, Sn | Sn2+ + 2 e → Sn | –0,136 | |
| Pb2+, Pb | Pb2+ + 2 e → Pb | –0,126 | |
| Fe3+, Fe | Fe3+ + 3 e → Fe | –0,036 | |
| Cu2+, Cu | Cu2+ + 2 e → Cu | +0,337 | |
| Cu+, Cu | Cu+ + e → Cu | +0,521 | |
| Ag+, Ag | Ag+ + e → Ag | +0,799 | |
| Hg2+, Hg | Hg22+ + 2 e → Hg | +0,854 | |
| Электроды, обратимые относительно аниона | |||
| Se, Se 2– | Se + 2 e → Se 2– | –0,92 | |
| S, S 2– | S + 2 e → S 2– | –0,447 | |
| Br2(ж), Br - | ½ Br2 + e → Br – | +1,065 | |
| Газовые электроды | |||
| H+, H2 | H+ + e → ½ H2 | 0,000 | |
| O2, OH- | ½ O2 + H2O + 2 e →2 OH– | +0,401 | |
| Cl2(г), Cl– | ½ Cl2 + e → Cl– | +1,360 | |
| F2, F– | ½ F2 + e → F– | +2,870 | |
| Электроды второго рода | |||
| Al, Al(OH)3, OH- | Al(OH)3 + 3 e → Al + 3 OH– | –2,300 | |
| Zn, Zn(OH)2, OH- | Zn(OH)2 + 2 e → Zn + 2 OH– | –1,245 | |
| Cd, Cd(OH)2, OH- | Cd(OH)2 + 2 e → Cd + 2 OH– | –0,809 | |
| Pb, PbSO4, SO42- | PbSO4 + 2 e → Pb + SO42- | –0,359 | |
| Ag, AgCl, Cl- | AgCl + e → Ag + Cl– | +0,222 | |
| Hg, Hg2Cl2, Cl- | ½ Hg2Cl2 + e → Hg + Cl– | +0,268 | |
| Ag, Ag2SO4, SO42- | Ag2SO4 + 2 e → 2 Ag + SO42– | +0,654 | |
| Окончание табл. 7.4 | |||
| Электрод | Реакция | φо, В | |
| Окислительно-восстановительные электроды | |||
| Cr3+, Cr2+ (Pt) | Cr3+ + e → Cr2+ | –0,408 | |
| Sn4+, Sn2+ (Pt) | Sn4+ + 2 e → Sn2+ | +0,150 | |
| Cu2+, Cu+ (Pt) | Cu2+ + e → Cu+ | +0,153 | |
| H+,C6H4O2, C6H4(OH)2 (Pt) | C6H4O2+2H++2e → C6H4(OH)2 | +0,699 | |
| Fe3+, Fe2+ (Pt) | Fe3+ + e → Fe2+ | +0,771 | |
| H+, O2 (Pt) | O2 + 4H+ +4e → 2 H2O | +1,229 | |
|
|
|
Таблица 7.5
Предельная эквивалентная электрическая проводимость ионов (при бесконечном разведении) при 25оС и температурный коэффициент электрической проводимости a;
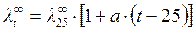
| Катионы |  ,
Ом-1см2× г-экв-1 ,
Ом-1см2× г-экв-1
| a | Анионы |  ,
Ом-1см2×г-экв-1 ,
Ом-1см2×г-экв-1
| a |
| Ag+ ½ Ba2+ ½ Cd2+ ½ Ca2+ ½ Cu2+ ½ Fe2+ H+ K+ Li+ ½ Mg2+ NH4+ Na+ ½ Pb2+ ½ Zn2+ | 61,9 63,6 59,5 53,5 349,8 73,5 38,6 53,0 73,5 50,1 70,0 54,0 | 0,0194 0,020 0,020 0,021 0,024 0,024 0,0142 0,0187 0,0214 0,0218 0,0187 0,0208 0,0178 0,0185 | Br – Cl– ½ CO32– F– J– NO3– OH– ½ SO42– HCOO– H3COO– МnO4– NO2– | 78,14 76,35 69,3 55,4 76,85 71,4 198,3 80,0 54,6 40,9 61,3 71,4 | 0,0185 0,0194 0,0192 0,021 0,0192 0,0184 0,0196 0,0206 0,0206 0,0224 0,0248 - |
Таблица 7.6
Средние ионные коэффициенты активности γ±
|
|
|
|
|
Дата добавления: 2017-01-14; Просмотров: 984; Нарушение авторских прав?; Мы поможем в написании вашей работы!