
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Специфические реакции аминокислот
|
|
|
|
Химические свойства аминокислот
Реакции по карбоксильной группе аминокислот, аминогруппа которых защищена ацилированием или солеобразованием, протекают аналогично превращениям карбоновых кислот. Аминокислоты легко образуют соли, сложные эфиры, амиды, гидразиды, галогенангидриды, смешанные ангидриды. Реакции по амино-группе аминокислот, карбоксильная группа которых защищена алкилированием, протекают аналогично аминам.

1. Кислотно- основные (аминокислоты амфотерны):

2. Образование комплексных солей (наиболее устойчивы комплексы с ионами Сu2+, Ni2+, Zn2+). С гидроксидом меди (II) образуется хелатный комплекс синего цвета (используется для выделения и очистки аминокислот):
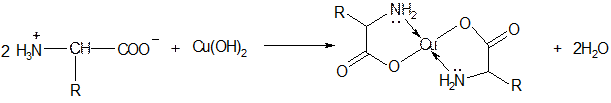
Образуемые хелатные соли синего цвета используются для выделения и очистки аминокислот.
3. Реакции по аминогруппе.
● дезаминирование азотистой кислотой (метод определения аминокислоты по объему выделившегося азота метод Ван - Слайка):
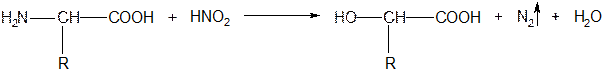
● реакция с формалином
(используется при формольном титровании – метод Серенсена)
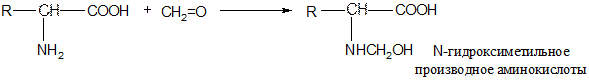
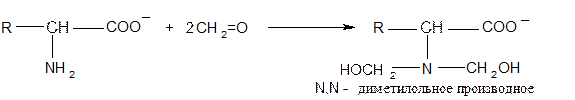
● реакция ацилирования (способ защиты аминогруппы):

● ацилирование аминокислотами аммиака
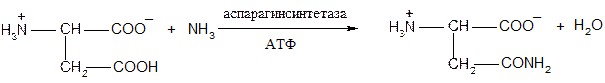
● алкилирование (2,4-динитрофторбензол – реактив Сэнджера)

●дезаминирование аминокислот
- неокислительное. Аминокислоты подвергаются дезаминированию; за счет этой реакции снижается избыток α-аминокислот в организме. Образующаяся фумаровая кислота – метаболит цикла трикарбоновых кислот.
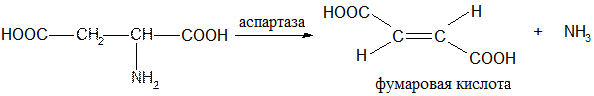
- окислительное (в присутствии оксидаз и НАД+)
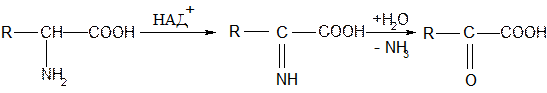
4. Реакции по карбоксильной группе
●декарбоксилирование. Амины, образующиеся в результате ферментативного декарбоксилирования аминокислота in vivo, называются биогенными аминами. Таким путем из серина получается коламин – предшественник холина и ацетилхолина в организме:

5. Трансаминирование (переаминирование) – основной путь биосинтез
α-аминокислот. Необходимая организму α-аминокислота (II) синтезируется из α-аминокислоты (I), имеющейся в клетках в достаточном количестве. Реакция осуществляется с помощью трансаминаз и кофермента пиридоксальфосфата. Процесс переаминирования является связующим звеном между метаболизмом белков (аминокислоты) и углеводов (кетонокислоты). С помощью этого процесса устраняется избыток отдельных α-аминокислот и таким образом регулируется содержание α-аминокислот в клетке.

6. Реакции с одновременным участием NH2- и СООН – групп
● дегидратация α-аминокислот

•β-аминокислоты термически не стабильны, при нагревании отщепляют аммиак и дают аммониевые соли непредельных кислот. Причиной такой реакции является подвижность водородных атомов в соседстве с карбоксильной группой.
NH2 – CH2 – CH2 – COOH 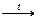 CH2=CH – COOH + NH3
CH2=CH – COOH + NH3
● дегидратация γ- и δ-аминокислот
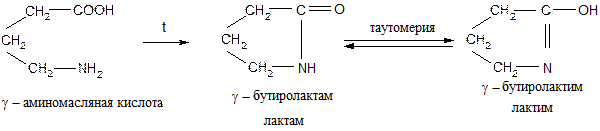
Этими реакциями пользуются для установления строения аминокислот. γ- и δ-Лактамы могут быть гидролизованы в соответствующие аминокислоты нагреванием с растворами сильных кислот или щелочей.
● нингидриновая реакция; в водных растворах при нагревании появляется сине-фиолетовая окраска.
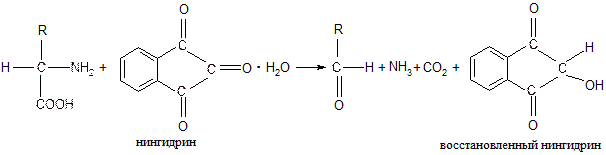
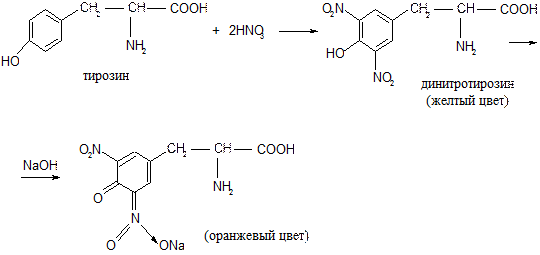
●ксантопротеиновая реакция (на ароматические α-аминокислоты). При нагревании с конц. HNO3 α-аминокислоты дают желтое окрашивание, при подщелачивании – оранжевое окрашивание:
Наибольший интерес представляют следующие L-a-аминокислоты, входящие в состав белковых молекул:
H2N – CH2 – COOH глицин (Gly)
CH3 – CH (NH2) – COOH аланин (Ala)
(CH3)2CH – CH (NH2) – COOH валин (Val)
CH3 – CH(CH3) – CH2 – CH(NH2) – COOH лейцин (Leu)
CH3 – CH2CH(CH3) – CH (NH2) – COOH изолейцин (Ile)
NH2(CH2)4 – CH (NH2) – COOH лизин (Lys)
NH2 –C – NH – (CH2)3 – CH (NH2) – COOH аргинин (Arg)
║
NH
NH2 – CO – CH2 – CH(NH2) – COOH аспарагин (Asn)
NH2 – CO – CH2 – CH2 – CH (NH2) – COOH глутамин (Gln)
HOOC – CH2 – CH (NH2) – COOH аспарагиновая к-та (Asp)
HOOC – CH2 – CH2 – CH (NH2) – COOH глутаминовая к-та (Glu)
HO – CH2 – CH (NH2) – COOH серин (Ser)
CH3 – CH(OH) – CH (NH2) – COOH треонин (Thr)
HS – CH2 – CH (NH2) – COOH цистеин (Cys)
CH3 – S–(CH 2)2 – CH (NH2) – COOH метионин (Met)
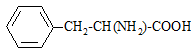 фенилаланин (Phe)
фенилаланин (Phe)
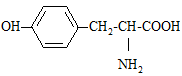 тирозин (Tyr)
тирозин (Tyr)
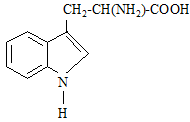 триптофан (Trp)
триптофан (Trp)
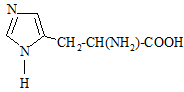 гистидин (His)
гистидин (His)
 пролин(Pro)
пролин(Pro)
Смеси L-аминокислот применяют в медицине для питания больных с заболеваниями пищеварительных и других органов; глутамат натрия и лизин – в пищевой промышленности, γ-аминомасляная кислота (амминалон) – медиатор в центральной нервной системе, как лекарственное средство при сосудистых заболеваниях головного мозга. На основе ГАМК созданы новые ноотропные средства, например:
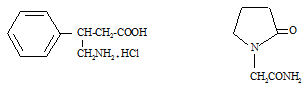
фенибут пирацетам
|
|
|
|
|
Дата добавления: 2017-02-01; Просмотров: 196; Нарушение авторских прав?; Мы поможем в написании вашей работы!