
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Молекулярность и порядок химических реакций
|
|
|
|
Для характеристики элементарных химических реакций используют понятие о молекулярности. Она может характеризоваться только целыми числами.
Молекулярность реакции определяется числом частиц (молекул), одновременно участвующих в элементарном акте химического взаимодействия. Если в элементарном акте взаимодействия участвует одна молекула, превращающаяся в одну или несколько молекул других веществ (реакции изомеризации, термического разложения, дегидратации в органической химии и т.д.), то такая реакция называется мономолекулярной.
Например:
А→продукты реакции (14.7)
Ca(HCO3)2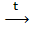 CaCO3 + CO2 + H2O.
CaCO3 + CO2 + H2O.
Бимолекулярными называются такие реакции, в которых в одновременном элементарном акте химического взаимодействия участвуют две
молекулы.
Например:
А + В → продукты реакции
или 2А → продукты реакции. (14.8)
Н2+I2→2HI;
CH3COOH + C2H5OH 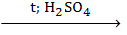 CH3COOC2H5 + H2O.
CH3COOC2H5 + H2O.
Тримолекулярными – называются такие реакции, элементарный акт которых сводится к одновременному столкновению и химическому взаимодействию трех молекул. Их немного.
Например:
A+B+C→продукты реакции,
2А+В → продукты реакции, (14.9)
или 3А → продукты реакции.
2NO+O2→2NO2;
2NO+H2→N2O+H2O.
Реакции с молекулярностью выше трех неизвестны, так как крайне мала вероятность столкновения и химического взаимодействия четырех молекул.
Окислительно-восстановительные химические реакции с большими
стехиометрическими коэффициентами, протекают по отдельным стадиям по типу моно-, би-, и тримолекулярных реакций.
Порядок реакции – это число, равное сумме показателей степеней концентраций реагирующих веществ в уравнении ЗДМ для скорости реакции:
аА+вВ→продукты реакции
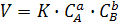 (14.10)
(14.10)
Общий порядок химической реакции а+b.
Порядок и молекулярность могут совпадать и различаться. В отличие от молекулярности порядок бывает дробным и даже отрицательным и нулевым.
N2+O2↔2NO.
Эта реакция имеет формально второй порядок.
Иногда порядок меняется в ходе химического процесса:
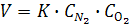 (порядок два);
(порядок два);
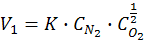 . (14.11)
. (14.11)
порядок согласно второму уравнению не 2, а 1,5. Возможен и нулевой порядок. Он означает, что скорость химической реакции при Т=const постоянна и не зависит от концентрации реагента.
Иногда порядок реакции ниже кажущейся молекулярности потому, что количество одного из реагентов, являющегося средой, в ходе химического превращения остается постоянным:
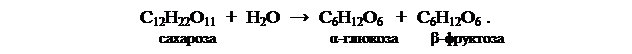
Это псевдомономолекулярная реакция первого порядка.
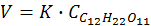 (14.12)
(14.12)
Эта бимолекулярная реакция является псевдомономолекулярной, т. к. концентрация воды в ходе реакции практически не меняется, и константа скорости инверсии может быть рассчитана по кинетическому уравнению реакции первого порядка.
Гидролиз тростникового сахара в нейтральном водном растворе практически не идет, он катализируется ионами водорода. Скорость гомогенного каталитического процесса пропорциональна концентрации катализатора (ионов водорода) в растворе.
Сахароза и продукты ее гидролиза принадлежат к числу оптически активных веществ, что связано с наличием в их молекулах асимметричных атомов углерода. Оптические изомеры отличаются по строению друг от друга, как несимметричный предмет от своего зеркального изображения. По физическим и химическим свойствам такие молекулы одинаковы и отличаются только различным по направлению вращением плоскости поляризации света.
Электромагнитные колебания естественного света происходят во всех плоскостях, проходящих через световой луч, колебания поляризованного света происходят лишь в одной из таких плоскостей.
Плоскость, перпендикулярная к плоскости колебаний поляризованного луча (также проходящая через луч), называется плоскостью поляризации. При пропускании поляризованного света через раствор оптически деятельного вещества плоскость поляризации поворачивается. Угол смещения плоскости колебаний поляризованного луча называется углом вращения плоскости поляризации.
Для растворов установлен следующий количественный закон: угол вращения плоскости поляризации а прямо пропорционален толщине слоя раствора d и концентрации активного вещества С:
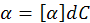 (14.13)
(14.13)
где d – это толщина слоя раствора, через который проходит поляризованный луч, дм;
С – концентрация, г/см3;
[α] – удельное вращение, равное углу вращения при прохождении луча через 1 дм слоя раствора, содержащего 1 г вещества в 1 мл раствора, при 20°С при определенной длине волны 5896 Ǻ (желтая Д-линия натрия), т. е. если d= 1 дм и С= 1 г/см3, то α=[α].
Удельное вращение плоскости поляризации в водных растворах сахарозы постоянно [α]=+66,55°, поэтому, зная угол вращения и толщину слоя раствора, легко найти концентрацию сахарозы.
Тростниковый сахар вращает плоскость поляризации вправо [α]=+66,55°, а смесь продуктов гидролиза – влево, так как фруктоза вращает ее влево [α] = 91,9° и больше, чем глюкоза, которая вращает вправо [α]=+52,5°. Поэтому по мере протекания гидролиза угол вращения плоскости поляризации уменьшается, падает до нуля, а затем становится отрицательным, т.е. правое вращение сменяется левым. Поэтому гидролиз тростникового сахара называют инверсией. Окончанию инверсии отвечает отрицательное предельное значение угла вращения.
|
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 7409; Нарушение авторских прав?; Мы поможем в написании вашей работы!