
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Лабораторная работа
|
|
|
|
Узловые вопросы, необходимые для усвоения темы занятия
Типовой билет входного контроля
1. Альдегиды вступают в реакции
1) Нуклеофильного присоединения;
2) Нуклеофильного замещения;
3) Электрофильного присоединения;
4) Электрофильного замещения.
2. Реакция, в которой не может быть получен названный продукт
1) СН3СН2СН=О + С6Н5NH2 → Основание Шиффа;
Н+
2) CH3CH=O + 2CH3CH2OH → Ацеталь;
3) CH3CH=O + С6Н5CONH2 → Финилгидразон;
Н+
3) CH3CH=O + CH3OH → Полуацеталь.
3. Соединения, способные вступать в реакцию альдольной конденсации
1) (СН3)3СН=О;
2) (СН3)2СНСН=О;
3) С6Н5СН=О;
4) СН3СН2СН2СН=О.
4. Пара соединений, которые можно различить с помощью йодоформной пробы
1) СН3СН=О и СН3СН2СН2ОН;
2) СН3СН=О и СН3СОСН3;
3) СН3СОСН3 и СН3СОСН2СН3;
4) СН3СН2ОН и СН3СН(ОН)СООН.
5. Вещество, вступающее в реакцию диспропорционирования (реакция Канниццаро)
1) уксусный альдегид;
2) бензальдегид;
3) пропионовый альдегид;
4) масяный альдегид.
1. Электронное строение карбонильной группы.
2. Реакционные центры в молекулах альдегидов и кетонов.
3. Химические свойства альдегидов и кетонов: реакции нуклеофильного присоединения; реакции конденсации (альдольное присоединение, кротоновая конденсация); окисление и восстановление альдегидов и кетонов; реакции диспропорционирования (Канниццаро).
Опыт 1. Восстановление альдегидом соединений двухвалентной меди
К 1 мл раствора исследуемого альдегида добавьте 0,5 мл разбавленного раствора щелочи и затем по каплям растворов сульфата меди до образования осадка. Полученную смесь нагрейте до начала кипения, при этом осадок изменяет свою окраску. Напишите схему реакции.
Опыт 2. Качественная реакция на ацетон с нитропруссидом натрия
Цветная реакция ацетона с нитропруссидом натрия Na2[Fe(CN)5NO], называется пробой Легаля, часто применяется в дополнение к йодоформной пробе. Эта реакция широко используется в клиническом анализе, например, для определения ацетона в моче у больных сахарным диабетом.
В пробирку налейте 3-4 мл 1% раствора ацетона, 0,5 мл разбавленного раствора нитропруссида натрия и несколько капель 10% едкого натра. Появляется оранжево-красное окрашивание, которое при подкислении уксусной кислотой переходит в вишнево-красное.
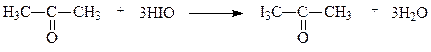
Опыт 3. Йодоформная проба на ацетон (проба Либена)
К 1 мл ацетона добавьте 1 мл раствора йода и несколько капель щелочи до исчезновения окраски. Образуется желтый осадок йодоформа с характерным запахом.

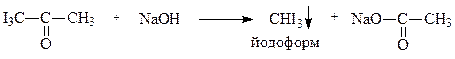
|
|
|
|
|
Дата добавления: 2014-10-31; Просмотров: 2453; Нарушение авторских прав?; Мы поможем в написании вашей работы!