
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Контроль усвоения темы занятия. Опыт 1. Свойства пиридина
|
|
|
|
Лабораторная работа
Опыт 1. Свойства пиридина
Пиридиновое ядро является основой многих алкалоидов (никотина, анабазина и др.), витаминов (никотиновой кислоты, витаминов группы В6), а также лекарственных средств.
В пробирку поместите 2 капли пиридина и около 2 мл воды. Отметьте растворимость пиридина в воде и его специфический запах. Раствор используйте для проведения опытов А-Б.

А. С помощью стеклянной палочки поместите по 1 капле полученного раствора пиридина на полоску красной лакмусовой и универсальной индикаторной бумаги. Отметьте изменение окраски индикаторов.
Б. В пробирку поместите 5 капель раствора пиридина и добавьте 5 капель 1% раствора хлорида железа (III). Отметьте цвет выпавшего осадка.
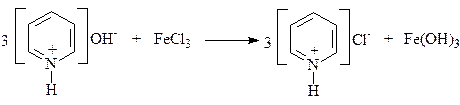
Образец билета выходного контроля
1. Напишите уравнения реакции взаимодействия пиридина с:
а) HCl;
б) метилйодидом;
в) нитрующей смесью.
2. Приведите таутомерные формы производных пиримидина: урацила и цитозина.
Вопросы и упражнения для аудиторной работы
1. Напишите схемы реакций взаимодействия пиридина с:
а) с соляной и серной кислотами на холоду;
б) йодистым этилом;
в) амидом натрия;
г) нитрующей смесью;
д) избытком водорода.
2. Объясните причины уменьшения основных свойств в ряду имидазол, пиридин, пиримидин. Напишите схемы реакций, доказывающих основные свойства этих соединений.
3. Кордиамин (стимулятор центральной нервной системы) представляет собой 25% водный раствор N,N-диэтиламида никотиновоый кислоты. Напишите схему синтеза кордиамина согласно следующей схеме:
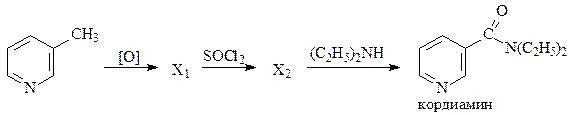
4. Никотиновая кислота - витамин, участвующий во многих окислительных реакциях живых клеток. Она может быть синтезирована окислением хинолина до пиридин-2,3-дикарбоновой кислоты с последующим ее декарбокслированием. Напишите схему синтеза никотиновой кислоты.
5. Какой тип таутомерии характерен для тимина и урацила? Напишите схему таутомерных превращений тимина и урацила. Укажите, какая таутомерная форма преобладает в смеси таутомеров.
6. Напишите схемы реакций взаимодействия хинолина с:
а) с соляной и серной кислотами на холоду;
б) йодистым этилом;
в) амидом натрия;
г) нитрующей смесью.
Назовите продукты реакции.
7. Химическая основа действия кофермента НАД+. Приведите реакцию алкилпиридиниевого иона с гидрид-ионом.
8. Осуществите превращения:
1)
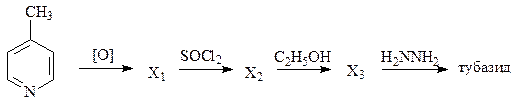
2)
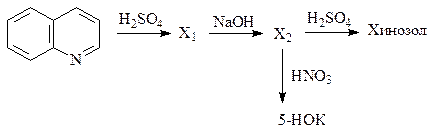
7.5 Подведение итогов занятия
7.6 Задание на дом: α-аминокислоты. Пептиды. Белки.
Место проведения самоподготовки: читальный зал и др.
Литература: [1], [2], [4].
Занятие №10
α-Аминокислоты. Пептиды. Белки
1. Актуальность темы. Белки как основа всего живого были издавна в центре внимания естественных наук. Белки составляют материальную основу химической деятельности клетки. Функции белков в природе универсальны. Пептиды имеют меньшую молекулярную массу, чем белки. В биологическом плане пептиды отличаются от белков более узким спектром функций. Многообразные пептиды и белки состоят из остатков α-аминокислот. Общее число встречающихся аминокислот в природе достигает 100, однако некоторые из них обнаружены лишь в определенном обществе организмов или даже в одном из видов. Известно 20 наиболее важных α-аминокислот, постоянно встречающихся во всех белках.
2. Учебные цели. Сформировать знания о строении и свойствах важнейших α-аминокислот, о структурной организации пептидов и белков.
3. Материалы для самоподготовки к усвоению данной темы.
Вопросы для самоподготовки
1. α-Аминокислоты, входящие в состав белков. Строение. Номенклатура.
2. Классификация α-аминокислот по химической природе радикала и содержащихся в нем заместителей; по кислотно-основным свойствам.
3. Химические свойства α-аминокислот по карбоксильной и аминогруппам. Специфические свойства α-аминокислот: отношение к нагреванию, комплексообразование. Качественные реакции.
4. Реакции трансаминирования и восстановительного аминирования. Реакции дезаминирования, декарбоксилирования, окисления тиольных групп.
5. Первичная структура пептидов и белков. Методы определения N- и С-концевых аминокислот. Образование ФТГ-производных (реакция Эдмана).
6. Частичный и полный гидролиз белков.
4. Вид занятия: практическое занятие.
5. Продолжительность занятия: 2 академических часа.
6. Оснащение рабочего места:
6.1Посуда и приборы:
| Штатив с пробирками, пипетки. | на группу |
6.2. Объекты исследования:
| 1% Раствор глицина, раствор яичного белка, раствор желатина. | на группу |
6.3. Реактивы:
| Метиловый красный, формалин, 5% раствор NaNO2, CН3СООН(конц.), 10% раствор NaOH, 2% раствор CuSO4. | на группу |
7. Содержание занятия
|
|
|
|
|
Дата добавления: 2014-10-31; Просмотров: 1880; Нарушение авторских прав?; Мы поможем в написании вашей работы!