
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Лабораторная работа. Узловые вопросы, необходимые для усвоения темы занятия
|
|
|
|
Узловые вопросы, необходимые для усвоения темы занятия
Типовой билет входного контроля
1. Выберите незаменимые в организме α-аминокислоты
1) валин;
2) аспарагин;
3) фенилаланин;
4) серин.
2. Установите соответствие
Название Формула
1) цистеин А) H2NCH(CH3)COOH
2) глицин Б) H2NCH(CH2SH)COOH
3) аланин В) H2NCH(CH2CH2SCH3)COOH
4) метионин Г) H2NCH2COOH
3. Дезаминирование α-аминокислот in vitro осуществляется
1) с участием ферментов дегидрогеназ и кофермента НАД+;
2) баритовой водой;
3) азотистой кислотой;
4) формальдегидом.
4. Установите соответствие
Аминокислота Оксокислота, образующаяся в результате
реакции трансаминирования
1) аланин А) СН3СН2СОСООН
2) аспарагиновая кислота Б) СН3СОСООН
В) НООССН2СОСООН
Г) СН3СОСН2СООН
5. Пептиды содержат в молекуле
1) до 100 аминокислотных остатков;
2) до 1000 аминокислотных остатков;
3) до 10000 аминокислотных остатков;
4) до 1000000 аминокислотных остатков
1. α-Аминокислоты, входящие в состав белков. Строение. Номенклатура.
2. Классификация α-аминокислот по химической природе радикала и содержащихся в нем заместителей; по кислотно-основным свойствам.
3. Химические свойства α-аминокислот по карбоксильной и аминогруппам. Специфические свойства α-аминокислот: отношение к нагреванию, комплексообразование. Качественные реакции.
4. Реакции трансаминирования и восстановительного аминирования. Реакции дезаминирования, декарбоксилирования, окисления тиольных групп.
5. Первичная структура пептидов и белков. Методы определения N- и С-концевых аминокислот. Образование ФТГ-производных (реакция Эдмана).
6. Частичный и полный гидролиз белков.
Опыт 1. Реакция глицина с формальдегидом
Реакция α-аминокислот с формальдегидом является основой метода формального титрования (метод Сёренсена). Этот метод используется в фармацевтическом анализе для количественного определения лекарственных средств аминокислотной природы.
В пробирку поместите 5 капель 1% раствора глицина и добавьте 1 каплю индикатора метилового красного. Раствор окрашивается в желтый цвет (нейтральная среда). К полученной смеси добавьте равный объем формалина. Отметьте появление красной окраски (кислая среда). Данная реакция под названием «формальное титрование» используется для количественного определения карбоксильных групп в α-аминокислотах.
Опыт 2. Реакция глицина с азотистой кислотой
Реакция с азотистой кислотой лежит в основе метода количественного определения α-аминкоислот по объему выделившегося азота (метод Ван-Слайка). В настоящее время реакция сохранила лишь историческое значение.
В пробирку поместите 5 капель 1% раствора глицина и равный объем 5% раствора нитрита натрия. Добавьте 2 капли концентрированной уксусной кислоты и осторожно взболтайте смесь. Наблюдайте выделение газа. Реакция используется для количественного определения аминогрупп в аминокслотах.
Опыт 3. Биуретовая реакция
Биуретовая реакция позволяет обнаружить структурный фрагмент, содержащий не менее двух амидных групп. Реакция основана на способности пептидной группы белков и полипептидов образовывать с ионами меди в щелочной среде комплексные соединения фиолетового цвета.
Реакция позволяет обнаружить наличие пептидной группы –СONH- в исследуемом веществе и, следовательно, является универсальной реакцией для обнаружения веществ белковой природы. Свое название реакция получила от производного мочевины биурета, который дает в данных условиях то же окрашивание, что и белок. Окрашивание появляется за счет образования медной комплексной соли следующего строения:
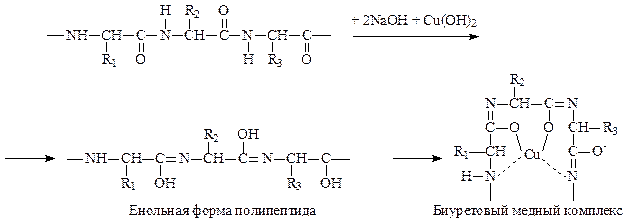
В одну пробирку поместите 5 капель раствора яичного белка, в другую – раствор желатина. В обе пробирки добавьте по 10 капель раствора едкого натра и по 1 капле раствора сульфата меди. В той и другой пробирке появляется красно-фиолетовое или сине-фиолетовое окрашивание.
|
|
|
|
|
Дата добавления: 2014-10-31; Просмотров: 1213; Нарушение авторских прав?; Мы поможем в написании вашей работы!