
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Электростатическое взаимодействие полярной и неполярной молекул или неполярной молекулы с внешним электростатическим полем
|
|
|
|
Индукционная составляющая
Силы Ван-дер-Ваальса
ЛЕКЦИЯ 6. ВЗАИМОДЕЙСТВИЯ МЕЖДУ МОЛЕКУЛАМИ
Конденсированное (жидкое, твердое) состояние вещества обусловлено межмолекулярными взаимодействиями
Основные виды:
●вандерваальсовы силы
●водородные межмолекулярные связи
●донорно-акцепторные взаимодействия
– силы межмолекулярного взаимодействия, проявляющиеся на расстояниях, превосходящих размеры частиц.
Три составляющие вандерваальсовых сил:
Ориентационная составляющая (диполь-дипольное взаимодействие)
- взаимодействие полярных молекул при их сближении
Е ориен уср ≈  4 /(Т • r 6)
4 /(Т • r 6)
Е ориен увеличивается:
· с увеличением 
· с уменьшением расстояния (r) между молекулами
· с понижением температуры (Т)
Диполи, действуя на неполярные молекулы, превращают их индуцированные (наведенные) диполи.
Е индуср ≈ α •  2/ r 6
2/ r 6
α - поляризуемость молекулы (атома)
● характеризует способность молекулы (атома)
деформироваться и поляризоваться (приобретать дипольный момент в электрическом поле)
● α ↑ с ↑ размеров, усложнением структуры и ↑ массы
молекулы
Е инд увеличивается:
· с ↑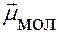
· с ↓ расстояния между молекулами
· с ↑ поляризуемости неполярной молекулы (атома)
Е инд < Е ориен
Дисперсионная составляющая (эффект Лондона)
-взаимодействие мгновенных диполей, возникающих за счет смещения е- и атомных ядер под действием электрического поля
Е диспуср ≈ α2/ r 6
Е дисп увеличивается:
· с увеличением поляризуемости молекул (атомов)
|
|
|
|
|
Дата добавления: 2014-10-31; Просмотров: 359; Нарушение авторских прав?; Мы поможем в написании вашей работы!