
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Например, ЭДС концентрационной цепи
|
|
|
|
Электрохимическая цепь будет равновесной, если электрохимическое равновесие осуществлено на каждой фазовой границе. При этом условии электродвижущая сила складывается из суммы скачков потенциала на всех фазовых границах.
Отметим, что стандартный потенциал стеклянного электрода со временем изменяется, поэтому стеклянный электрод перед каждым измерением рН калибруется по стандартным буферным растворам с точно известным значением рН.
Классификация электрохимических цепей. Электрохимической цепью называется система, состоящая из двух или нескольких электродов. Это устройство для преобразования энергии химической окислительно-восстановительной реакции в электрическую за счет пространственного разделения процессов окисления и восстановления.
При схематической записи электрохимических цепей (гальванических элементов), а также уравнений протекающих в них реакций принято соблюдать следующие основные правила:
– при записи электрохимической цепи, составленной из двух электродов, слева записывают отрицательный электрод (анод), например

С тандартный водородный электрод всегда записывают слева.
– при включении между растворами солевого мостика (насыщенный раствор КСl, обозначается ║), используемого для устранения диффузионного потенциала (возникает на границе растворов электролитов вследствие различной подвижности ионов) схема элемента записывается следующим образом

Полное уравнение окислительно-восстановительной реакции, протекающей в гальваническом элементе, записывается как разность электродных реакций, протекающих на катоде (Cu2+ + 2е = Cu, восстановление) и аноде (2H++ 2е = H2, окисление)
H2 + Cu2+ = 2H++ Cu
Предельное значение напряжения гальванического элемента при токе через элемент, стремящемся к нулю, называется электродвижущей силой (ЭДС). ЭДС любого гальванического элемента без учета диффузионного потенциала определяется как разность потенциалов положительного и отрицательного электродов
E = Е катод – Е анод. (16)
По характеру суммарного процесса, лежащего в основе действия гальванического элемента электрохимические цепи делятся на химические, концентрационные и физические.
– Концентрационные электрохимические цепи состоят из электродов с одинаковыми потенциалопределяющими реакциями, но активности одного (или нескольких) участников реакции на каждом из электродов различны. Стандартные электродные потенциалы электродов одинаковы, поэтому они не входят в уравнение Нернста для ЭДС цепи
 .
.
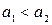
|
|
|
|
|
Дата добавления: 2014-11-16; Просмотров: 856; Нарушение авторских прав?; Мы поможем в написании вашей работы!