
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Реакции окисления. Ацетилен и его гомологи с концевой тройной связью R-C=C-H (алкины-1) вследствие полярности связи С(sp)-Н проявляют слабые кислотные свойства и способны
|
|
|
|
_
Кислотные свойства
Ацетилен и его гомологи с концевой тройной связью R-C=C-H (алкины-1) вследствие полярности связи С(sp)- Н проявляют слабые кислотные свойства и способны отщеплять протон под действием достаточно сильных оснований. Подвижный атом водорода может замещаться на металл с образованием солей - ацетиленидов. Например:

|
Ацетилениды щелочных и щелочноземельных металлов используются для получения гомологов ацетилена.
При взаимодействии ацетилена или алкинов-1 с аммиачными растворами оксида серебра или хлорида меди (I) выпадают осадки нерастворимых ацетиленидов:

|
Образование белого осадка ацетиленида серебра (или красно-коричневого ацетиленида меди) служит качественной реакцией на концевую тройную связь. Если тройная связь находится не на конце цепи, то кислотные свойства отсутствуют (нет подвижного атома водорода) и ацетилениды не образуются.
В сухом состоянии ацетилениды тяжелых металлов чувствительны к удару и легко взрываются. Их разлагают, пока они еще влажные, действием сильных минеральных кислот.

|
Реакции образования ацетиленидов с последующим их разложением могут использоваться для выделения алкинов из смесей с другими углеводородами.
Ацетилен и его гомологи окисляются перманганатом калия с расщеплением тройной связи и образованием карбоновых кислот:

|
Алкины обесцвечивают раствор KMnO4, что используется для их качественного определения.
При сгорании (полном окислении) ацетилена выделяется большое количества тепла:
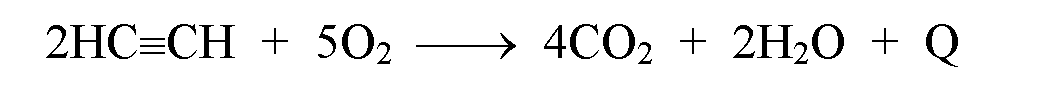
|
Температура ацетиленово-кислородного пламени достигает 2800-3000°С. На этом основано применение ацетилена для сварки и резки металла. Ацетилен образует с воздухом и кислородом взрывоопасные смеси. В сжатом, и особенно в сжиженном, состоянии он способен взрываться от удара. Поэтому ацетилен хранится в стальных баллонах в виде растворов в ацетоне, которым пропитывают асбест или кизельгур.
|
|
|
|
|
Дата добавления: 2014-11-18; Просмотров: 1410; Нарушение авторских прав?; Мы поможем в написании вашей работы!