
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Первичный амебный менингоэнцефалит 1 страница
|
|
|
|
Первичный амебный менингоэнцефалит — это заболевание, вызываемое свободноживущими амебами рода Naegleria или Acanthamoeba. Первые чаще всего поражают детей и взрослых людей молодого возраста, заражение ими происходит, по-видимому, во время купания в пресной теплой воде, заболевание почти неизменно заканчивается летальным исходом. Заражение акантамебами встречается у лиц зрелого возраста, и в некоторых случаях отмечается спонтанное выздоровление.
В природных условиях свободноживущие амебы распространены повсеместно, обычные места их обитания — почва и вода. Хотя в целом они считаются безвредными, некоторые их разновидности обладают четко выраженной патогенностью для млекопитающих с поражением преимущественно центральной нервной системы. В тех случаях, когда от людей, заболевших менингоэнцефалитами, удавалось выделить и культивировать возбудителя, им, за редким исключением была, амеба Naegleria fowleri.
В различных странах мира, включая Австралию, Бельгию, Бразилию, ЧСФР, Великобританию, Ирландию, Новую Зеландию, Замбию и США, описано в общей сложности более 100 случаев заболеваний, вызванных представителями рода Naegleria. Серологические исследования свидетельствуют о том, что значительно чаще встречаются инаппарантные случаи инфекции. Большая часть из 50 выявленных в США случаев отмечена в юго-восточных штатах, в частности во Флориде, Джорджии и Вирджинии. Характерно, что заболевание начинается в летние месяцы, примерно через 1 нед после купания в водоемах с пресной или солоноватой водой. В ЧСФР 16 случаев заболевания возникли после плавания в закрытом бассейне с хлорированной водой при температуре 24°С и в 6 случаях заражение произошло, очевидно, после купания в водах горячего минерального источника. В странах Африки южнее Сахары заражение больных происходило, по-видимому, при вдыхании содержащего цисты воздуха в период сухого ветреного сезона харматтан. Гистологические данные свидетельствуют о том, что входными воротами инфекции служит непосредственно слизистая оболочка носа в области решетчатой кости. Клинически заболевание начинается остро, протекает быстро и заканчивается летально. Первым симптомом болезни является резкая, упорная головная боль в области лба с последующей тошнотой, рвотой, лихорадкой и ригидностью затылочных мышц. Возможно изменение вкуса или обоняния. Далее появляются сонливость, спутанность сознания, судороги и кома. По ходу болезни могут возникнуть признаки очагового поражения нервной системы.
Акантамебы вызывают более доброкачественную, хроническую форму менингоэнцефалита. По-видимому, они попадают в мозг и другие органы с кожных покровов или дыхательных путей. Клинически болезнь чаще проявляется у людей более старшего возраста, имеющих иммунные нарушения; в анамнезе у них могут отсутствовать указания о купании в пресноводных водоемах; в подобных случаях возможно спонтанное выздоровление. Патоморфологически данное заболевание отличается от такового, вызванного представителями рода Naegleria, развитием гранулематозных воспалительных реакций и наличием в тканях как трофозоитов, так и цист. К сожалению, идентификация возбудителя болезни не всегда бывает бесспорной, поскольку его редко удается выделить путем культивирования. Возможно, что данное заболевание вызывают несколько видов свободноживущих амеб. Описано около десятка случаев кератита, вызванного акантамебами.
Единственным точным методом диагностики является тщательное исследование спинномозговой жидкости (СМЖ). При инфекции, вызванной Naegleria, СМЖ кровянистая или гнойно-кровянистая и содержит множество нейтрофилов. Содержание белка повышено, глюкозы—понижено. В обычных посевах грамотрицательные возбудители не обнаруживаются. При микроскопическом исследовании свежих нативных нецентрифугированных препаратов спинномозговой жидкости обычно обнаруживаются живые трофозоиты диаметром 10—20 мкм, с зернистой цитоплазмой, четкой эктоплазмой и выступающими псевдоподиями. При охлаждении препарата трофозоиты могут потерять подвижность и распознать их становится значительно труднее. Диагноз подтверждается с помощью прямой реакции флюоресцирующих антител (ПРФА). Хотя Naegleria можно легко выращивать на обычных культуральных средах с добавлением кишечной палочки, этот метод непригоден для клинических целей, поскольку заболевание весьма быстро прогрессирует. При заболеваниях, вызванных акантамебами, в спинномозговой жидкости обычно находят множество моноцитов. Культивирование или микроскопия нативных препаратов не позволяют обнаружить трофозоиты. В немногих случаях наблюдалась положительная прямая реакция флюоресцирующих антител. Лечение с помощью стандартных антипротозойных препаратов является, по-видимому, совершенно неэффективным. Однако Naegleria высокочувствительны к действию амфотерицина В, миконазола, тетрациклина и рифампицина. В настоящее время известны только четыре случая излечения больных с заболеванием, вызванным Naegleria. Во всех этих случаях диагноз был установлен своевременно, в процессе лечения трое больных получали амфотерицин В, а один — амфотерицин В, миконазол и рифампицин. Вероятно, чтобы быстро получить эффективный уровень препарата в спинномозговой жидкости, весьма существенно вводить амфотерицин В внутривенно и субокципитально. Дозировка препарата при внутрижелудочковом введении составляет 0,5—1,0 мг в течение первых нескольких дней. В случае внутривенного введения дозировка препарата такая же, как при криптококкозном менингите (см. гл. 146). Акантамебы чувствительны к сульфаниламидам, клотримазолу, 5-FC и полимиксину В, однако клинических исследований такого рода не проводилось.
При обнаружении источника инфекции следует запретить купание в зараженном водоеме, что поможет предотвратить дальнейшее распространение болезни.
ГЛАВА 154. МАЛЯРИЯ
Джеймс Дж. Плорд, Николае Дж. Уайт (James J. Plorde, Nicholas J. White)
Определение. Малярия — это протозойная болезнь, передаваемая человеку при укусах комаров рода Anopheles, сопровождающаяся лихорадкой, ознобами, спленомегалией, анемией и характеризующаяся хроническим рецидивирующим течением. Несмотря на впечатляющие результаты начатой в 1956 г. по инициативе Всемирной организации здравоохранения программы по ликвидации малярии, технические и социально-экономические трудности вновь привели к появлению болезни во многих странах мира. Вследствие этого в настоящее время малярия, как и на протяжении многих веков, представляет собой одну из самых серьезных проблем для инфекционистов.' В США и Европе ежегодно отмечается несколько тысяч завозных случаев малярии среди лиц, прибывающих из эндемичных районов.
Этиология. Возбудителями малярии являются простейшие рода Plasmodium. Для человека патогенны Р. vivax, P. ovale, P. malariae и Р. falciparum. Человек заболевает в момент инокуляции самкой малярийного комара спорозоитов возбудителя в лимфогематогенную систему при кровососании. После кратковременного пребывания в периферической крови спорозоиты проникают в гепатоциты, давая тем самым начало доклинической печеночной (экзоэритроцитарной) стадии болезни. В процессе бесполого размножения, называемого шизогонией, из одного спорозоита в конечном счете образуется от 2000 до 40 000 печеночных мерозоитов. В большинстве случаев эти дочерние клетки через 1—6 нед снова попадают в систему кровообращения. При инфекциях, вызываемых некоторыми северными штаммами Р. vivax, выход в кровь мерозоитов из печени происходит примерно через 10 мес от момента заражения, в сроки, совпадающие с кратковременным периодом выплода комаров в следующем году. При инфекциях, вызываемых Р, falciparum и Р. malariae, печеночная стадия на этом заканчивается. Если инфекция вызвана остальными видами возбудителей, печеночные стадии (гипнозоиты) персистируют и вызывают, спустя месяцы и годы новые эпизоды выхода паразитов в кровь.
Эритроцитарная, или клиническая, стадия малярии начинается с прикрепления попавших в кровь мерозоитов к специфическим рецепторам на поверхности эритроцитов. Эти рецепторы, по-видимому, неодинаковы для разных видов малярийных паразитов; так, для Р. vivax они связаны с антигенами группы крови Даффи (Fy8 или FyY В этой связи существует предположение, что лица, не имеющие антигена Даффи (FyFy) (к ним относятся большинство населения Западной Африки и их потомки), устойчивы к заражению трехдневной малярией. Считают, что рецептором для Р. falciparum является гликофорин, сиалогликопротеин мембраны эритроцита. После прикрепления мерозоит инвагинирует мембрану эритроцита и постепенно оказывается внутри клетки. Там возбудитель переходит на стадию кольцевидного трофозоита, который, затем, увеличиваясь в размерах, приобретает неправильную или амебовидную форму. Далее начинается деление ядра на несколько фрагментов и трофозоит превращается в многоядерный шизонт. Наконец, цитоплазма концентрируется вокруг каждого дочернего ядра, при этом формируется новое поколение мерозоитов. Через 48 ч (72 ч в случае Р. malariae) после начала инвазии эритроцит разрывается, высвобождая от 6 до 24 мерозоитов, каждый из которых способен положить начало новому эритроцитарному циклу. При повторении такого цикла в некоторых эритроцитах образуются имеющие характерные морфологические признаки половые формы возбудителей малярии (гамонты); они не вызывают разрыва эритроцита и не способны к дальнейшему развитию, если не попадут при кровососании в организм комаров соответствующего вида. В кишечнике комара происходит оплодотворение, образуется зигота, которая инцистируется в наружной стенке кишки и высвобождает десятки тысяч спорозоитов. Последние проникают в слюнные железы комара и инокулируются человеку при очередном кровососании.
Эпидемиология. Малярия сохраняется только в тех районах мира, где плотность популяций как малярийных комаров, так и инвазированных людей поддерживается выше определенного критического уровня, необходимого для стойкой передачи болезни. Мероприятия по борьбе проводятся с.целью уменьшения плотности обеих популяций до уровней, достаточно низких для того, чтобы прервать цепь передачи возбудителя болезни. В число важных мер борьбы входят дренирование или ликвидация мест выплода переносчика, обработка инсектицидами остаточного действия, использование пологов и кожных репеллентов, эффективное лечение больных, а также проведение крупномасштабных программ подавляющей химиотерапии среди некоторых групп населения.
В результате активного сотрудничества по осуществлению международной программы по ликвидации малярии в 1956—1968 гг. было достигнуто значительное снижение заболеваемости. На более чем 75% пораженной территории болезнь была ликвидирована либо было начато активное осуществление программ по ее ликвидации. Однако в настоящее время малярия все еще поражает 250—300 млн жителей 104 стран Африки, Латинской и Южной Америки, Азии и Океании. Ежегодно на долю только одной тропической Африки приходятся 200 млн случаев заболевания малярией и большая часть из 1 млн случаев смерти от этой болезни. Наличие мигрирующих групп населения, значительная распространенность переносчиков и высокий уровень передачи болезни — все это ставит под сомнение возможность успешной ликвидации малярии в этих районах. Более того, развитие устойчивости к инсектицидам, равно как и различные административные и социально-экономические проблемы, привело к утрате результатов, достигнутых при осуществлении ранее успешных программ ликвидации малярии в ряде стран. К указанным выше трудностям добавилось продолжающееся распространение лекарственной устойчивости у штаммов малярии в ряде районов Южной Азии, Западной части Тихого океана, Центральной и Южной Америки. Устойчивые штаммы обнаружены в восточных и центральных районах Африки и на Индийском субконтиненте, где раньше этой проблемы не существовало.
В США эндемическая малярия встречалась до 50-х годов текущего столетия. В последующие годы в США продолжали регистрироваться завозные случаи болезни и в результате передачи возбудителя комарами-переносчиками спорадические вспышки малярии (интродуцированная малярия). Однако до 1966 г. их общее число не превышало 200 случаев в год. Однако это число стало быстро возрастать по мере возвращения инфицированных военнослужащих из Юго-Восточной Азии, достигнув пика свыше 4000 случаев в 1970 г. С этой волной завозной малярии был связан небольшой подъем числа случаев малярии, связанных с переливанием крови и внутривенным введением наркотиков. Хотя указанная эпидемия угасла, заболеваемость малярией среди гражданского населения не снизилась (рис. 154-1). С 1970 по 1979 г. число ежегодно регистрируемых случаев малярии среди туристов, деловых людей, учителей, студентов и других гражданских лиц возросло со 151 до 825; в 1984 и 1985 г. в СЩА ежегодно отмечалась примерно 1000 диагностированных случаев малярии. За редким исключением, заражение малярией происходило за рубежами США: примерно 40% в Азии, 30% в Африке и 20% в странах Карибского региона и Латинской Америки. Из числа недавно зарегистрированных случаев малярии на долю граждан США приходится 40%; больше половины из них заразились в Африке. Большая часть случаев малярии среди иностранных граждан была отмечена у иммигрантов из Юго-Восточной Азии. Данные эпидемиологического надзора свидетельствуют о том, что 2—5% лиц этой группы бывают инфицированы к моменту въезда в США. Клинические проявления малярии развиваются обычно в течение 6 мес с момента прибытия в США, однако в 30% случаев трехдневной малярии. они появляются в более поздние сроки. В 1983 г. тропическая малярия составляла 25% всех случаев болезни и все три летальных исхода были вызваны вирулентным штаммом ее возбудителя. Подавляющее большинство этих случаев можно было бы предупредить посредством соответствующей химиопрофилактики. До тех пор, пока туристы не будут получать -достаточно полную информацию об опасностях, связанных с поездками без должной защиты в эндемичные по малярии районы, количество завозных случаев болезни в США будет продолжать увеличиваться.
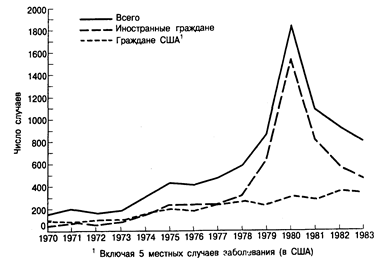
Рис. 154-1. Случаи малярии у граждан США и иностранных граждан, проживающих в США (включая Пуэрто-Рико, Виргинские острова и остров Гуам), 1970—1983 гг. (по данным Эпидемиологического надзора: Ежегодные данные, 1984, Атланта, ДжА, Центр по борьбе с болезнями, 1985 г.).
Патогенез и патологические изменения. Инвазирование, повреждение и разрушение эритроцитов малярийными паразитами, местные и системные нарушения кровообращения и связанные с ними метаболические изменения — все это играет важную роль в патофизиологии малярии.
Изменения эритроцитов. Различные виды малярийных плазмодиев существенно различаются по способности инфицировать эритроциты. Возбудители трехдневной малярии и малярии овале поражают только незрелые эритроциты, возбудители четырехдневной малярии — только стареющие. Поэтому при заболеваниях, вызванных указанными возбудителями, поражается не более 1—2% эритроцитов. Возбудитель тропической малярии, хотя и предпочитает молодые эритроциты, поражает красные кровяные клетки любых возрастов и может вызывать исключительно высокие уровни паразитемии, что и является фактором, обусловливающим высокую летальность при этом заболевании. Однако наличие определенных аномалий эритроцитов является, по-видимому, фактором, ограничивающим интенсивность паразитами и связанной с ней заболеваемости и смертности. Особенно убедительно это было показано у больных с серповидно-клеточной анемией. Развитие паразита замедляется в эритроцитах AS, находящихся в условиях низкого давления кислорода, как, например, в русле капилляров внутренних органов. Тактоиды, формирующиеся при образовании серповидных эритроцитов AS, могут также оказывать негативное воздействие на паразитов и способствовать тому, что деформированные эритроциты становятся более подверженными фагоцитозу. Подобный же эффект, хотя и не столь подробно изученный, наблюдается при талассемии и дефиците глюкозо-6-фосфатдегидрогеназы или пиридоксалькиназы, поскольку эти аномалии обнаруживаются чаше всего в районах распространения малярии. Возможная защита от инвазии отчасти может быть связана с повышенной чувствительностью таких эритроцитов к повреждению окислителями. При талассемии и сходных с ней гемоглобинопатиях постоянная продукция фетального гемоглобина также может иметь определенное значение, поскольку развитие возбудителя тропической малярии замедляется в содержащих гемоглобин эритроцитах. У лиц с меланезийским овалоцитозом своеобразная защита от малярии обеспечивается благодаря ригидности стенки эритроцитов, которая препятствует проникновению в него мерозоитов.
В инфицированных эритроцитах происходит ряд изменений. До 75% гемоглобина в эритроците поглощается и переваривается возбудителем по мере его роста. При паразитировании возбудителя тропической малярии в местах скопления специфического антигена на мембране эритроцита формируются электронно-плотные бугорки. Эти структуры, по-видимому, участвуют в прикреплении инфицированных клеток к эндотелию капилляров и посткапиллярных вен в глубоких тканях, что приводит к внутрисосудистой агглютинации и застою эритроцитов («слэж»). При поражении любым из четырех видов возбудителей малярии эритроциты становятся менее эластичными и, следовательно, более подверженными захвату селезенкой. По мере стимулирования иммунной системы циркуляция эритроцитов по селезеночным тяжам усиливается, захват эритроцитов селезенкой увеличивается, при этом пораженные эритроциты подвергаются тесному контакту с активированными макрофагами. Здесь внутриэритроцитарные плазмодии повреждаются или разрушаются секретируемыми макрофагами цитотоксинами и/или происходит фагоцитоз самих эритроцитов. Избежавшие захвата селезенкой пораженные эритроциты разрушаются в момент меруляции, процесса, вызывающего повышение температуры тела больного. Последнее, как полагают, связано с высвобождением внутриклеточного пирогена, однако участвующие в этом конкретные механизмы остаются неизученными.
Тяжесть анемии при острой малярии часто превосходит степень таковой, которую можно было бы предсказать, учитывая гибель только инфицированных эритроцитов. Это расхождение объясняется рядом факторов. Секвестрация (задержка эритроцитов в селезенке. — примеч. пер.) приводит к заниженной оценке общего числа пораженных эритроцитов, угнетается эритропоэз, и наряду с этим как неинфицированные, так и инфицированные эритроциты исключаются из кровообращения.
Весьма редким, но ярким примером процесса такого рода является гемоглобинурийная лихорадка, сопровождающаяся массивным внутрисосудистым гемолизом. Чаще всего эритроциты разрушаются в рет.икулоэндотелиальной системе печени и селезенки. Иногда отмечается положительная реакция Кумбса. Указанные явления отражаются также и на других компонентах крови. Часто отмечается тромбоцитопения в результате как депонирования крови в селезенке, так и сокращения срока жизни тромбоцитов. Диссеминированное внутрисосудистое свертывание встречается при тяжелом течении тропической малярии, однако в целом отмечается менее чем в 5% случаев. Количество лейкоцитов и лейкоцитарная формула обычно бывают в пределах нормы.
Нарушения кровообращения. За исключением периодов сужения сосудов кожи, которыми сопровождаются приступы озноба при малярии, кожные покровы у лихорадящего больного теплые, кровообращение хорошее, артериальное давление слегка понижено или в пределах нормы, пульс учащен. При тяжелой тропической малярии такое состояние вазодилатации может быть усилено в результате гипотензии и снижения центрального венозного давления. Увеличение пространства, занимаемого сывороточным альбумином, меченным радиоизотопным йодом, и выделения альдостерона и антидуретического гормона свидетельствуют об уменьшении объема эффективно циркулирующей крови вследствие расширения объема сосудистого русла. Функция миокарда сохраняется, несмотря на секвестрацию инвазированных эритроцитов в мелких сосудах сердца. Следует очень тщательно следить за введением больному жидкостей, чтобы избежать двойной опасности, заключающейся в остром некрозе канальцев и отеке легких. Иногда без видимой причины развивается тяжелый шок; такое состояние называется альгидной малярией и, возможно, является вторичным следствием спонтанной бактериемии, вызванной грамотрицательными палочками.
Если малярия заканчивается смертью больного, то почти во всех случаях она наступает в результате окклюзии микроциркуляции во внутренних органах эритроцитами, инвазированными Р. falciparum, что является отражением способности этих возбудителей инфицировать значительную часть эритроцитов у неиммунного больного, а также избирательного прикрепления пораженных эритроцитов к сосудистому эндотелию капилляров и посткапиллярных венул. Хотя указанный процесс охватывает все глубокие ткани, он наиболее выражен в головном мозге. Чаще всего поражаются дети, беременные женщины, туристы, выезжаю щие в эндемичные районы, и другие неиммунные лица или лица с нарушенным иммунитетом, а также лица, у которых уровень паразитемии может превышать 100•109/л.
Метаболические нарушения. Развитие большинства патологических реакций, описанных при тропической малярии, обусловлено местной тканевой гипоксией на участках нарушения микроциркуляции крови. К смертельному исходу может привести молочнокислый ацидоз в результате анаэробного гликолиза в организме хозяина или паразита. У беременных женщин или больных с интенсивной паразитемией значительные метаболические потребности малярийных паразитов могут вызывать выраженную рецидивирующую гипогликемию; индуцированная хинином гиперинсулинемия часто усугубляет эту проблему.
Иммунитет. Иммунный ответ при малярии, контролирующий нелетальные формы болезни и в конечном счете обеспечивающий защиту от реинфекции, изучен недостаточно. Предполагают, что за формирование противомалярийного иммунитетеа у обезьян ответственны как Т-, так и В-лимфоциты. Хотя известно, что. Т-клетки играют важнейшую роль, механизм их действия неясен. Некоторые авторы полагают, что они стимулируют эффекторные клетки, вероятно макрофаги, которые высвобождают при этом неспецифические факторы, способные повреждать или разрушать внутриэритроцитарных паразитов; они могут также способствовать выработке антител.
Штаммоспецифические противомалярийные антитела появляются на раннем этапе паразитемии и затем достигают высоких уровней, что совпадает с падением численности циркулирующих паразитов. Относительная редкость малярии у детей первых месяцев жизни объясняется, наличием у них попавших через плаценту антител IgG. Хотя наличие таких антител не гарантирует полного, иммунитета, исследования in vitro показали, что они способны блокировать инвазию эритроцитов мерозоитами, тормозить внутриклеточный рост паразитов и опсонизировать как мерозоиты, как и инфицированные эритроциты. При малярии у обезьян антигенные изменения плазмодиев приводят к рецидивным циклам паразитемии и выработке вариантоспецифических антител. Представляется вероятным, что аналогичные изменения происходят и у человека, что в конечном счете ведет к исчезновению эритроцитарных форм возбудителя малярии. При тропической малярии в результате этих процессов больной выздоравливает. При малярии трехдневной и овале внутриклеточные печеночные формы возбудителей ускользают от воздействия защитных факторов гуморального иммунитета и позднее могут давать начало новым генерациям малярийных плазмодиев в крови и поддерживать заболевание на протяжении 3—5 лет. Возбудитель четырехдневной малярии вызывает хроническое заболевание исключительно большой длительности (до 53 лет в одном случае), несмотря на отсутствие персистирующей экзоэритроцитарной стадии. Полагают, что это связано с длительным выживанием эритроцитарных форм возбудителя, концентрация которых бывает настолько низкая, что они не обнаруживаются в обычных препаратах крови. Каким образом возбудитель ускользает от воздействия иммунной системы, неизвестно, однако при весьма сходной форме малярии у обезьян спленэктомия быстро ведет к купированию инфекционного процесса, что свидетельствует о возможной защитной роли Т-клеток-супрессоров в селезенке.
Клинические проявления. Общая характеристика. Инкубационный период при трехдневной и тропической малярии составляет обычно 10— 14 дней, четырехдневной малярии — от 8 дней до 6 нед. Однако продолжительность его может увеличиваться при определенных формах трехдневной малярии, приобретенной в зоне умеренного климата, и у лиц, принимавших противомалярийные препараты подавляющего действия (супрессанты). В США интервал между моментом прибытия в страну и началом заболевания превышает 6 мес у 25% больных с трехдневной малярией и 1 мес у такой же части больных с тропической малярией. Имеются некоторые различия в клинических проявлениях малярии, вызванной разными видами возбудителей у неиммунных хозяев, однако для всех форм болезни характерны ознобы, повышение температуры тела, головная боль, боли в мышцах, спленомегалия и анемия. В разгар болезни на губах часто появляются герпетические высыпания. Нередко, особенно при тропической малярии, отмечаются гепатомегалия, умеренная желтушность и отечность. Хроническая малярия часто сопровождается крапивницей.
Отличительным признаком всех видовых форм малярии, кроме тропической, служат лихорадочные пароксизмы. Типичный приступ начинается с озноба, длящегося от 20 до 60 мин — «стадия холода», за которой следует «стадия жара» продолжительностью от 3 до 8 ч с повышением температуры тела до 40—41,7°С. «Стадия пота» характеризуется нормализацией температуры тела, обильным потоотделением, изнеможением больного.
Первые приступы малярии часто бывают тяжелыми и при отсутствии лечения могут повторяться на протяжении нескольких недель. Постепенно они становятся менее регулярными, более редкими и после исчезновения возбудителя из крови прекращаются совсем, знаменуя окончание периода первичных приступов. Рецидивы возникают в тех случаях, когда из персистирующих в печени гипнозоитов снова образуются эритроцитарные стадии возбудителя. В гипер- и голоэндемичных районах (например, в Западной Африке), где имеется интенсивная и постоянная передача возбудителя, дети заражаются малярией впервые в возрасте 6 мес, после снижения уровня материнских антител. Если ребенок переживает период первичных приступов, последующие эпизоды повторных заражений малярией протекают все более умеренно, хотя и при этом может отмечаться определенное ослабление организма, склонное к прогрессированию; у взрослых хронически инфицированных лиц температура тела, как правило, не повышается, причем бывают периоды, характеризующиеся отсутствием каких-либо симптомов болезни. Иммунитет непродолжительный. Если человек выезжает из эндемичных районов и возвращается туда через несколько лет, новое заражение вновь приводит к клинически выраженной форме заболевания. В тех районах мира, где передача малярии происходит с интервалами в случае миграции неиммунных лиц в эндемичные районы, у взрослых людей могут отмечаться клинически выраженные и иногда летальные случаи малярии.
Трехдневная малярия (Р. vivax и Р. ovale). [В нашей стране принято выделять заболевание, вызываемое Р. ovale, в отдельную форму, малярию овале. — Примеч. пер.]. Болезнь характеризуется наличием рецидивов, и, хотя редко заканчивается летально, полностью излечить больного весьма трудно. Началу острого заболевания предшествует продромальный период, сопровождающийся миалгией, головной болью, ознобом и небольшим повышением температуры тела в течение 48—72 ч. В начале лихорадка не носит периодического характера, поскольку циклы Созревания возбудителя не синхронизированы. Синхронизация обычно наступает к концу 1-й недели, вслед за чем приступы начинают повторяться ежедневно. Селезенка становится пальпируемой к концу 2-й недели болезни. При заболевании, вызываемом Р. ovale, симптомы выражены умереннее в период первичных приступов короче, чем при инфекции, вызываемой Р. vivax.
Четырехдневная малярия. Приступы отмечаются каждый третий день и повторяются регулярно. Четырехдневная малярия отличается от всех других форм болезни умеренной тяжестью и выраженной склонностью к хроническому течению; хорошо поддается лечению. Иногда эта форма малярии сопровождается отеками, альбуминурией и гематурией (не гемоглобинурией), клиническим синдромом, аналогичным острому геморрагическому нефриту. Это осложнение не следует путать с гемоглобинурийной лихорадкой. Хроническая четырехдневная малярия может быть связана с развитием уникального с клинической и гистологической точки зрения нефроза. В базальной мембране клубочков наблюдаются гранулярные отложения IgG, IgM, С3-компонента системы комплемента и антигенов возбудителя четырехдневной малярии, что свидетельствует о формировании иммунокомплексной нефропатии. Характерные для этой формы малярии длительные периоды бессимптомной паразитемии объясняют тот факт, что такие случаи часто являются источником трансфузионной малярии. В Африке имеется, по-видимому, положительная связь между паразитемиями, вызванными возбудителями тропической и четырехдневной малярии. В том или ином случае первый из них чаще встречается во время сухого сезона, а последний — в период влажного сезона.
Тропическая малярия. Ввиду асинхронного цикла размножения возбудителя начало болезни может быть постепенным, а лихорадка — постоянной, перемежающейся или нерегулярной. У меньшей части больных отмечаются типичные малярийные приступы. Быстро развивается спленомегалия, от мечаются головные боли, спутанность сознания, постуральная гипотензия, отеки и симптомы поражения желудочно-кишечного тракта. Если при острых приступах лечение проводится своевременно, заболевание протекает в средне-тяжелой форме и заканчивается выздоровлением больного без каких-либо осложнений. У неиммунных лиц при отсутствии лечения секвестрация инвазированных эритроцитов в глубоких тканях может привести к развитию тяжелых осложнений. Угроза появления последних весьма велика, если интенсивность паразитемии превышает 100•109/л возбудителей. К числу угрожающих клинических признаков относятся выраженная анемия, желтуха, гипервентиляция, а также признаки нарушения деятельности центральной нервной системы, такие как делирий, ступор или кома. В зависимости от того, какие преимущественно поражаются органы и системы, возможно развитие одного или нескольких из следующих злокачественных синдромов.
|
|
|
|
|
Дата добавления: 2014-11-20; Просмотров: 603; Нарушение авторских прав?; Мы поможем в написании вашей работы!