
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Химическая связь. Ковалентная, ионнная и металлическая связь. Водородная связь
|
|
|
|
Периодические свойства элементов. Энергия ионизации. Сродство к электрону. Радиус атома.
Перечислим важнейшие из них: радиус атома и атомный объем; потенциал ионизации; сродство к электрону; электроотрицательность атома (рис); степени окисления; физические свойства соединений (плотность, температуры плавления и кипения). Потенциал (энергия) ионизации I - энергия, необходимая для отрыва наиболее слабо связанного электрона от атома: X → Х+ + е. Наименьшие потенциалы ионизации - у щелочных металлов, наибольшие - у инертных газов. Сродство к электрону Е - энергия, которая выделяется при присоединении электрона к атому: X + е → X-. Наибольшее сродство к электрону - у галогенов, наименьшее - у металлов. Радиусом атома-расстояние между атомным ядром и самой дальней из стабильных орбит электронов в электронной оболочке этого атома
Химическая связь - это взаимодействие двух атомов, осуществляемое путем обмена электронами. При образовании химической связи атомы стремятся приобрести устойчивую восьмиэлектронную (или двухэлектронную) внешнюю оболочку, соответствующую строению атома ближайшего инертного газа.
КОВАЛЕНТНАЯ СВЯЗЬ
Осуществляется за счет электронной пары, принадлежащей обоим атомам. Различают обменный и донорно-акцепторный механизм образования ковалентной связи.
1) Обменный механизм. Каждый атом дает по одному неспаренному электрону в общую электронную пару:
| H• + •H ® H: H | 
| ® | 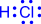
|
2) Донорно-акцепторный механизм. Один атом (донор) предоставляет электронную пару, а другой атом (акцептор) предоставляет для этой пары свободную орбиталь;
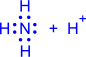
| ® | 
|
Два атома могут обобществлять неcколько пар электронов. В этом случае говорят о кратных связях:

| ® | 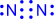
| (или NºN) – тройная связь |
Если электронная плотность расположена симметрично между атомами, ковалентная связь называется неполярной.
Если электронная плотность смещена в сторону одного из атомов, то ковалентная связь называется полярной.
|
|
|
|
|
Дата добавления: 2014-12-16; Просмотров: 481; Нарушение авторских прав?; Мы поможем в написании вашей работы!