
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Предмет органічної хімії. Особливості органічних сполук
|
|
|
|
ВСТУП
Стислий історичний нарис розвитку органічної хімії.
Людина стикалася з органічними сполуками і використовувала їх для своїх практичних потреб з глибокої давнини. Давні народи знали різноманітні природні органічні сполуки і переробляли їх на їжу (хліб), напої (вино, пиво), одяг, пофарбований природними барвниками, паливо тощо. Це був період практичного використання органічних речовин, хоча хімії як науки ще не існувало.
VIII—XVI ст. — період алхімії. У цей час основна увага приділялася пошукам «філософського каменя» — особливої речовини, за допомогою якої нібито можна було перетворити неблагородні метали на золото, а також створенню еліксиру життя — «золотого напою». Значного розвитку вивчення органічних речовин на той час ще не набуло, однак уже існувала класифікація хімічних сполук (поки що примітивна) — за зовнішніми ознаками.
Наприкінці XVI ст. починається новий період розвитку хімії. З появою промислового виробництва накопичуються речовини, як виділені з природних джерел, так і такі, що не існують у природі у вільному стані. Виникають поняття «органічні речовини» й «органічна хімія», їх увів у 1806 р. шведський хімік Й. Берцеліус, на думку якого органічними є речовини, що наявні в рослинних і тваринних організмах. Зазначивши деякі особливості органічних сполук, він виділив органічну хімію у самостійну науку. Його основною помилкою було уявлення про участь недоступної для пізнання «життєвої сили» в утворенні й перетвореннях органічних речовин, а звідси й неможливість добування таких речовин поза організмом. Таким чином на деякий час це стало перешкодою на шляху розвитку органічної хімії.
Ще за життя Й. Берцеліуса було проведено експериментальні дослідження, в яких доводилась можливість утворення органічних речовин поза рослинним або тваринним організмом, наприклад синтез щавлевої кислоти (Ф. Велер, 1824 p.), сечовини (Ф. Велер, 1828 p.), аніліну (М. М. Зінін, 1842 p.), оцтової кислоти (А. В. Кольбе, 1845 p.), жирової (П. Бертло, 1854 р.) і цукристої (О. М. Бутлеров, 1861 р.) речовин тощо. Після цього почався період розвитку синтетичної органічної хімії (сучасний період органічної хімії).
З сучасної точки зору, органічна хімія — це наука, яка вивчає сполуки Карбону з іншими елементами і закони, за якими утворюються ці сполуки. Тому органічну хімію називають ще хімією сполук Карбону (за винятком найпростіших його сполук — карбонатної кислоти та її солей, оксидів карбону, ціановодню).
Більшість органічних сполук містить у своєму складі крім Карбону ще й Гідроген. Тому й досі діє класичне визначення К. Шорлеммера (1871 р.) — органічна хімія є хімією вуглеводнів та їх похідних, тобто продуктів, які утворюються у разі заміни атомів Гідрогену на інші атоми або групи атомів.
Молекули багатьох органічних сполук містять крім Карбону та Гідрогену атоми інших елементів — Оксигену, Нітрогену, Сульфуру тощо. Ці елементи назвали органогенними.
Є кілька передумов виділення органічної хімії в окрему галузь науки. Насамперед - це численність і різноманітність органічних сполук. Нині відомо понад 10 млн. органічних сполук, що набагато перевищує кількість неорганічних речовин (останніх відомо близько 700 тис). Така численність органічних сполук зумовлюється здатністю атомів Карбону сполучатись один з одним, утворюючи ланцюги й кільця (цикли) з практично необмеженою кількістю атомів, а також сполучатися з атомами більшості елементів періодичної системи. Крім того, атоми Карбону утворюють один з одним не лише прості (одинарні, ординарні), а й кратні (подвійні, потрійні) зв'язки. Завдяки таким особливостям атома Карбону серед органічних сполук дуже поширене явище ізомерії.
Органічні сполуки складніші, ніж неорганічні, а органічна хімія вивчає більш високоорганізовану матерію. Органічні сполуки відіграють важливу роль у процесах життєдіяльності рослинних і тваринних організмів. Вони мають виключне практичне значення у багатьох галузях народного господарства. Природний газ, нафта, синтетичні волокна і пластмаси, медичні препарати, вітаміни, пестициди, харчові добавки (емульгатори, антиоксиданти, консерванти тощо) є органічними речовинами.
Виникнення і сировинні джерела органічних сполук. У природі органічні сполуки утворюються з карбондіоксиду (карбон(ІУ) оксиду) і води в процесі фотосинтезу, що відбувається в зеленому листі під дією сонячного випромінювання. Органічні сполуки з'явилися на Землі ще до виникнення життя на ній. Так, у газах первинної земної атмосфери під дією сильного радіоактивного випромінювання та інтенсивних атмосферних розрядів могли спостерігатися реакції типу:
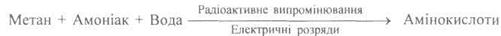
Можливість перебігу таких реакцій була доведена експериментально в лабораторних умовах. Виникнення органічних сполук у природі без участі живої матерії називається абіотичним процесом на відміну від біотичного процесу — виникнення органічних сполук у живій клітині.
Природними сировинними джерелами органічних сполук є нафта і природний газ, кам'яне вугілля та продукти його коксування, буре вугілля, горючі сланці, торф, деревина та продукти її сухої перегонки і гідролізу, тваринна сировина (вовна, шкури, пух) тощо.
Розвиток теоретичних уявлень в органічній хімії. Теорія хімічної будови. Перші теоретичні уявлення в органічній хімії пов'язані з електрохімічною теорією Й. Берцеліуса, згідно з якою речовини складаються з електронегативних і електропозитивних атомів або груп атомів, що утримуються в молекулі силами електростатичного притягання.
Перша теорія органічної хімії — теорія радикалів — виходила з того, що в багатьох перетвореннях органічних речовин певна група атомів, названа «радикалом», у незмінному вигляді переходить із вихідної сполуки в продукт реакції. На думку авторів теорії (Й. Берцеліуса, Ю. Лібіха, Ф. Велера), молекула органічної сполуки складається з двох протилежно заряджених радикалів, що утримуються разом за рахунок електростатичної взаємодії. Принциповим недоліком цієї теорії було те, що вона не ставила питання про будову самого радикала.
На зміну теорії радикалів у 40-х роках XIX ст. прийшла теорія типів (Ш. Ф. Жерар, О. Лоран), в якій основна увага приділялася тій частині молекули органічної сполуки, що змінюється в процесі реакції. Ця теорія ґрунтувалася на уявленні про те, що в органічній хімії існують певні типи, які зберігають свій характер навіть після заміщення Гідрогену в них еквівалентною кількістю, наприклад, Хлору, Брому або якоюсь групою атомів. У цій теорії органічні сполуки розглядаються як похідні неорганічних, утворені заміщенням атомів у молекулі на групи, що мають назву «залишки», а добуті в результаті органічні речовини вступають у всі реакції, характерні для неорганічних. У зв'язку з цим було виділено кілька основних типів: тип водню, хлороводню, води, амоніаку та болотного газу.
Одним із перших було визначено тип води, до якого належать оксигеновмісні органічні сполуки:
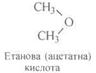
|

|

|
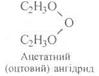
|
Теорія типів дала змогу створити подібну до сучасної класифікацію органічних речовин, так звану «унітарну» систему, в якій органічні сполуки були поділені на класи зі спільними хімічними властивостями. Крім того, за належністю речовини до певного класу іноді було можливим передбачити способи її добування і деякі хімічні властивості.
До 60-х років XIX ст. в органічній хімії вже було накопичено величезний матеріал, що потребував систематизації і пояснення. Головною проблемою було з'ясування питання про те, є молекули частками певної будови чи хаотичним нагромадженням атомів. Успішному розв'язанню цього питання сприяло встановлення чотиривалентності Карбону (А. Ф. Кекуле, А. В. Кольбе).
Відкриття валентності взагалі, а особливо валентності Карбону, впритул підводило до думки про певну будову молекул.
Основи теорії хімічної будови були закладені А. Я. Купером (1858 p.), який вважав, що всі особливості органічних сполук можна пояснити, враховуючи лише дві властивості атомів — валентність і зв'язок. Він також дійшов важливого висновку про здатність атомів Карбону сполучатись у ланцюги і запропонував зображувати зв'язки між атомами за допомогою рисок. Значний внесок у розвиток структурної теорії зробив Ф. А. Кекуле, який не тільки встановив чотиривалентність Карбону, а й увів тип метану, запропонував відому формулу бензену (бензолу), а також сформулював одне з основних завдань органічної хімії того часу — встановлення істинної будови молекул. Усі перелічені відкриття зумовили створення теорії хімічної будови органічних речовин.
Основні положення теорії хімічної будови були сформульовані і доведені О. М. Бутлеровим (1861 р.) на основі фактичного матеріалу:
1.У молекулах органічних речовин атоми сполучені один з одним у певній послідовності відповідно до їх валентності. Ця послідовність, або порядок зв'язку атомів у молекулі, називається хімічною будовою.
2.Властивості молекул визначаються не тільки типом і кількістю атомів у молекулі (якісним і кількісним складом молекули), а й порядком їх сполучення, тобто хімічною будовою.
3.Органічні сполуки з однаковим якісним і кількісним складом, але різною будовою, називають ізомерами. Вони різняться за фізичними, а вбільшості випадків і за хімічними властивостями.
4.Атоми або групи атомів у складі молекули взаємно впливають один на одного, а через це й на хімічну поведінку (реакційну здатність) молекули.
5.Оскільки під час окремих реакцій змінюються не всі, а лише деякі частини молекули, то, вивчаючи продукти хімічних перетворень речовини, можна встановити її хімічну будову.
Теорія хімічної будови дала можливість хімікам проводити експерименти цілеспрямовано. Її великим успіхом було пояснення явища ізомерії, відкритого ще в першій чверті XIX ст. О. М. Бутлеров докладно вивчив явище структурної ізомерії (наприклад, хімічна поведінка бутану й ізобутану, етанолу і діетилового етеру), відкрив і вперше пояснив явище динамічної ізомерії (таутомерії), розглянув явища гомології та ізології. Його учні (В. В. Марковніков, О. М. Зайцев і Е. Е. Вагнер) глибоко дослідили взаємний вплив атомів у молекулах органічних сполук.
О. М. Бутлеров вважав, що теорія хімічної будови розвиватиметься в міру накопичення нового практичного матеріалу. Він передбачав, наприклад, існування зв'язку між просторовою будовою і властивостями органічних молекул. Теорія хімічної будови створила можливість систематизації практичного матеріалу органічної хімії, пояснила її найважливіші закономірності і стала основою для прогнозування нових фактів, тобто основою для створення теорій сучасної органічної хімії.
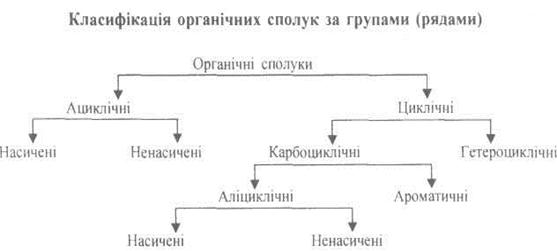
Класифікація органічних сполук. Основою сучасної класифікації органічних сполук є теорія хімічної будови. Залежно від будови ланцюга атомів Карбону молекули органічні сполуки поділяють на дві великі групи сполук: нециклічні та циклічні. Нециклічні, або ациклічні (від грец. а — префікс, що означає заперечення, відсутність чогось), сполуки називають ще аліфатичними, або сполуками жирного ряду. В їхніх молекулах атоми Карбону сполучені в нерозгалужені або розгалужені «розкриті» ланцюги, що не містять циклів, або кілець. У молекулах циклічних сполук цикли можуть утворюватись або тільки атомами Карбону (вони складають групу карбоциклічних сполук), або в побудові циклів крім Карбону можуть брати участь атоми інших елементів, наприклад Оксигену, Нітрогену, Сульфуру тощо. Останні належать до гетероциклічних сполук (від грец. єхероо — інший), або просто гетероциклів.

|
Залежно від характеру зв'язків у ланцюгу атомів Карбону карбоциклічні сполуки поділяються на аліциклічні та ароматичні. Ароматичні містять у молекулах замкнену систему кон'югованих зв'язків, так званий ароматичний зв'язок, який буде докладно розглянуто далі. Це бензен, нафтален, антрацен тощо. Всі інші карбоциклічні, або ізоциклічні, сполуки
можуть містити ординарні або кратні зв'язки і бути, відповідно, насиченими або ненасиченими. Аналогічно на насичені й ненасичені поділяються й ациклічні сполуки (табл. 1).
Кожна із зазначених груп органічних сполук поділяється на класи залежно від наявності в молекулах тих чи інших атомів або угруповань атомів, які визначають типові хімічні властивості даного класу,— так званих функціональних груп. Розглянемо деякі найхарактерніші функціональні групи і відповідні їм класи органічних сполук. До складу молекули органічної сполуки може входити одна або кілька функціональних груп. У таких випадках ідеться, відповідно, про моно- або багатофункціональні сполуки.
КЛАСИФІКАЦІЯ ОРГАНІЧНИХ СПОЛУК
Принципи номенклатури органічних сполук. Розвиток органічної хімії потребує однозначного найменування органічних сполук.
1. Тривіальні назви були першими з назв органічних сполук. Вони відображають не структуру сполуки, а деякі її властивості, зовнішні ознаки або походження. Наприклад, мурашина кислота вперше була виділена з мурашок; винний спирт — вилучений при виготовленні вина; анілін — від арабського ан-ніл (аль-ніл) — блакитний; пікринова кислота — від грец. лікроо — гіркий тощо. Для деяких простих і давно відомих сполук тривіальні назви збереглись і вживаються й досі.
2. Раціональна номенклатура була запропонована для простих сполук і давала можливість відобразити в назві структуру, а також розв'язати зворотну задачу — побудувати за назвою формулу. В основу раціональної номенклатури покладено назви вуглеводнів. У кожному класі органічних сполук будь-яка сполука розглядається як перший член гомологічного ряду таких сполук, у молекулі якого один або кілька атомів Гідрогену заміщені на вуглеводневі залишки. Раціональну номенклатуру використовують не для всіх типів похідних вуглеводнів, по-перше, тому, що для деяких сполук раціональні назви є занадто складними, а, по-друге, для певних класів сполук традиційно використовують тривіальні назви (наприклад, для амінокислот).
3. Радикало-функціональна (замісникова) номенклатура наближається до раціональної тим, що вуглеводневі залишки (застаріла назва — радикали) мають за нею ті самі назви, що й за раціональною номенклатурою. Відмінність полягає в тому, що назва за радикало-функціональною номенклатурою складається з двох елементів — групової назви,що відповідає певній функціональній групі, і назви вуглеводневого залишку (або кількох залишків — відповідно до валентності функціональної групи), сполученого з цією функціональною групою. Такі назви поширені для простих похідних вуглеводнів.
4. Систематична номенклатура є найбільш досконалим способом словесного опису структури органічних сполук і може бути застосована в усіх випадках (для всіх класів органічних сполук). Найчастіше систематичні назви ґрунтуються на принципі заміщення, тобто будь-яка сполука розглядається як нерозгалужений вуглеводень — ациклічний чи циклічний, в молекулі якого один або кілька атомів Гідрогену заміщені іншими атомами і групами, в тому числі вуглеводневими залишками. Сучасній систематичній номенклатурі передувала Женевська номенклатура (затверджена міжнародною нарадою представників хімічних товариств у 1892 р. у Женеві), доповнена пізніше Льєжськими правилами (1930 p.). З розвитком органічної хімії систематична номенклатура постійно вдосконалюється і доповнюється; за цим слідкує комісія з номенклатури Міжнародної спілки теоретичної і прикладної хімії (International Union of Pure and Applied Chemistry—ЫUPAC). Тому систематична номенклатура ще має назву номенклатура ІUPAC.
На межі зазначених видів номенклатури перебувають напівтривіальні або напівсистематичні назви. Вони засновані на тривіальних назвах, але використовують префікси, суфікси або закінчення, типові для систематичної номенклатури (наприклад, назви деяких вуглеводнів, амінокислот).
В Україні питаннями хімічної номенклатури займається Національна комісія з хімічної термінології і номенклатури (УНКоХіТерН), створена 1992 року при Київському національному університеті ім. Тараса Шевченка. Наведені в цьому посібнику назви хімічних елементів і сполук ухвалені УНКоХіТерН і відповідають державному стандарту України ДСТУ 2439-94 «Елементи хімічні і речовини прості. Терміни та визначення основних понять. Умовні позначення».
Сучасна українська хімічна термінологія максимально наближена до відповідних латинських назв на відміну від традиційного перекладу-кальки з російської мови. За упорядкованими з точки зору української наукової мови правилами систематичної номенклатури чітко розрізняються назви хімічних елементів і відповідних простих речовин: українські назви хімічних елементів розглядаються як власні назви і пишуться з великої літери, тоді як назви простих речовин, а також традиційні, технічні і систематичні назви хімічних сполук, як і раніше — з малої літери, наприклад, елементи Карбон (С), Гідроген (Н), Оксиген (О), Нітроген (N), Сульфур (S), але прості речовини алмаз, графіт, карбін і фулерен — як алотропні модифікації Карбону, гази: водень, кисень і азот, аморфна чи кристалічна сірка тощо. Написання з малої літери стосується і похідних від них термінів — карбоновий, вуглеводи, вуглеводні, азотування, окиснення.
Застосування в основі латинських назв показує генетичний зв'язок між назвою елемента і його сполуками: Карбон — карбонові кислоти, карбоксил, карбоніл, карбаніон; Гідроген — гідрогенування, гідрогенізація, гідро-ксигрупа; Нітроген — нітрати, нітрил, нітрогрупа, нітрування тощо.
Використання сучасної української номенклатури дає змогу уникнути тих непорозумінь і відхилень від систематичної номенклатури, що виникають у результаті калькування українських термінів із російських. Наприклад, у російській номенклатурі одноядерні арени мають назви бензол, толуол, ксилоли тощо, хоч суфікс -ол за правилами IUРАС вказує на наявність спиртової групи (якої в цих сполуках немає). Найпростіший двох'ядерний арен з конденсованими ядрами — нафталін (хоч суфікс -ін указує на наявність потрійного зв'язку). У найновішій українській номенклатурі вживаються назви бензен, толуен, ксилени, нафтален тощо, які відповідають англійським термінам benzene, toluene, xylene, naphthalene (суфікс -ен вказує на подвійний зв'язок, який хоч би формально є в молекулах цих сполук).
Відродження і становлення української термінології дає змогу повернути вдалі терміни, наближені до міжнародних стандартів, такі як етер, естер, естерифікація, що вперше з'явилися в українських словниках ще в 20-х роках XX сторіччя, але були витіснені копіюванням невдалих російських термінів простий ефір та складний ефір. Зараз треба вживати терміни етер (англ. ether) — на заміну поняття простий ефір, етерифікація — утворення етеру, естер (англ. ester) — на заміну поняття складний ефір, естерифікація — утворення естеру.
Не треба забувати, що українська назва Іод, що походить від латинського iodum (англійська назва — iodine), цілком відповідає хімічному символу цього елемента — І, впровадженому за пропозицією IUPAC ще в 1962 р. на заміну застарілого символа J.
Сучасна українська хімічна номенклатура є доцільною і з точки зору застосування комп'ютерів у наукових дослідженнях. Чітке розмежування назв елементів і простих речовин, тобто усунення синонімії в хімічних термінах, дає змогу використовувати комп'ютерні програми, за допомогою яких можна складати за правилами IUРАС назви більшості органічних сполук відповідно до їх структурних формул. Одна з таких програм — AUTONOM (від англ. aromatic «owenclature»).
|
|
|
|
|
Дата добавления: 2014-11-29; Просмотров: 3501; Нарушение авторских прав?; Мы поможем в написании вашей работы!