
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Значения Cv, Cp, к
|
|
|
|
Сопоставление результатов расчёта по формулам (1.22) и (1.24) зависимости «давление - объём» для азота
| Р, атм | 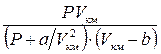
|
| 1,00 | 1,000 |
| 1,004 | |
| 1,038 | |
| 1,371 | |
| 2,317 |
Отдельно следует остановиться на количественном определении удельных теплоёмкостей Cv и Cp различных газов.
Согласно кинетической теории газа теплоёмкость киломоля идеального газа при постоянном объёме определяется соотношением
Cv 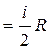 , (1.25)
, (1.25)
где i – сумма числа поступательных, числа вращательных и удвоенного числа колебательных степеней свободы молекулы (у молекул с жёсткой связью колебательные степени свободы отсутствуют).
Из соотношения (1.25) следует, что теплоёмкость идеального газа Cvоказывается постоянной величиной.
Теплоёмкость идеального газа при постоянном давлении определяется соотношением (1.7)
Cp=Cv+AR
Выше приводилось значение газовой постоянной R в Дж /(град×моль) и кал /(град×моль). При R =1,99 кал /(град×моль) коэффициент А =1 и соотношение (1.7) записывается в виде
Cp=Cv+R (1.26)
В табл.2 приведены значения Cv,Cp и к = Cp/Cv для газов, состоящих из одноатомных, двухатомных и многоатомных молекул.
Таблица 2
| Молекула | Характер связи между атомами | Число степеней свободы | i | Cv | Cp | к | ||
| Посту-патель-ные | Вра-щатель-ные | Коле батель ные | ||||||
| Одноатомная | - | - | - |  R R
|  R R
| 1,67 | ||
| Двухатомная | жёсткая | - |  R R
| 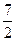 R R
| 1,4 | |||
| Двухатомная | упругая | 1* | 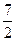 R R
|  R R
| 1,29 | |||
| С числом атомов три и более | жёсткая | - | 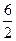 R R
| 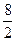 R R
| 1,33 |
Примечание: индекс (*) указывает на необходимость удвоения числа данных связей.
|
|
|
|
|
Дата добавления: 2014-12-27; Просмотров: 780; Нарушение авторских прав?; Мы поможем в написании вашей работы!