
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Лекарственные средства альдегидов
|
|
|
|
Фармацевтический анализ лекарственных средств альдегидов и углеводов
Лабораторно-практическое занятие № 17
Перечень лекарственных средств – альдегидов и углеводов в соответствие с учебной программой:
· Раствор формальдегида 35% / Solutio Formaldehydi
· Хлоралгидрат / Chloralum hydratum
· Гексаметилентетрамин / Hexamethylentetraminum
· Глюкоза / Glucosum
· Галактоза / Galactosum
· Сахароза / Saccharum
· Лактоза / Lactosum
· Крахмал / Amyla
Альдегидами называются органические соединения, в которых карбонильная группа связана с водородом и с алифатическим или ароматическим углеводородным радикалом:
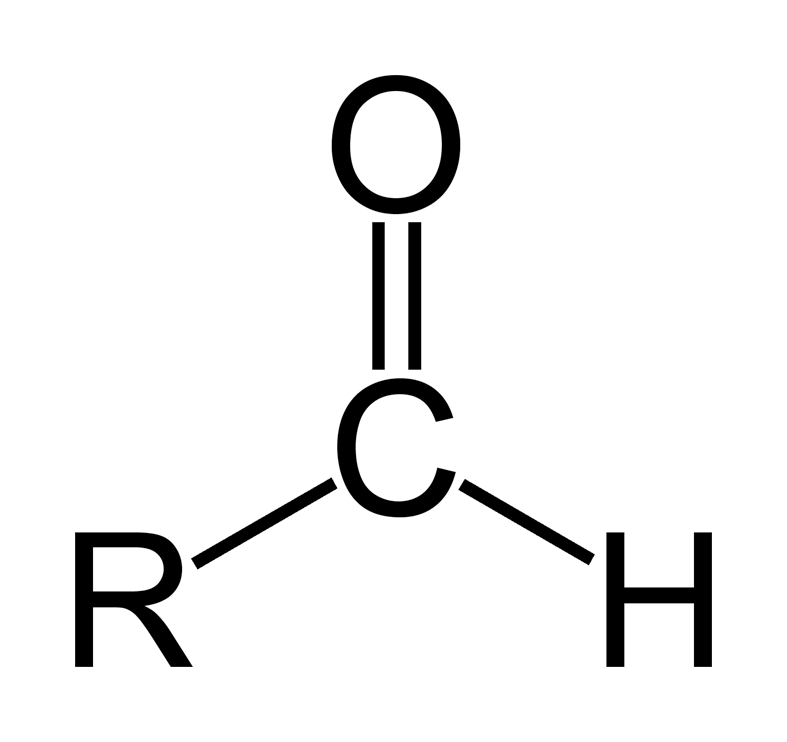
У альдегидов сохраняются наркотические свойства, присущие спиртам. Альдегиды, как и спирты, обладают дезинфицирующими свойствами. Однако альдегидная группа усиливает токсичность вещества. В ряду альдегидов наркотические свойства усиливаются при удлинении алкильного радикала и при введении галогена в молекулу. При повышении наркотического действия альдегидов одновременно и в той же последовательности растет и их токсичность.
Поскольку водород и углерод имеют близкие значения относительной электроотрицательности, в альдегидах практически отсутствуют межмолекулярные водородные связи, поэтому температуры кипения альдегидов ниже, чем у соответствующих спиртов или карбоновых кислот.
Низшие альдегиды хорошо растворимы в воде. При удлинении углеродной цепи растворимость в воде снижается. Альдегиды растворяются в органических растворителях, например в спиртах и эфирах. Низшие альдегиды имеют резкий запах, у альдегидов с 3-6 углеродными атомами весьма неприятный запах, в то время как высшие альдегиды обладают цветочными запахами и применяются в парфюмерии.
В химическом отношении альдегиды — весьма реакционноспособные соединения. Наиболее характерны для альдегидов реакции нуклеофильного присоединения, что обусловлено присутствием в молекуле электрофильного центра — атома углерода карбонильной группы. Для них характерны реакции полимеризации, конденсации и окисления.
Свойства ЛСгалогенпроизводные альдегидов описаны в таблице 17-1:
Таблица 17-1. Лекарственные средства производные альдегидов
| Лекарственное вещество Структурная формула | Описание Фармакологическая группа, применение |
| Раствор формальдегида35%
Solutio Formaldehydi
| Прозрачная, бесцветная жидкость. Смешивается с водой и этанолом (96%). Оказывает антисептическое и дезодорирующее действие. Применяется при повышенном потоотделении. |
Хлоралгидрат
Chloralum hydratum
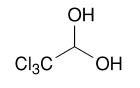 2,2,2-трихлороэтан-1,1-диол
2,2,2-трихлороэтан-1,1-диол
| Бесцветные прозрачные кристаллы. Очень легко растворим в воде, легко растворим в этаноле (96%). Успокаивающее, снотворное и анальгезирующее средство. Используется при психическом возбуждении и как противосудорожное средство при спазмофилии, столбняке и т. п. |
Гексаметилентетрамин
Hexamethylentetraminum
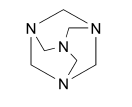 1,3,5,7-тетраазотрициклодекан
1,3,5,7-тетраазотрициклодекан
| Белый или почти белый кристаллический порошок, или бесцветные кристаллы. Легко растворим в воде, растворим в этаноле (96%) и метиленхлориде. Противомикробное средство. Активен в отношении большинства микроорганизмов, вызывающих заболевания мочевыводящих путей. Оказывает дозозависимый бактерицидный или бактериостатический эффект. Является пролекарством — после расщепления в кислой моче высвобождается формальдегид, денатурирующий белковые структуры микробов. |
Раствор формальдегида 35% / Solutio Formaldehydi
формальдегид
СН2О Mr 30,0
Содержит от 34,5% до 38,0% формальдегида. В качестве стабилизатора содержит метанол.
Определение подлинности
10 мл раствора формальдегида разводят водой до 50 мл (раствор S). Далее 1 мл раствора S разводят водой до 10 мл. К 0,05 мл полученного раствора добавляют 1 мл 15 г/л раствора натриевой соли хромотроповой кислоты, 2 мл воды и 8 мл H2SO4. В течение 5 минут появляется сине-фиолетовое или красно-фиолетовое окрашивание.
К 0,1 мл раствора S добавляют 10 мл воды, 2 мл 10 г/л раствора фенилгидразина гидрохлорида, 1 мл раствора феррицианида калия и 5 мл HCl. Появляется интенсивное красное окрашивание. При этом формальдегид реагирует с фенилгидразином с образованием фенилгидразона, который при взаимодействии с раствором калия феррицианида K3[Fe(CN)6] вступает в реакацию замещения лигандов (CN-) во внутренней сфере комплексного иона, при этом образуется продукт красного цвета.
Реакция серебряного зеркала: смешивают 0,5 мл раствора формальдегида с 2 мл воды и 2 мл раствора AgNO3, добавляют раствор аммиака до слабо щелочной реакции среды, и нагревают на водяной бане. Выпадает серый осадок или на стенках пробирки формируется «серебряное зеркало».
Реакция конденсации с салициловой кислотой: 0,1 г салициловой кислоты растворяют в 5 мл H2SO4, и добавляют 2 капли раствора формальдегида, нагревают. Образуется ауриновый (арилметановый) краситель красного цвета.

|
|
|
|
|
Дата добавления: 2014-12-26; Просмотров: 7012; Нарушение авторских прав?; Мы поможем в написании вашей работы!