
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Оценка чистоты. Раствор S (см. выше) должен быть бесцветным
|
|
|
|
Раствор S (см. выше) должен быть бесцветным.
Кислотность определяют индикаторным методом: к 10 мл раствора S добавляют 1 мл фенолфталеина. Не более 0,4 мл 0,1 моль/л раствора NaOH требуется для изменения цвета индикатора.
Содержание метанола определяют методом газовой хроматографии.
Сульфатная зола - не более 0,1% на 1,0 г вещества.
Количественное определение проводят методомобратного йодометрического титрования.
В мерную колбу на 100,0 мл вносят 2,5 мл воды и 2 мл раствора NaOH, добавляют 1,000 г раствора формальдегида, взбалтывают и доводят водой до метки. К 10,0 мл полученного раствора добавляют 30,0 мл 0,05моль/л раствора йода. Перемешивают и добавляют 10 мл раствора NaOH. Через 15 минут добавляют 25 мл разведенной H2SO4 и 2 мл раствора крахмала. Титруют 0,1 моль/л раствором натрия тиосульфата.
Определение основано на окислении альдегидной группы стандартным раствором йода в щелочной среде, где протекает реакция диспропорционирования с образованием натрия гипойодита и йодида:
Образовавшийся гипойодит окисляет формальдегид в щелочной среде до натриевой соли муравьиной кислоты:
При добавлении избытка серной кислоты не прореагировавший гипойодит натрия выделяет йод, который оттитровывают стандартным раствором тиосульфата натрия.
1 мл 0,05 моль/л раствора йода эквивалентен 1,501 мг СН2О.
Хлоралгидрат / Chloralum hydratum
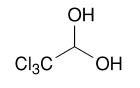
2,2,2-трихлороэтан-1,1-диол
С2H3Cl3O2 Mr 165,4
Содержание действующего вещества в субстанции должно составлять не менее 98,5% и не более 101,0%.
|
|
|
|
|
Дата добавления: 2014-12-26; Просмотров: 913; Нарушение авторских прав?; Мы поможем в написании вашей работы!