
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Хід роботи. Матеріали та обладнання
|
|
|
|
Матеріали та обладнання
Реактиви
1. А – 2%-ний розчин Na2CO3 в 0,10 M NaOH;
2. Б – 0,3%-ний розчин CuSO4×5H2O в 1%-ному розчині двузаміщеного Na- або К-тартрату;
3. В – для приготування лужного розчину міді змішують 50 мл реактиву А та 1 мл реактиву Б. Придатний для використання протягом 2 діб;
4. Г – змішують 50 мл 2%-ного розчину Na2CO3 з 1 мл реактиву Б. Придатний для використання 1 добу;
5. Д – реактив Фоліна-Чікольте. Після приготування використовують в той же день. Використовують готовий реактив з більш довгим терміном зберігання при 0-40 С. Такий реактив перед використанням титрують аліквоту до рН 10,0 по фенолфталеїну, на основі результатів титрування розбавляють реактив приблизно в 2 рази до концентрації 1 моль/л.
6. Бичий сироватковий альбумін (БСА).
7. Суспензії білків невідомої концентрації.
1. Фотометричне обладнання здатне вимірювати оптичну щільність розчинів при довжині хвилі 750 нм в діапазоні 0-1,0 одиниць оптичної щільності;
2. Кювети з довжиною оптичного шляху 5 мм;
3. Аналітичні ваги
4. Колба мірна ємністю 500 мл,
5. Штатив з пробірками ємністю 10 мл;
6. Піпетки місткістю 0,1; 1,0 та 5,0 мл
7. Міліметровий папір, олівець, лінійка
1. Побудова калібрувальної кривої.
У флакон, який містить 5 мг ліофілізованого бичого сироваткового альбуміну (БСА) або γ-глобуліну та ін., обережно додають 5 мл фізіологіч-ного розчину NaCl (концентрація маточного розчину 1мг/1мл). Потім легкими обертальними рухами перемішують до повного розчинення. Зберігати при температурі від +2 до +4 град.С.
В окремих пробірках розводять маточний розчин для побудуви калібрувальної кривої як показано в таблиці (табл.1)
Таблиця 1.
Схема розведення БСА для побудови калібрувальної кривої
| Розчин БСА (мл) | Фіз.р-н (мл) | Кільк. білку (мг/мл) | Поглинання |
| 0,025 | 0,975 | 0,025 | |
| 0,05 | 0,950 | 0,05 | |
| 0,1 | 0,9 | 0,1 | |
| 0,2 | 0,8 | 0,2 | |
| 0,3 | 0,7 | 0,3 | |
| 0,4 | 0,6 | 0,4 | |
| 0,5 | 0,5 | 0,5 |
До 1 мл білкового розчину додають 4 мл суміші розчинів А и В. Струшують і залишають на 10 хв при кімнатній температурі. Потім швидко доливають 0,4 мл реактиву Фоліна, енергійно перемішують і залишають на 30-90 хв для розвитку забарвлення. Жовте забарвлення розчину поступово переходить у синє. Оптичну щільність розчину вимірюють на фотоелектро-колориметрі при 750 нм (червоний світлофільтр), кювета 5 мм.
За одержаними даними будують калібрувальну криву. Величину поглинання відкладають по осі ординат, а відповідну їй концентрацію білку в пробі по осі абсцис.
2. Визначення невідомих концентрацій розчинів білків
Для аналізу беруть три пробірки на 10 мл (1-ша контроль, 2-га та 3-тя розчини білків невідомої концентрації). В дослідні пробірки вносять 0,4 мл розведеного в ???? разів розчину білку невідомої концентрації, а в контрольну – 0,4 мл фізіологічного розчину або води. В обидві пробірки доливають по 2 мл реактиву В, перемішують і залишають на 10 хвилин.Потім швидко доливають 0,3 мл реактиву Д, перемішують (загальний об¢єм ????? мл), витримують 30 - 40 хв. і вимірюють поглинання проти “холостої” проби (1-ша пробірка, де замість білку прилити рівний об¢єм води або фізіологічного р-ну) при 750 нм (червоний світлофільтр), кювета 5 мм.
ΔD
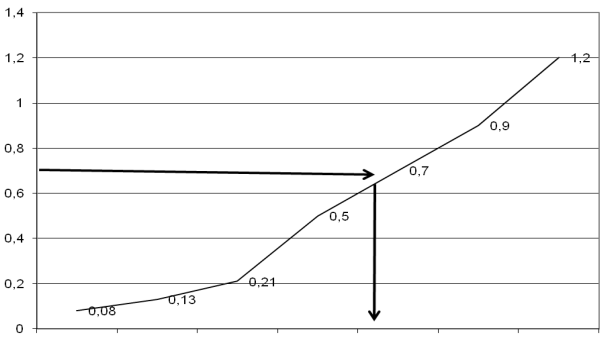
0,025 0,05 0,1 0,2 0,4 0,5
Концентрація білку, мг/мл
Рис. Визначення концентрації білку по калібрувальній кривій
Вміст білку в розчинах невідомої концентрації знаходять за калібруваль-ною кривою. Для цього величину поглинання для кожної проби знаходять на осі ординат, з’єднують цю точку горизонтальною прямою з калібрувальною кривою і з точки перетину опускають перпендикуляр на вісь абсцис. Точка його перетину з віссю абсцис покаже вміст білку в пробі в мг/мл в пробі. Потім роблять розрахунок концентрації білку з урахуванням розведення.
Примітка. Інтенсивність забарвлення визначається природою білку. На розвиток забарвлення впливає наявність в розчині сахарози та тритону Х-100.
|
|
|
|
|
Дата добавления: 2015-05-23; Просмотров: 397; Нарушение авторских прав?; Мы поможем в написании вашей работы!