
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Хід роботи. Цитохроми відіграють важливу роль в метаболізмі ксенобіотиків в організмі людини (метаболізують біля 60% лікарських речовин)
|
|
|
|
Мал. Будова гема
Цитохроми відіграють важливу роль в метаболізмі ксенобіотиків в організмі людини (метаболізують біля 60% лікарських речовин), здійснюють реакції окиснення молекулярним киснем органічних сполук і є важливим елементом системи детоксикації ксенобіотиків. Локалізовані, в основному, в мембранах, а в еукаріотів (рослини та тварини) - в мітохондріальних мембранах та ендоплазматичному ретикулумі.
Цитохром Р450 має широку субстратну специфічність, утворює свою ізоформу для кожного субстрату. Сім¢я ізоформ цитохрому Р450 бере участь в великій кількості реакцій з ксенобіотиками. Цими субстратами можуть бути нормальні клітинні компоненти, метаболіти таких реакцій вводяться в шляхи метаболізму клітин. Однак субстратами цитохрому Р450 можуть бути речовини, що не є компонентами клітин живих організмів. Це можуть бути хімічні сполуки, лікарські засоби. Цитохром Р450 може приймати участь в детоксикації чужорідних сполук (ксенобіотиків). В цих випадках під дією цитохрома Р450 сполуки перетворюються в продукти, що можуть мати цитостатичні, мутагенні та канцерогенні властивості.
Цитохром b5. Мембранний білок, що каталізує перенесення електронів, входить до складу білків ендоплазматичних мембран. Має 93 амінокислотних залишки і одну гемову групу, що пов¢язана з білком двома гістидиновими залишками, які є аксиальними лігандами. Цитохром b5 є одним з компонентів системы цитохрому Р450. Цитохром b5 є гемопротеїном, гемова група представлена гемом. Фермент (мікросомальна ізоформа) бере участь в окисно-відновних реакціях, що проходять в клітинах організму, в якості переносника
електронів. Всі відомі ізоформи цитохрому b5 можна разділити на 2 групи - розчинні та мембранопов'язані. Розчинна форма локалізована в еритроцитах. Мембранопов'язана ізоформа цитохрому b5 має мітохондріальну і мікросо-мальну формы, які пов'язані з відповідними органелами клітин в органах і тканинах.
Самостійна робота студентів
1. Вирахувати за спектрами поглинання D D для цитохрому Р450;
2. Вирахувати за спектрами поглинання D D для цитохрому b5;
3. Вирахувати концентрацію білку в розчині, якщо відомо об¢єм білку відомої концентрації взятий для дослідження;
4. Розрахувати вміст цитохромів Р450 та b5 за спектрами поглинання, якщо відомо:
- концентрацію білку у розчині;
- коефіцієнт молярної екстинкції цитохрому Р450 (табличні дані);
- коефіцієнт молярної екстинкції цитохрому b5 (табличні дані).
5. Написати висновок.
Вимірювання вмісту цитохромів b5 та Р450 проводяться в суспензії мікросом, виділених з гомогенатів печінки щурів за допомогою 2-променевого спектрофотометра (див. мал.).
Визначення вмісту цитохрому b5 основано на величині поглинання відновленої форми (min при 409 нм та max при 428 нм):
ΔD для цит b5 = поглинання при 428нм – поглинання при 408нм
Вміст цитохрому b5 в мікросомальній фракції розраховували за допомогою коефіциєнта молярної екстинкції для цит. b5 =164. 103 см -1 . М -1.
Вміст цитохрому Р450 вимірюється величиною поглинання комплекса відновленого цитохрома з оксидом (СО) при 450 нм.
ΔD для цит Р450 = поглинання при 450нм – поглинання при 490 нм
Вміст цитохрому Р450 в мікросомальній фракції розраховували за допомогою коефіциєнта молярної екстинкції для цит. Р450 = 91. 103 см -1 . М -1.
Коефіцієнт молярної екстинкції або молярний коефіцієнт поглинання – це поглинання 1 М (одномолярного) розчину даної речовини або білку в кюветі товщиною 1 см.
Таблиця молярних коефіцієнтів поглинання деяких цитохромів
| Назва речовини | Довжина хвилі, нм | Молярний коефіцієнт поглинання, М-1 × см-1 |
| Цитохром с | 29,5 × 103 | |
| Цитохром Р420 | 110 × 103 | |
| Цитохром Р450 | 91 × 103 | |
| Цитохром b5 | 164 × 103 |
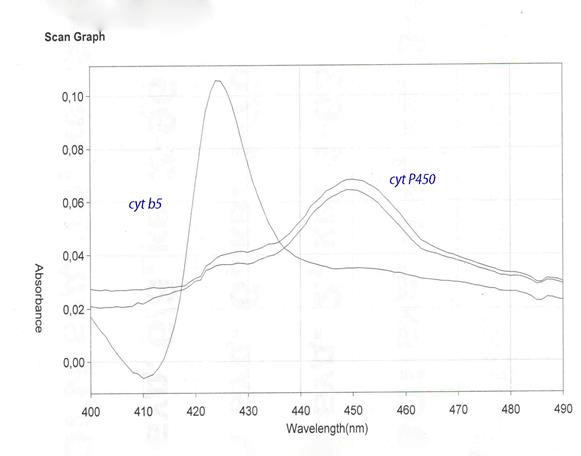
Рис. Спектр поглинання відновленого цитохрому b5 та відновленого цитохрому Р-450 у присутності СО
Присутність в білках іонів перехідних металів (у цитохромах b5 та Р450 це атом Fe2+) дозволяє застосувати широкий набір фізичних методів дослідження таких як спектроскопія.
Основне рівняння квантової теорії випромінення та поглинання виглядає так: DЕ = Е2 – Е1 = hn,
де Е1 та Е2 – енергія двох квантових рівнів, між якими здійснюється перехід;
h - стала Планка, постійна величина;
n - число довжин хвиль енергії, що випромінюється або поглинається.
За допомогою закону Ламберта-Бера можна встановити зв¢язок між поглинанням і природою білку, що поглинає. Згідно цього закону
I0
DD = lg ----- = e × c × l × концентрація загального білку, мг/мл (1)
I
де I0 - інтенсивність світового пучка, що падає на розчин білку;
I - інтенсивність світового пучка, що виходить після розчину білку;
e - молярний коефіцієнт поглинання, (М-1 × см-1), величина, що
приводиться в спеціальних таблицях;
c - концентрація білку, який поглинає світло, тобто концентрація
ферментного білку, моль/л;
l - товщина поглинаючого шару, см. Для спектрофотометра це
товщина кювети, в якій знаходиться розчин (l = 1 см).
З формули (1) визначаємо
D D
с = ----------------------------------------- = А мілімоль/мл, де
e × l × конц.заг.білку в мг/мл
DD = I – I0 поглинання білкового розчину, вимірюється спектрофотометром;
e - коефіциєнт молярної екстинкції для цит. b5 =164. 103 см -1 . М -1;
e - коефіциєнта молярної екстинкції для цит. Р450 = 91. 103 см -1 . М -1;
l = 1 см
1 М × см × мл мілімоль × мл
с = ------------------------------ = ---------------- = -------------------
М-1× см-1 ×см × мгбілку/мл см × мгбілку мл × мгбілку
|
|
|
|
|
Дата добавления: 2015-05-23; Просмотров: 442; Нарушение авторских прав?; Мы поможем в написании вашей работы!