
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
В мясных продуктах методом Фольгарда
|
|
|
|
Цель работы - определить содержание хлорид-ионов в мясном продукте, используя метод осаждения Фольгарда.
Сущность работы. К фильтрату водной вытяжки измельченного мясного продукта добавляют фиксированный объем нитрата серебра (AgNO3) в избытке по отношению к хлорид-ионам. Хлорид-ионы связываются в белый осадок ионами серебра по реакции:
CI - + Ag + ® AgCI¯.
Избыток нитрата серебра оттитровывают раствором KSCN с образованием белого осадка AgSCN согласно реакции:
SCN - + Ag + ® AgSCN¯.
В качестве индикатора используют раствор железоаммонийных квасцов, ионы Fe3+ которого образуют с ионами SCN- соединение красного цвета согласно реакции:
Fe 3+ + 6SCN - ® [Fe(SCN)6]3-.
Вначале при титровании полностью осаждается тиоцианат серебра, и только дополнительная капля KSCN идет на взаимодействие с индикатором, придавая раствору красноватый цвет.
Оборудование и реактивы: весы аналитические; мерная колба, вместимостью 200 см3; цилиндр, вместимостью 100 см3; водяная баня; цилиндры, вместимостью 10 см3(2 шт.); фильтровальная бумага; воронка; реактив Корреза I (106 г соли К4[Fe(CN)6] × 3H2O растворяют дистиллированной водой в мерной колбе, вместимостью 1 дм3, и доводят до метки); реактив Корреза II (200 г Zn(CH3COO)2 × 2H2O и 30 см3 ледяной уксусной кислоты переносят в мерную колбу, вместимостью 1 дм3, и доводят раствор дистиллированной водой до метки); раствор азотной кислоты, Сэк(HNO3) = 4 моль/дм3; раствор нитрата серебра, Сэк(AgNO3) = 0,1000 моль/дм3; насыщенный раствор железоаммонийных квасцов; нитробензол; раствор тиоцианата калия, Сэк(КSCN) = 0,1000 моль/дм3.
Методика выполнения анализа. 10 г измельченной пробы, взвешенной с точностью до 0,001 г, количественно переносят в мерную колбу, вместимостью 200 см3, добавляя небольшими порциями около 100 см3 горячей дистиллированной воды. Для полного экстрагирования хлорида натрия из пробы колбу выдерживают 15 минут на кипящей водяной бане, после чего охлаждают до комнатной температуры. Для осаждения белков в колбу последовательно добавляют 10 см3 реактива Карреза I и 10 см3 реактива Карреза II, встряхивая колбу после добавления каждого реактива. Доводят дистиллированной водой раствор до метки, тщательно перемешивают и фильтруют через складчатый бумажный фильтр. Пипеткой в мерную колбу переносят 20 см3 фильтрата, добавляют 5 см3 раствора азотной кислоты, 2 см3 насыщенного раствора железоаммонийных квасцов, 20 см3 раствора нитрата серебра и 3 см3 нитробензола (для коагуляции осадка). Содержимое колбы титруют раствором тиоцианата калия при энергичном перемешивании до появления не исчезающей красноватой окраски раствора. Титр раствора тиоцианата калия устанавливают по раствору нитрата серебра с тем же индикатором - железоаммонийными квасцами.
Содержание хлорида натрия (Х, %) вычисляют по формуле:
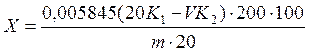 , (87)
, (87)
где 0,005845 - титр нитрата серебра по хлориду натрия, Т(AgNO3/NaCl), г/см3;
К1 - поправочный коэффициент концентрации раствора нитрата серебра к Сэк(AgNO3) = 0,1000 моль/дм3;
К2 - поправочный коэффициент концентрации раствора тиоцианата калия к Сэк(КSCN) = 0,1000 моль/дм3;
V - объем раствора KSCN, израсходованный на титрование, см3;
m - масса пробы, г.
|
|
|
|
|
Дата добавления: 2015-06-04; Просмотров: 621; Нарушение авторских прав?; Мы поможем в написании вашей работы!