
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
IV. Кислородные соединения углерода
|
|
|
|
| СO –угарный газ, ядовит, содержит тройную связь:С = О: слабо-полярная | |
· Углекислый газ СO2 как типичный кислотный оксид взаимодействует с щелочами (например, вызывает помутнение известковой воды), с основными оксидами и водой. Он не горит и не поддерживает горения и потому применяется для тушения пожаров. Однако магний продолжает гореть в углекислом газе с образованием оксида и выделением углерода в виде сажи:
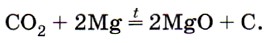
Угольная кислота и её соли
При растворении углекислого газа в воде образуется очень слабая угольная кислота Н2СО3.
Угольная кислота – слабая неустойчивая кислота, которую в свободном состоянии из водных растворов выделить нельзя.
Проявляет свойства слабых кислот. Будучи двухосновной, образует два типа солей карбонаты и гидрокарбонаты.
Свойства карбонатов
1. Карбонаты двухвалентных металлов трудно растворимы в воде, но их растворимость повышается в присутствии углекислого газа за счет образования гидрокарбонатов:
СаСО3 + СО2 + Н2О = Са(НСО3)2.
2. Карбонаты металлов (кроме щелочных металлов) при нагревании декарбоксилируются с образованием оксида:
CuCO3 = CuO + CO2.
карбонаты щелочных металлов не разлагаются.
3. Гидрокарбонаты разлагаются до карбонатов:
2NaHCO3 = Na2CO3 + H2O + CO2.
Качественной реакцией на карбонат и гидрокарбонат ионы является их взаимодействие с сильной кислотой, наблюдается образование углекислого газа с характерным вскипанием:
Na2CO3 + 2HCl = 2NaCl + H2O + CO2↑;
Кремний n=14 1s 2 2s 2 2p 6 3s 2 3p 2
Возможные степени окисления:
Si0 – 4e → Si+4
Восстановитель Si0 + 4e → Si-4Окислитель
Нахождение в природе SiO2 – кремнезем, составная часть песка Al2O3 ∙2 SiO2 ∙2 H2 O – каолинит – глина
Получение В лаборатории:SiO2 + 2 Mg = 2 MgO + Si
В промышленности: SiO2+2C = Si +
1) Кристаллический кремний –вещество серовато- стального цвета с металлическим блеском, полупроводник, электропроводность при нагревании повышается.
|
|
|
|
|
Дата добавления: 2015-08-31; Просмотров: 385; Нарушение авторских прав?; Мы поможем в написании вашей работы!