
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Физические теории 6 страница
|
|
|
|
-Q2=U1-U 2-A 2b1
Сложим эти уравнения: Q1-Q2=A1a2-A2b1=A. Здесь А – работа в цикле.
Блок - схема тепловой машины изображена на рис. 29. Всякая тепловая машина состоит из трех элементов:
1) горячего тела, его называют нагревателем, передающего рабочему телу за цикл Q 1 тепла;
2) рабочего тела, состояние которого циклически изменяется, в результате совершается механическая работа А;
3) холодного тела, его называют холодильником, которому рабочее тело отдает за цикл тепло Q2.
 Обратите внимание на принципиальную невозможность создать такую тепловую машину, которая бы превращала все полученное ею тепло в механическую работу и обладала бы 100% коэффициентом полезного действия. КПД тепловой машины h определяется как отношение полезной работы к затраченной энергии:
Обратите внимание на принципиальную невозможность создать такую тепловую машину, которая бы превращала все полученное ею тепло в механическую работу и обладала бы 100% коэффициентом полезного действия. КПД тепловой машины h определяется как отношение полезной работы к затраченной энергии:
h=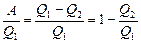 (6.4.1)
(6.4.1)
2. Холодильная машина забирает тепло у холодного тела и передает его горячему телу вместе с энергией, полученной извне для совершения работы. Рабочее тело при этом совершает цикл в обратном направлении: 1b2a1 (см. рис 28). Примером холодильной машины служит домашний холодильник. В нем рабочее тело забирает тепло из камеры холодильника, поддерживая в ней пониженную температуру, и отдает тепло в окружающую среду, нагревая ее. Для такой работы холодильник потребляет из сети электрическую энергию. Обратите внимание, что задняя стенка работающего холодильника нагревается. Примером холодильной машины является кондиционер, охлаждающий воздух в помещении. Холодильную машину, именуемую тепловым насосом, можно использовать для отапливания помещения. Тепловой насос забирает у наружного холодного воздуха внутреннюю энергию и передает ее в помещение. Разумеется, такой способ обогрева требует больших затрат энергии, поэтому традиционный способ обогрева зданий сжиганием топлива является более эффективным и экономичным.
§ 6.5. Цикл Карно
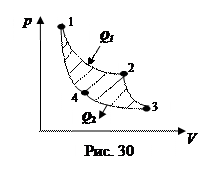 1. Французский инженер Карно в 1924 г. теоретически рассмотрел идеальный обратимый цикл, обеспечивающий максимальный КПД тепловой машины. Этот цикл и использующая его тепловая машина носят имя Карно. Нагреватель и холодильник имеют бесконечно большие теплоемкости. Это значит, что, сколько бы тепла ни забирали у нагревателя, и сколько бы тепла ни передавали холодильнику, их температуры не меняются. Температуры нагревателя и холодильника соответственно Т 1 и Т 2. Рабочим телом в цикле Карно является идеальный газ. На стадии расширения из состояния 1 в состояние 2 газ при температуре Т 1 изотермически получает от нагревателя тепло (рис.30), и это тепло идет на совершение работы:
1. Французский инженер Карно в 1924 г. теоретически рассмотрел идеальный обратимый цикл, обеспечивающий максимальный КПД тепловой машины. Этот цикл и использующая его тепловая машина носят имя Карно. Нагреватель и холодильник имеют бесконечно большие теплоемкости. Это значит, что, сколько бы тепла ни забирали у нагревателя, и сколько бы тепла ни передавали холодильнику, их температуры не меняются. Температуры нагревателя и холодильника соответственно Т 1 и Т 2. Рабочим телом в цикле Карно является идеальный газ. На стадии расширения из состояния 1 в состояние 2 газ при температуре Т 1 изотермически получает от нагревателя тепло (рис.30), и это тепло идет на совершение работы:
Q1= А 12= nRT 1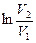 (6.5.1)
(6.5.1)
Перед сжатием температуру газа надо понизить. Для этого его подвергают адиабатическому расширению из состояния 2 в состояние 3, и он остывает до температуры холодильника Т 2. Потом газ изотермически сжимают до такого состояния 4, чтобы затем его путем адиабатического сжатия вернуть в исходное состояние 1 и завершить цикл. При сжатии газ совершает отрицательную работу - А 34 = А 43 и передает холодильнику тепло Q 2:
Q2= А 34= nRT 2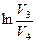 (6.5.2)
(6.5.2)
Уравнение адиабатного процесса (см. § 6.3) дает соотношения: T1V2g-1= T2V3g-1 и T1V1g-1 T2V4g-1, откуда получаем: 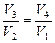 , соответственно,
, соответственно, 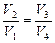 . Подставляя формулы (6.5.1) и (6.5.2) в формулу (6.4.1) и учитывая полученное соотношение объемов при изотермических процессах в цикле, получаем:
. Подставляя формулы (6.5.1) и (6.5.2) в формулу (6.4.1) и учитывая полученное соотношение объемов при изотермических процессах в цикле, получаем:
h=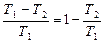 (6.5.3)
(6.5.3)
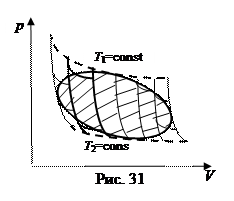
2. Любой обратимый цикл может быть представлен как сумма элементарных циклов Карно. На рис 31 овальной линией изображен такой цикл. Наибольшая температура в этом цикле Т 1, наименьшая Т 2. Через эти состояния проведены штриховыми линиями две изотермы цикла Карно, внутри которого помещается рассматриваемый цикл. Он разделен адиабатами на шесть частей. Эти адиабаты являются границами соответствующих циклов Карно (их площади заштрихованы), суммарная площадь которых приблизительно соответствует площади исходного цикла. Рассмотрим один из этих циклов, обозначенных жирной линией. Температура изотермического расширения в нем меньше Т 1, а температура изотермического сжатия больше, чем Т 2, и его КПД меньше, чем в цикле Карно с Т 1 и Т 2. Аналогичный вывод можно сделать относительно других элементарных циклов Карно. Следовательно, в любом обратимом цикле значение КПД меньше, чем рассчитанное по формуле (6.5.3), где Т 1 и Т 2 соответственно наибольшая и наименьшая температуры в цикле. Таким образом, цикл Карно обеспечивает наибольший КПД тепловой машины, работающей с заданными тепловыми резервуарами. Еще одним замечательным свойством формулы (6.5.3) является ее независимость от рабочего тела и от конструкции двигателя.
 3. Если тепловыми резервуарами машины Карно служат кипящая и замерзающая вода, то h=
3. Если тепловыми резервуарами машины Карно служат кипящая и замерзающая вода, то h=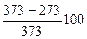 %= 27%. У реальной паровой машины КПД при тех же условиях значительно ниже теоретического значения. Это связано с необратимостью реальных тепловых процессов, потерями энергии на преодоление трения и непродуктивное нагревание окружающих тел. Повышение КПД лежит на пути увеличения температуры нагревателя. Заметим, что при горении бензина температура горячего резервуара может превышать 2000 К. Однако в любой реальной тепловой машине значительная часть энергии, полученной при сжигании топлива, возвращается холодильнику, роль которого нередко играет окружающая среда. Происходящий при этом нагрев называется тепловым загрязнением окружающей среды. В наши дни это явление стало серьезной экологической проблемой, волнующей не только ученых и политиков, но и так называемых «простых людей».
%= 27%. У реальной паровой машины КПД при тех же условиях значительно ниже теоретического значения. Это связано с необратимостью реальных тепловых процессов, потерями энергии на преодоление трения и непродуктивное нагревание окружающих тел. Повышение КПД лежит на пути увеличения температуры нагревателя. Заметим, что при горении бензина температура горячего резервуара может превышать 2000 К. Однако в любой реальной тепловой машине значительная часть энергии, полученной при сжигании топлива, возвращается холодильнику, роль которого нередко играет окружающая среда. Происходящий при этом нагрев называется тепловым загрязнением окружающей среды. В наши дни это явление стало серьезной экологической проблемой, волнующей не только ученых и политиков, но и так называемых «простых людей».
§ 6.6. Энтропия.
1. Энтропия (от греч. поворот, превращение) является функцией состояния термодинамической системы в том же смысле, что и внутренняя энергия. Это значит, что каждому состоянию термодинамической системы соответствует определенное значение энтропии. При переходе системы из одного состояния в другое изменение энтропии одинаково для любых процессов, связывающих эти два состояния, а в цикле изменение энтропии равно нулю. Рассмотрим цикл Карно. Его КПД может быть выражен так: h=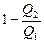
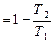 , откуда следует:
, откуда следует: 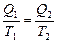 , и далее:
, и далее: 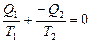 . Напомним, что тепло – алгебраическая величина. Q <0 означает, что у тела «забирают» тепло, т.е. оно получает отрицательное количество тепла. Количество тепла, изотермически сообщенное телу, деленное на температуру, называют приведенным количеством тепла. В цикле Карно приведенное количество тепла равно нулю. В предыдущем параграфе мы отмечали, что любой обратимый цикл можно рассматривать как сумму элементарных циклов Карно, следовательно, в любом обратимом цикле приведенное количество тепла равно нулю. При элементарном изменении состояния приведенное количество тепла выразится формулой:
. Напомним, что тепло – алгебраическая величина. Q <0 означает, что у тела «забирают» тепло, т.е. оно получает отрицательное количество тепла. Количество тепла, изотермически сообщенное телу, деленное на температуру, называют приведенным количеством тепла. В цикле Карно приведенное количество тепла равно нулю. В предыдущем параграфе мы отмечали, что любой обратимый цикл можно рассматривать как сумму элементарных циклов Карно, следовательно, в любом обратимом цикле приведенное количество тепла равно нулю. При элементарном изменении состояния приведенное количество тепла выразится формулой: 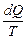 , и приведенное количество тепла в обратимом цикле[20]:
, и приведенное количество тепла в обратимом цикле[20]:
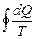 =0 (6.6.1)
=0 (6.6.1)
Полученная формула показывает, что термодинамическая система характеризуется некоторой функцией состояния, изменение которой равно приведенному количеству тепла. Эту функцию состояния называют энтропией и обозначают S. Ее изменение в элементарном процессе 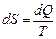 . При переходе из состояния 1 в состояние 2 изменение энтропии
. При переходе из состояния 1 в состояние 2 изменение энтропии
D S=S 2- S 1= (6.6.2)
(6.6.2)
Найдем формулу энтропии идеального газа. Подставим в формулу (6.6.2) формулу первого начала термодинамики для идеального газа:
D S=  =
=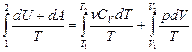 . Интегрирование с учетом уравнения состояния идеального газа
. Интегрирование с учетом уравнения состояния идеального газа 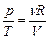 дает:
дает:
D S= (6.6.3)
(6.6.3)
Из (6.6.3) следует формула энтропии идеального газа:
S=S0 +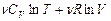 (6.6.4)
(6.6.4)
Здесь S0 – некоторая постоянная.
2. Выясним физический смысл энтропии. На примере идеального газа мы убедились, что энтропия в каждом состоянии тела имеет определенное значение, и, подобно энергии, является функцией состояния. Энергия характеризует способность тела совершать работу и может быть запасена в виде внутренней энергии термодинамической системы. Рассматривая цикл Карно, мы увидели, что внутренняя энергия нагревателя тем эффективнее превращается в работу, чем больше перепад температур нагревателя и холодильника. Если их температуры одинаковы, то КПД равен нулю, и внутренняя энергия не может работать. Напомним, что в равновесной термодинамической системе температура во всех ее областях одинакова. Следовательно, равновесная термодинамическая система может иметь большой запас внутренней энергии, но совершать механическую работу не может. Говорят, что энтропия – мера «обесцененности» внутренней энергии. Знание энтропии позволяет судить о том, можно ли внутреннюю энергию использовать для совершения работы. Мы уже отмечали, что работать может только неравновесная термодинамическая система. Таким образом, энтропия – мера приближения термодинамической системы к равновесию. Термодинамическое равновесие означает полнейшую идентичность друг другу разных участков системы, т.е. ее полную «хаотизацию», следовательно, энтропия – мера «хаотизации». Больцман, используя статистический метод, получил формулу энтропии в виде:
S=к lnW (6.6.5)
к – постоянная Больцмана, W – термодинамическая вероятность состояния системы, она равна числу микросостояний, каким может быть получено данное макросостояние. Поясним смысл этих
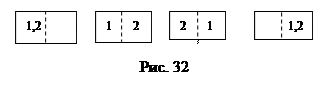
понятий на примере газа. Макроскопическое состояние газа определяют его параметры состояния: давление, объем, температура. Микроскопическое состояние определяется состоянием каждой его конкретной молекулы, т.е. ее положением в пространстве и скоростью. При тепловом движении молекул их состояния меняются хаотически, а состояние газа остается неизменным. Для примера рассмотрим сосуд, в котором содержатся 2 молекулы, каждая из которых может находиться в одной из половинок сосуда, т.е. каждая молекула имеет 2 микросостояния. Пронумеруем молекулы и распределим их в сосуде согласно возможностям хаотического движения. На рис. 32 показан сосуд и молекулы в нем в разных микросостояниях. Общее число микросостояний W, соответствующих данному макросостоянию – в сосуде содержится две молекулы - равно 4, т.е. W =22=4. Заметим, что в равновесном состоянии системы, когда молекулы равномерно распределены по объему, W= 2, а каждому неравновесному состоянию системы – обе молекулы собрались в правой или в левой половине сосуда – соответствует по одному микросостоянию. Добавляя по одной молекуле в сосуд и увеличивая их число до N, получим: W= 2N, причем, равновесному макросостоянию всегда соответствует наибольшее число возможных микросостояний. Мы получили еще один результат: состоянию термодинамического равновесия, когда система, обладая энергией, не может совершать работу, соответствует наибольшая термодинамическая вероятность, а вместе с ней и наибольшая энтропия. В состоянии термодинамического равновесия энтропия максимальна, и максимально «обесценена» внутренняя энергия.
§ 6.7. Второе начало термодинамики.
1. Из опыта мы знаем, что нагретые тела самопроизвольно остывают, а холодные, наоборот, самопроизвольно нагреваются, до температуры окружающей среды. При нагревании внутренняя энергия тела увеличивается, при охлаждении уменьшается. Если горячему телу сообщить дополнительную энергию, забрав соответствующее количество внутренней энергии у холодного тела, то температура горячего тела повысится, а холодного понизится. Такой процесс не противоречит первому началу термодинамики, в нем выполняется закон сохранения энергии. Но такие процессы самопроизвольно не происходят, они запрещены законом природы, который называется вторым началом (законом) термодинамики. Этот закон констатирует, что тепловые процессы в замкнутой системе идут только в определенном направлении, а именно, тепло самопроизвольно передается от горячего тела к холодному. С действием второго закона термодинамики мы постоянно встречаемся в повседневной жизни, примером являются нагретые батареи системы отопления.
2. Существуют другие математически эквивалентные формулировки второго начала термодинамики. Приведем некоторые из них.
· Никакая тепловая машина периодического действия не может иметь КПД, превышающий (Т 1 -Т 2)/ Т 1, где Т 1 и Т 2 – соответственно наибольшая и наименьшая температуры в цикле.
· Невозможен вечный двигатель второго рода.
· Энтропия замкнутой системы не может убывать: D S³ 0.
Первую из приведенных формулировок второго начала термодинамики мы уже обсудили в § 6.5.
Обсудим вторую формулировку. Вечным двигателем первого рода называется машина, которая производит работу без всякого внешнего источника энергии. Вечный двигатель первого рода имеет только рабочее тело, а нагреватель и холодильник в ней отсутствуют. Рабочее тело является замкнутой системой, и его состояние циклически изменяется. Такое устройство противоречит закону сохранения энергии. Невозможность создания вечного двигателя первого рода есть еще одна формулировка первого начала термодинамики. Вечный двигатель второго рода представляет собой циклически работающую машину, которая, получая тепло от внешнего источника энергии, целиком превращает его в механическую работу и имеет КПД 100%. У этой машины есть нагреватель и рабочее тело, но нет холодильника. Ранее мы уже убедились, что циклическое превращение тепла в механическую работу требует три обязательных тела: нагреватель, рабочее тело и холодильник.
Обсудим третью формулировку. Мы подошли к этому утверждению, рассматривая понятие энтропии в предыдущем параграфе. Действительно, если в замкнутой системе нет термодинамического равновесия, то вследствие теплового движения оно рано или поздно установится. Если замкнутая система уравновешена, то это ее состояние не может измениться без внешнего воздействия, а по определению замкнутой системы такого воздействия быть не может. Состоянию термодинамического равновесия соответствует наибольшая термодинамическая вероятность W и максимальное значение энтропии (см. формулу 6.6.5). Таким образом, если в результате предполагаемого процесса энтропия замкнутой системе уменьшится, то заведомо ясно, что такой процесс невозможен.
Тепловые процессы статистические, они происходят в результате хаотического, случайного движения частиц. Легко представить, что следствием случайностей может быть небольшое нарушение равновесия, например, в некоторый момент времени число частиц в одной половине сосуда может оказаться немного больше, или, наоборот, немного меньше, чем в другой. Такие самопроизвольные отклонения от положения равновесия называются флуктуациями. Понятно, что вероятность малых флуктуаций велика, а вероятность больших флуктуаций мала. При возникновении флуктуации нарушается термодинамическое равновесие, и энтропия уменьшается. Следовательно, в замкнутой системе возможны процессы, энтропия которых немного уменьшается. Учет статистического характера тепловых процессов отменяет категоричность ранее приведенной формулировки второго начала термодинамики. Ее более точная формулировка имеет вид: в замкнутой термодинамической системе наиболее вероятными являются такие процессы, в результате которых энтропия не уменьшается, т.е. D S³ 0.
3. Направленность тепловых процессов, о которой говорит второе начало термодинамики, связана с необратимостью реальных физических процессов. Чисто механические процессы, когда нет сил трения, обратимы. Например, выпущенный из рук мячик падает на пол, его потенциальная энергия превращается в кинетическую. После упругого удара мяч отскакивает и движется вверх, причем, обратный процесс складывается из последовательности тех же состояний, но проходимых в обратной последовательности, что и прямой путь. В процессе движения мяча происходит превращение механической энергии тела как целого из одного вида в другой, и это никак не отражается на внутреннем состоянии тела как совокупности частиц.
В термодинамических процессах участвует огромное число частиц, образующих тело. Принципиально необратимы процессы, в которых участвует большое число хаотически движущихся частиц: расширение газа в пустоту и теплопередача от горячего тела к холодному. Процесс расширения газа в пустоту выглядит так: одну половину сосуда, разделенного перегородкой на две части, заполним газом; после снятия перегородки молекулы необратимо разлетятся по всему сосуду. В § 6.2 мы отмечали, что при передаче тепла происходит передача энергии от «горячих» частиц к «холодным» путем непрерывного совершения микроскопической работы. Подобный механизм хаотического перераспределения энергии сопровождает действие силы трения. Работа этой силы приводит к уменьшению механической энергии тела: она превращается в тепло и перераспределяется между отдельными частицами тела, увеличивая «хаотизацию». Поясним рассмотренный механизм понятным примером из повседневной жизни. Если Вы дали деньги в долг своему надежному товарищу, то процесс обратим – деньги вернутся. Если же Вы вытащили из своего кармана некую сумму и бросили ее в толпу – процесс необратим. Во всех реальных процессах всегда присутствует рассмотренный механизм, и все реальные процессы необратимы, они приближают систему к положению равновесия. Полностью «хаотизированная», т.е. равновесная система неработоспособна. Вся наша разумная деятельность направлена на уменьшение «хаотизации» в локальной области незамкнутой системы.
Как показало развитие науки, Вселенная является незамкнутой системой, и гипотеза о «тепловой смерти Вселенной», возникшая в науке более века назад, несостоятельна. Суть этой гипотезы такова. В замкнутой системе самопроизвольно наступает полный хаос, и температура во всех ее частях и прочие термодинамические параметры выравниваются. Источником жизни на Земле является Солнце. Установление теплового равновесия во Вселенной означает возникновение всеобщего молекулярного хаоса и прекращение всякого направленного движения, которым является жизнь. Мы уже не раз отмечали, что все физические законы имеют определенную область применения. Незамкнутость термодинамической системы означает неприменимость к ней второго начала термодинамики.
§ 6.8. Основные выводы главы 6.
1. Термодинамические процессы и их законы используются в тепловых и холодильных машинах, без применения которых немыслима современная техника.
2. Термодинамический метод рассмотрения свойств любых тел, которые являются термодинамическими системами, широко применяется при изучении разных физических явлений и объектов.
3. Термодинамическая система является статистической, и механизм происходящих в ней явлений носит статистический характер.
Раздел 3. Электромагнетизм
Глава 7. Электростатика
§7.1.Электрический заряд. Закон Кулона.
В основе всего разнообразия явлений природы лежат четыре фундаментальных взаимодействия: сильное, электромагнитное, слабое и гравитационное. В механике мы уже упоминали, что гравитационное взаимодействие проявляет себя силой тяжести, а упругая сила и сила трения есть проявление электромагнитного взаимодействия. Каждый вид взаимодействия связан с определенной характеристикой частицы. Так, гравитационное взаимодействие связано с массой, а электромагнитное с электрическим зарядом частицы. Электрический заряд частицы является одной из основных, первичных ее характеристик. Перечислим фундаментальные свойства заряда:
1. Знак - существуют положительные и отрицательные заряды.
2. Квантование – заряд любой частицы (тела) равен целому числу элементарных зарядов; величина элементарного заряда в единицах СИ составляет 1,6.1019 Кл; электрон имеет элементарный отрицательный заряд, протон - элементарный положительный заряд.
3. Релятивистская инвариантность – величина заряда не зависит от скорости его движения и одинакова в любой инерциальной системе отсчета[21].
4. Закон сохранения заряда – в любой электрически изолированной (замкнутой) системе частиц алгебраическая сумма зарядов не изменяется.
5. Закон Кулона выражает силу взаимодействия двух точечный зарядов. 
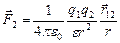
 (7.1.1)
(7.1.1)
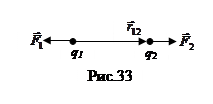 Точечным зарядом называется заряженная частица, к которой применима модель материальной точки. Рис. 33 иллюстрирует закон Кулона: показаны два точечных заряда на расстоянии и их силы взаимодействия.
Точечным зарядом называется заряженная частица, к которой применима модель материальной точки. Рис. 33 иллюстрирует закон Кулона: показаны два точечных заряда на расстоянии и их силы взаимодействия. 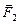 -вектор силы, действующей на второй заряд со стороны первого,
-вектор силы, действующей на второй заряд со стороны первого, 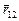 - вектор, проведенный из точки, где находится первый заряд, в точку, где находится второй заряд. Модуль этого вектора равен расстоянию между зарядами: r= ç
- вектор, проведенный из точки, где находится первый заряд, в точку, где находится второй заряд. Модуль этого вектора равен расстоянию между зарядами: r= ç 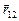 ç. Отметим, что закон Кулона, как и закон всемирного тяготения, утверждает, что сила взаимодействия обратно пропорциональна квадрату расстояния между частицами. Однако, гравитационное взаимодействие всегда есть притяжение масс, тогда как одноименные заряды отталкиваются, а разноименные притягиваются. Это отражено в формуле (7.1.1): произведение одноименных зарядов дает положительное число, и векторы
ç. Отметим, что закон Кулона, как и закон всемирного тяготения, утверждает, что сила взаимодействия обратно пропорциональна квадрату расстояния между частицами. Однако, гравитационное взаимодействие всегда есть притяжение масс, тогда как одноименные заряды отталкиваются, а разноименные притягиваются. Это отражено в формуле (7.1.1): произведение одноименных зарядов дает положительное число, и векторы 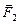 и
и 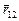 направлены одинаково, заряды отталкиваются. Произведение разноименных зарядов дает отрицательное число, в этом случае векторы
направлены одинаково, заряды отталкиваются. Произведение разноименных зарядов дает отрицательное число, в этом случае векторы 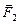 и
и 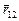 направлены противоположно друг другу, а заряды притягиваются. В соответствии с третьим законом Ньютона F1=F2=F. В скалярной форме закон Кулона имеет вид:
направлены противоположно друг другу, а заряды притягиваются. В соответствии с третьим законом Ньютона F1=F2=F. В скалярной форме закон Кулона имеет вид:
F=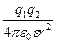 (7.1.2)
(7.1.2)
e0 – электрическая постоянная, зависит от выбора системы единиц, в СИ e0= 8,85.1012 Ф/м. e - безразмерная величина, диэлектрическая постоянная, индивидуальная характеристика свойств диэлектрика. Она показывает, во сколько раз сила взаимодействия зарядов в диэлектрике меньше, чем в вакууме, при прочих равных условиях. Позже мы выясним ее физический смысл. Отметим, что в воздухе e = 1.
§7.2. Электрическое поле. Напряженность.
1. Взаимодействие частиц на расстоянии в физике описывают с помощью особого вида материи – силового поля. Примером является гравитационное поле: оно создается частицей, имеющей массу, и действует на другую частицу, помещенную в гравитационное поле и обладающую массой. Аналогичным образом можно рассматривать взаимодействие частиц, обладающих зарядами. Заряд изменяет свойства окружающего его пространства, создавая в нем электрическое поле. Обнаруживает себя это поле силой, действующей на другой заряд. Рассмотрим закон Кулона (формула 7.1.1). Будем считать, что первый заряд создает поле, и это поле действует на второй заряд, причем, 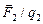 зависит только от источника поля, и от положения точки поля относительно источника, т.е. является силовой характеристикой поля. Можно сказать, что поле первого заряда бдительно следит за появлением «чужака», и, как только он где-либо в поле появится, тут же действует на него соответствующей силой. Этот способ описания взаимодействия зарядов абсолютно симметричен: можно считать, что второй заряд создает поле, а это поле действует силой на первый заряд. Силовая характеристика электрического поля называется напряженностью, обозначается
зависит только от источника поля, и от положения точки поля относительно источника, т.е. является силовой характеристикой поля. Можно сказать, что поле первого заряда бдительно следит за появлением «чужака», и, как только он где-либо в поле появится, тут же действует на него соответствующей силой. Этот способ описания взаимодействия зарядов абсолютно симметричен: можно считать, что второй заряд создает поле, а это поле действует силой на первый заряд. Силовая характеристика электрического поля называется напряженностью, обозначается 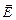 , в СИ измеряется в вольтах на метр (В/м). На посторонний заряд q поле действует силой
, в СИ измеряется в вольтах на метр (В/м). На посторонний заряд q поле действует силой
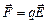 (7.2.1)
(7.2.1)
Поле, созданное неподвижными зарядами, называется электростатическим. Напряженность поля точечного заряда q в точке, заданной вектором 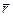 , проведенным из заряда (см. формулу 7.1.1):
, проведенным из заряда (см. формулу 7.1.1):
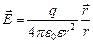 (7.2.2)
(7.2.2)
Вектор напряженности электростатического поля точечного заряда направлен вдоль прямой, соединяющей точку, где находится заряд, с данной точкой поля. Он выходит из точки поля и направлен от заряда, если он положительный, и к заряду, если он отрицательный. Величина напряженности
E=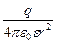 (7.2.3)
(7.2.3)
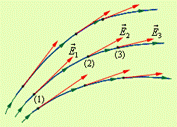
Пусть имеется система точечных зарядов qi (i= 1, 2, …). Поместим в некоторую точку системы, положение которой относительно каждого ее заряда указывает вектор 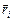 , посторонний заряд q. На него со стороны каждого заряда системы действует кулоновская сила. Их равнодействующая:
, посторонний заряд q. На него со стороны каждого заряда системы действует кулоновская сила. Их равнодействующая:
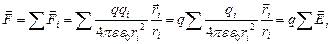 (7.2.4)
(7.2.4)
Полученный результат называется принципом суперпозиции (независимого сложения) электрического поля: если имеется несколько источников, то каждый из них создает свое поле независимо от всех прочих, и эти поля, складываясь, дают результирующее поле[22]. Формула принципа суперпозиции такова:
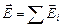 (7.2.5)
(7.2.5)
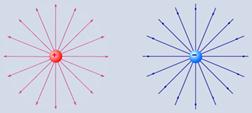
2. Поле известно, если известен вектор напряженности в каждой точке. Электрическое поле можно изображать графически векторами напряженности. Этот способ удобен для изображения поля в отдельных точках. Если поле надо нарисовать в некоторой области пространства, то используют линии напряженности (их называют еще силовыми линиями). Касательная к силовой линии указывает направление 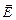 в данной точке поля, густота (плотность) силовых линий вблизи этой точки равна величине напряженности. Силовые линии электростатического поля выходят из положительного заряда и входят в отрицательный заряд.
в данной точке поля, густота (плотность) силовых линий вблизи этой точки равна величине напряженности. Силовые линии электростатического поля выходят из положительного заряда и входят в отрицательный заряд.
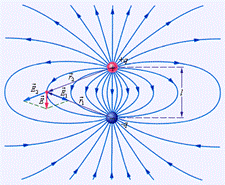
На рис. 34 показаны силовые линии поля положительного и отрицательного точечных зарядов, поля диполя, а также области некоторого электростатического поля - образующие его заряды находятся вне рассматриваемой области.
|
|
|
|
|
Дата добавления: 2014-01-06; Просмотров: 323; Нарушение авторских прав?; Мы поможем в написании вашей работы!