
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Тест тапсырмалары 3 страница
|
|
|
|
Егер V1 мл NaOH ерітіндісінің метилоранж қатысында кеткен көлемі, V2 мл – фенолфталеинмен кеткен көлемі болса (жалпы көлемі), онда (V2-V1) айырымы фосфор қышқылын екінші сатысында титрлеуге сәйкес болады. Осыдан:
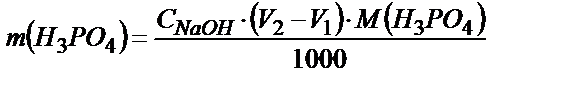
Н2SO4-ті титрлеуге V1-(V2-V1) =(2· V1- V2) мл сілті жұмсалады:
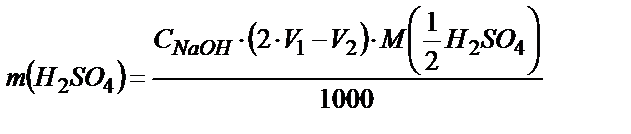
6.9.2. Судың кермектілігін анықтау
Қышқылдық-негіздік тікелей титрлеу әдісімен карбонатты, не жойылатын кермектілікті анықтауға болады. Карбонатты кермектілік (Ккарб) суда еріп жүрген кальций және магний гидрокарбонаттарымен анықталады. Суды қайнатқанда олар ыдырайды:
Ca(HCO3)2= CaCO3↓+ H2O+ CO2
Mg(HCO3)2= MgCO3↓+ H2O+ CO2
Сондықтан судың кермектілігі азаяды. Карбонатты кермектілікті суды метилоранж қатысында тұз қышқылымен титрлеп анықтайды:
Ca(HCO3)2+2 НCl= 2H2O+ 2CO2+ CaCl2
Судың кермектілігі 1 литр суда жүрген Са2+, Мg2+ тұздарының ммэкв. мөлшерімен анықталады – ммэкв/л. Егер 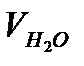 мл суды титрлеуге VHCl мл тұз қышқылы жұмсалса, онда судың карбонатты кермектілігі былай анықталады:
мл суды титрлеуге VHCl мл тұз қышқылы жұмсалса, онда судың карбонатты кермектілігі былай анықталады:
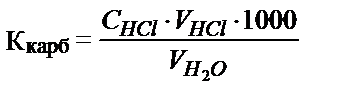
6.9.3. Аммоний тұздарын және органикалық қосылыстардағы азотты Кьелдал әдісімен анықтау
Аммоний ионы өте әлсіз қышқыл (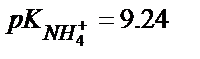 ),сондықтан оны тікелей титрлеу мүмкін емес. Аммоний тұздарын кері титрлеу жолымен анықтайды. Кері титрлеудің бір әдісінде анализдейтін ерітіндіге артық мөлшерде NaOH құйып, оны NH3 толық ұшып кеткенше қыздырады. Содан кейін артық қалған сілтіні метилоранж қатысында қышқылмен титрлейді. Сілті ерітіндісінің ауадағы СО2 – мен әрекеттесуі нәтижесінде индикатор ретінде фенолфталеинді алса, нәтиже дұрыс шықпауы мүмкін.
),сондықтан оны тікелей титрлеу мүмкін емес. Аммоний тұздарын кері титрлеу жолымен анықтайды. Кері титрлеудің бір әдісінде анализдейтін ерітіндіге артық мөлшерде NaOH құйып, оны NH3 толық ұшып кеткенше қыздырады. Содан кейін артық қалған сілтіні метилоранж қатысында қышқылмен титрлейді. Сілті ерітіндісінің ауадағы СО2 – мен әрекеттесуі нәтижесінде индикатор ретінде фенолфталеинді алса, нәтиже дұрыс шықпауы мүмкін. 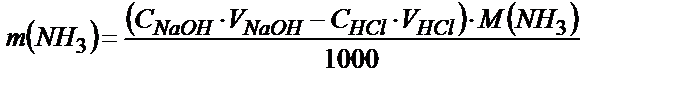
Кері титрлеудің екінші жолында анализдейтін аммоний тұзының ерітіндісіне артық мөлшерде сілті құйылады, бөлініп шыққан NH3 титрі белгілі артық алынған қышқылмен сіңіріледі. Аммиакпен әрекеттескеннен кейінгі артық қалған қышқылдың мөлшерін метилоранж қатысында сілтімен титрлейді. Бұл жағдайда да фенолфталеинді, не рТ>7 индикаторларды пайдалануға болмайды, себебі реакцияға ерітіндіде жүрген аммоний иондары қатысуы мүмкін. Анализдің нәтижесін кері титрлеу формуласымен есептейді:
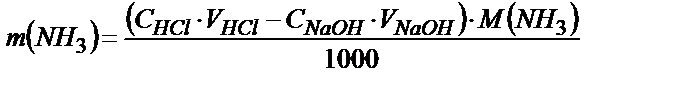
Аммиакты айдау әдісі органикалық заттардағы азотты кең тараған Кьелдаль әдісімен анықтауға пайдаланылады. Бұл әдістің ең қарапайым түрі – анализдейтін органикалық заттарды сынап тұздары қатысында (катализатор) концентрлі күкірт қышқылымен өңдеу, нәтижесінде органикалық қосылыстар СО2 және H2O-ға дейін тотығады, ал азот NH4HSO4 –ке ауысады. Пайда болған аммоний тұзын кері титрлеу әдістерінің бірін пайдаланып анықтайды.
Аммоний иондарын анықтаудың тағы бір жолы аммоний ионының формальдегидпен әрекеттесуіне негізделген:
4NH4Cl+6CH2O=(CH2)6N4+4HCl+6 H2O
Бұл реакция орын басу реакциясына жатады. Пайда болған гексаметилентетраамин не уротропин әлсіз негіз (рК=5,0), сонымен қатар реакцияның нәтижесінде алынған NH+4 иондарына эквивалентті сутек иондары бөлінеді. Бөлініп шыққан қышқылды фенолфталеин қатысында сілтінің ерітіндісімен титрлейді:
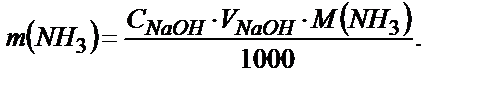
Бақылау сұрақтары мен жаттығулар
1. 500,0 мл ерітіндіде 2,6580 г Na2СO3 бар. Осы ерітіндіні а) СО2 – ге дейін; б) NaНСO3-ке дейін бейтараптағандағы 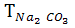 ,
,  мәндерін есептеңдер.
мәндерін есептеңдер.
2. 1,0 л 0,100 М НCl ерітіндісін дайындау үшін 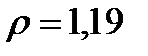 г/мл сәйкес тұз қышқылының қандай көлемін алу керек?
г/мл сәйкес тұз қышқылының қандай көлемін алу керек?
3. 0,4217 г бураны титрлеуге 17,50 мл НCl жұмсалды. Осы қышқылдың эквивалентінің молярлы концентрациясын және титрін есептеңдер.
4. Күкірт қышқылы эквивалентінің молярлы концентрациясын анықтау үшін оның 10,00 мл – не ВаCl2-нің артық мөлшері қосылған. Тұнбаны сүзіп, қыздырып өлшегеннен кейін оның массасы 0,2762 г болды. Осы қышқылдың С(fэ) және Т мәндерін анықтаңдар.
5. 0,6000 г Н2С2О4·2Н2О 100,0 мл өлшем колбасында ерітілді. Осы ерітіндінің С(fэ) мәнін және Н2С2О4 арқылы титрін табыңдар.
6. Құрамында 92,00 % NaOH және 8,00 % қоспасы бар 0,5341 г сілті 100,0 мл өлшем колбасында ерітілді. Егер осы ерітіндінің 15,00 мл титрлеуге 19,50 мл тұз қышқылы кетсе, осы қышқылдың С(fэ) және ТНCl/NaOH мәндері неге сәйкес?
7. 15,00 мл КОН ерітіндісін титрлеуге 18,70мл НСІ кеткен (ТНСІ=0,002864 г/мл). КОН ерітіндісі эквивалентінің молярлы концентрациясы неге тең?
8. Егер ерітіндінің 20,00 мл аликвотын титрлеуге 14,70 мл НСІ (ТНСІ=0,003800 г/мл) жұмсалуы қажет болса, құрамында 1,5320 г NaOH бар ерітіндіні қандай көлемге дейін сұйылту керек?
9. 20,00 мл азот қышқылын титрлеуге 21,12 мл 0,112 М NaOH жұмсалады. Ерітіндінің 1,0 л –де неше грамм N2O5 бар?
10. Қымыздық қышқылының 0,1372 г еріген ерітіндіні титрлеуге 22,10 мл 0,0980 М NaOH кетті. Алғашқы қышқылдың құрамында кристалдық судың неше молекуласы бар?
11. Титрлеуге 20,00 мл 0,100 М NaOH жұмсалуы үшін ерітіндідегі Н2С2О4 · 2Н2О массасы неге сәйкес болуы керек?
12. Метилоранж индикаторы қатысында титрлеуге 20,00 мл 0,100 М НСІ ерітіндісі жұмсалу үшін құрамыда 90,0 % Na2CO3 бар заттың қандай массасын алу керек?
13. 0,0997 г NaOH еріген ерітіндіні титрлеуге 22,00 мл НСІ ерітіндісі жұмсалды. Осы ерітіндінің Na2O арқылы титрін табыңдар.
14. Фосфор қышқылыың 2,6040 г ерітіндісі (р=1,68 г/мл) 250,0 мл өлшем колбасында сумен сұйытылды. Алынған ерітіндінің 20,00 мл метилоранж қатысында титрлеуге 18,00 мл NaOH кетті. NaOH ерітіндісі эквивалентінің молярлы концентрациясын анықтаңдар.
15. Фенолфталеин қатысында титрлеуге 20,00 мл 0,100 М KOH жұмсалуы үшін KH2PO4 тұзының қандай массасын алу керек?
16. 0,1182 г фосфор қышқылының судағы ерітіндісін фенолфталеин қатысында титрлеуге 22,18 мл 0,100 М NaOH жұмсалды. Фосфор қышқылының P2O5-ке есептегендегі массалық үлесін(%) табыңдар.
17. 3,1580 г техникалық КОН еріген ерітіндіні титрлеуге 27,45 мл НСІ (ТНСІ/NaOH=0,07862 г/мл) жұмсалды. Үлгідегі КОН-тың массалық үлесін (%) есептеңдер.
18. Егер 1,2000 г олеумді метилоранж қатысында титрлеуге 49,25 мл 0,520 М NaOH жұмсалса, бос SO3 –тің олеумдегі массалық үлесі (%) қанша болғаны?
19. Колчеданның 1,4000 г нақты мөлшерін күйдіргенде бөлінген газ Н2О2 ерітіндісімен сіңірілді. Пайда болған күкірт қышқылын титрлеуге 24,86 мл 0,150 М NaOH жұмсалды. Күкіртің колчедандағы массалық үлесін(%) есептеңдер.
20. Белгісіз заттың 2,0000 г өлшендісі 100,0 мл өлшем колбасында ерітілді. Осы ерітіндінің 25,00 мл титрлеуге 20,00 мл 0,445 М HCI жұмсалды. Анализденген заттың құрамында NaOH әлде КОН бар ма?
21. Құрамында Na2CO3, NaHCO3, NaCI бар 0,4478 г қоспа ерітіндісін фенолфталеин қатысында титрлегенде 18,80 мл 0,199 М HCI ерітіндісі жұмсалды. Тағы да 0,4478 г осы қоспа еріген ерітіндіні метилоранж қатысында титрлеуге 40,00 мл НСІ кетті. Қоспадағы Na2CO3 және NaHCO3-тің массалық үлесін есептеңдер.
22. 5,00 мл тұз және фосфор қышқылдарының қоспасы 200,0 мл-ге дейін сұйытылған. Алынған ерітіндінің 20,00 мл метилоранж қатысында титрлеуге 18,20 мл 0,101 М NaOH кетті. Осындай 20,00 мл ерітіндіні фенолфталеин қатысында титрлеуге 37,40 мл NaOH ерітіндісі жұмсалды. 100,0 мл қоспадағы НСІ мен Н3РО4-тің массасын анықтаңдар.
23. NO3- -ионын тотықсыздандырғанда бөлінген аммиакты титрлеуге 40,00 мл 0,100 М NaOH жұмсалуы үшін алғашқы NaNO3 массасы қандай болу керек?
24. 1,0000 г аммоний тұзы концентрлі NaOH ерітіндісімен өңделді. Бөлінген аммиак 50,00 мл 1,072 М HCI ерітіндісінен өткізіліп, артық қалған қышқылды титрлеуге 24,50 мл NaOH (ТNaOH=0,004120 г/мл) ерітіндісі жұмсалды. Үлгідегі NH3 –тің массалық үлесін (%) табыңдар.
25. Қышқылдың артық мөлшерін метилоранж қатысында титрлеуге 19,50 мл NaOH (TNaOH/CaO=0,002910 г/мл) ерітіндісін жұмсау үшін мссасы 0,1234 г таза –СаСО3 -ті тұз қышқылының (ТHCI=0,003638 г/мл) қандай көлемінде еріту керек?
26. 0,015 М НСІ мен 0,005 М NaOH ерітінділерінің рН неге тең?
27. 0,003 М сірке қышқыл ерітіндісінің рН 3,61-ге тең. Осы қышқылдың протонизациялану константасы қандай?
28. 0,010 М құмырсқа қышқылының (КНСООН =1,8·10-4) рН неге тең?
29. 0,01 М аммиактың судағы ерітіндісінің(К=1,76·10-5) рН неге тең?
30. 0,010 М CH3COOH және 0,100 М CH3COONa ерітінділері қоспасының рН неге тең?
31. 0,200 М NH3 · H2O және 0,020 М NH4CI ерітінділері қоспасының рН неге тең?
32. 0,010 М NH4CI ерітіндісінің қышқылдық константасы мен рН неге тең?
33. 20,0 мл 0,100 М НСІ ерітіндісіне 30,00 мл 0,100 М NaOH құйылды, алынған ерітіндінің рН-ы неге тең?
34. 25,00мл 0,200 М СН3СООН ерітіндісіне: 1) 24,00мл: 2) 25,10 мл 0,200 М NaOH құйылды. Алынған ерітінділердің рН неге тең?
35. 0,2000 М КОН ерітіндісін 0,0200 М HNO3 ерітіндісінен титрлеу қисығын қорытып шығарыңдар және эквивалентті нүктені анықтауға сәйкес индикаторларды таңдап алыңдар.
36. 0,100 М құмырсқа қышқылын 0,100 М КОН ерітіндісімен титрлеу қисығын қорытып шығарыңдар және титрлеуге сәйкес индикаторды таңдап алыңдар.
37. 0,500 М NH3·H2O ерітіндісін 0,500 М HCI ерітіндісімен титрлеу қисығын қорытып шығарыңдар және титрлеуге сәйкес индикатор таңдап алыңдар.
38. Келтірілген титрлеулердің қайсысының эквивалентті нүктедегі рН=7, рН>7, рН<7 сәйкес?: 1) HNO3+NaOH; 2) HCOOH+NaOH; 3) NH3+HCI; 4) KOH+HCI; 5) CH3CH2COOH+KOH; 6) Na2CO3+HCI.
39. Фосфор қышқылын NaOH ерітіндісімен а) метилоранж, б) фенолфталеин қатысында титрлегенде пайда болатын буферлі қоспалардың құрамын көрсетіңіздер.
40. 1) K2CO3 және KHCO3; 2) NaOH және Na2CO3; 3) H3PO4 және Ca(H2PO4)2; 4) H3PO4 және HCI бірге жүргенде олардың мөлшерін қалай анықтауға болады? Есептеу теңдіктерін келтіріңдер.
41. Үш негізді қышқылдың Н3А протолиздену константалары K1= 1·10-2; K2=1·10-6; K3=1·10-12. Осы қышқылды NaOH ерітіндісімен титрлегендегі бірінші және екінші эквивалентті нүктелерге сәйкес рН-ты есептеп шығарыңдар, қандай индикаторлар пайдаланасыздар? Қышқылды үшінші эквивалентті нүктесіне дейін титрлеуге бола ма? Үшінші э.н. сәйкес ( 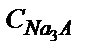 =0,10 M) pH мәні неге тең?
=0,10 M) pH мәні неге тең?
42. Титрлеудің индикаторлық қатесі деген не? Титрлеудің индикаторлық қателерінің түрлерін келтіріңіздер.
43. 0,100 М НСІ ерітіндісін 0,100 М NaOH ерітіндісімен 1) метилоранж (рТ= 4); 2) метилді қызыл(рТ= 5,5); 3) фенолфталеин (рТ = 9) қатысында титрлегенде индикаторлық қателер неге тең?
44. 0,010 М тұз қышқылын 0,010 М NaOH ерітіндісімен метилоранж қатысында титрлеуге бола ма?
45. 0,100 М сірке қышқылын 0,100 М NaOH ерітіндісімен 1) метилоранж, 2) фенолфталеин қатысында титрлеудің индикаторлық қателерін есептеңдер.
46. 0,100 М аммиактың ерітіндісін 0,100 М тұз қышқылымен 1) фенолфталеин; 2) метилоранж қатысында титрлеудің индикаторлық қателерін есептеңдер.
47. 0,100 М NaOH ерітіндісін құмырсқа қышқылымен бейтарап қызыл индикаторы (рТ =7) қатысында титрлеудің индикаторлық қатесін есептеңдер.
1. Төменде келтірілген титрлеулер қатарының қайсысының эквиваленттік нүктесі рН=7 мәніне сәйкес келеді?
1) HNO3 + NaOH, CH3COOH + NaOH, HCl + NH3;
2) Na2CO3 + HCl, KCN + HCl, Na2B4O7 + HCl;
3) HNO3 + NaOH, HCl + KOH, HClO4 + NaOH;
4) CH3COOH + KOH, HCOOH + NaOH, H2CO3 + KOH;
5) NH3 + HCl, NH3 + HNO3, KOH + HCl.
2. Төменде келтірілген титрлеулер қатарының қайсысының эквиваленттік нүктесі рН<7 мәндер аймағында жатады?
1) HNO3 + NaOH, CH3COOH + NaOH, HCl + NH3;
2) NH3 + HCl, Na2B4O7 + HCl; NaHCO3 + HCl;
3) CH3COOH + KOH, HCl + KOH, NH3 + HNO3;
4) HNO3 + KOH, HCl + KOH, HCOOH + NaOH;
5) KOH + HNO3, HClO4 + NH3, CH3COOH + KOH.
3. Төменде келтірілген титрлеулер қатарының қайсысының эквиваленттік нүктесі рН>7 мәндер аймағында жатады?
1) NH3 + HCl, KOH + HCl, CH3COOH + NaOH;
2) KCN + HCl, Na2B4O7 + HCl; HCOOH + NaOH;
3) CH3COOH + NaOH, HCOOH + NaOH, H2CO3 + KOH;
4) KOH + HCl, CH3COOH + KOH, Na2CO3 + HCl;
5) NH3 + HCl, HNO3 + NaOH, CH3COOH + NaOH.
4. Қышқыл-негіздік титрлеу әдісінде титрлеу қисығы деп нені айтады?
1) рН мәнінің құйылған титрант көлеміне тәуелділігін көрсететін қисық;
2) СН+ мәнінің Ститрант мәніне тәуелділігін көрсететін қисық;
3) Сқышқыл мәнінің Снегіз мәніне тәуелділігін көрсететін қисық;
4) Сқышқыл мәнінің негіздің көлеміне тәуелділігін көрсететін қисық;
5) рН мәнінің Ститрант мәніне тәуелділігін көрсететін қисық.
5. Индикатордың диссоциациялану константасы мен оның түсі ауысу аралығында қандай байланыс бар?
1) ∆рН = К 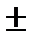 1;
1;
2) ∆рН = рК 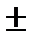 1;
1;
3) 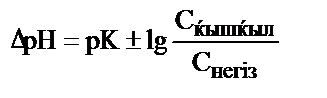 ;
;
4) 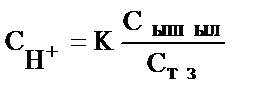 ;
;
5) 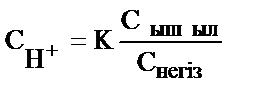 .
.
6. KOH-тың титрленген ерітіндісін оның дәл өлшендісінен дайындауға бола ма?
1) болады;
2) болмайды, себебі, КОН-ты қоспалардан тазарту мүмкін емес;
3) болмайды, себебі КОН өте гигроскопты және ол ауадағы көмірқышқыл газымен байланысады;
4) болады, КОН-ты жабық бюксте өлшеу арқылы;
5) болады, қайта кристалданған КОН-ты қолдану арқылы.
7. Қышқыл-негіздік титрлеуде индикаторды қалай дұрыс таңдап алу керек?
1) индикатордың түсі ауысу аралығының жоғарғы немесе төменгі шектері титрлеу қисығының күрт өзгеруі ішінде жатуы керек;
2) индикатордың түсі ауысу аралығы титрлеу қисығының күрт өзгеруі шамасына тең болуы керек;
3) индикатордың түсі ауысу аралығы титрлеу қисығының күрт өзгеруіне байланысты емес;
4) индикатордың түсі ауысу аралығының төменгі шегі титрлеу қисығының күрт өзгеруі ішінде жатуы керек;
5) барлық жауаптар дұрыс.
8. Қайсы жауап күшті қышқылды күшті негізбен титрлеуді дұрыс сипаттайды?
1) эквивалентті нүктеге дейін рН келесі формула бойынша есептелінеді:
2) pH = -lgCышыл ;
3) титрлеу кезінде рН төмендейді және эквивалентті нүктеде минимальды мәнге ие болады;
4) титрлеу барысында рН түзу сызықты түрде өзгереді және эквивалентті нүктеде 9-ға тең болады;
5) титрлеу барысында рН түзу сызықты түрде артады;
6) титрлеу барысында рН өзгермейді.
9. Қайсы жауап әлсіз қышқылды күшті негізбен титрлеуді дұрыс сипаттайды?
1) эквивалентті нүктеде рН=7;
2) эквивалентті нүктеге дейін рН мына формула рН= -lgCқыш. бойынша есептелінеді;
3) эквивалентті нүктеге дейін рН мына формула бойынша есептелінеді: 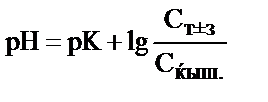 ;
;
4) титрлеу барысында рН түзу сызықты түрде өседі;
5) барлық жауаптар дұрыс.
10. Күшті негізбен бейтараптауда қайсы қышқылдың титрлеу қисығында рН-тың күрт өзгеруі ең үлкен шамаға ие болады?
1) CH3COOH (K=10-5); 2) H3BO3 (K=6.0-10); 3) HCOOH (K=10-4);
4) HCN (K=7.10-10); 5) HF (K=6,8.10-4).
11. 50 мл 0,1н. NH3 ерітіндісіне 25 мл 0,1н. НСІ ерітіндісі қосылған. Алынған ерітіндінің рН-ын қайсы теңдеумен есептеу қажет?
1) 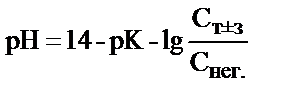 ; 2)
; 2) 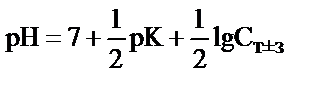 ;
;
3) 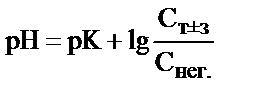 ; 4)
; 4) 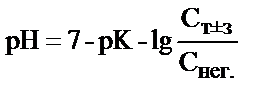 ;
;
5) pH = -lgCHCl.
12. 50,0 мл 0,1н. сірке қышқылы ерітіндісіне 25,0 мл 0,1н. күйдіргіш натрий ерітіндісі қосылған. Алынған ерітіндінің рН-ын қайсы теңдеумен есептеуге болады?
1) 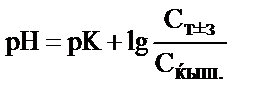 ; 2)
; 2) 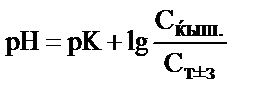 ; 3) pH = 7+
; 3) pH = 7+ 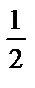 pK;
pK;
4) pH = -lgCқыш.; 5) pH = -lgCтұз.
13. 0,1н. Na2CO3 ерітіндісін 0,1н. НСІ ерітіндісімен 1-сатысы бойынша титрлегенде эквивалентті нүктедегі рН мәнін қайсы теңдеу бойынша есептеуге болады?
1)  2) pH = 7+
2) pH = 7+ 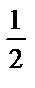 pK2 +
pK2 + 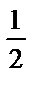 lgCтұз;
lgCтұз;
3) pH = -7- 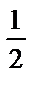 lgK2.Cтұз; 4) pH = 7+
lgK2.Cтұз; 4) pH = 7+ 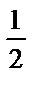 pK2 +
pK2 + 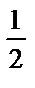 lgCтұз;
lgCтұз;
5) pH = 7- 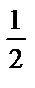 (lgK2 -lgCтұз).
(lgK2 -lgCтұз).
14. Егер химиялық таза екі негізді янтарь қышқылының 0,1180 г өлшендісі еріген ерітіндіні титрлеуге 10,00 мл KOH ерітіндісі жұмсалса, оның (КОН) эквивалентінің молярлы концентрациясы (нормальдығы) қандай болғаны? (MH6C4O4= 118 г/моль).
1) 0,01; 2) 0,10; 3) 0,02; 4) 0,20; 5) 0,05.
15.Қандай жағдайда эквивалентті нүктедегі рН шамасы 7-ден кіші болады?
1) күшті қышқылды күшті негізбен титрлегенде;
2) әлсіз қышқылды күшті негізбен титрлегенде;
3) әлсіз негізді күшті қышқылмен титрлегенде;
4) күшті негізді күшті қышқылмен титрлегенде;
5) дұрыс жауабы жоқ.
16. Метилді-қызғылт индикаторы қатысында Na2CO3 және NaOH қоспасы HCl ерітіндісімен титрленген. Бұндай жағдайда қоспа қалай титрленеді?
1) NaOH + Na2CO3 жартысы;
2) NaOH;
3) NaOH + Na2CO3;
4) Na2CO3;
5) Na2CO3 жартысы.
17. Әлсіз қышқылды күшті негізбен титрлеу қисығының эквивалентті нүктеден кейінгі өзгерісі қандай факторға тәуелді?
1) қышқылдың концентрациясына;
2) негіздің концентрациясына;
3) қышқылдың табиғатына;
4) қышқылдың күшіне;
5) дұрыс жауап келтірілмеген.
18. Индикатордың екі түрінің концентрацияларының қандай қатынасында оның қышқылдық түрінің түсін байқауға болады?
1) 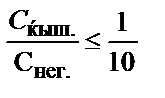 ; 2)
; 2) 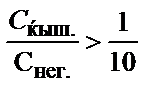 ; 3)
; 3)  ;
;
4) 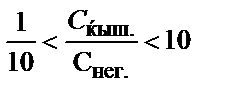 ; 5)
; 5) 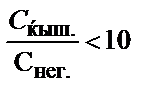 .
.
19. Индикатордың екі түрі концентрацияларының қандай қатынасында оның негіздік түрінің түсін байқауға болады?
1) 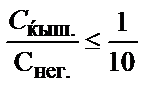 ; 2)
; 2)  ; 3)
; 3) 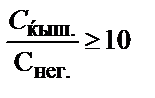 ;
;
4) 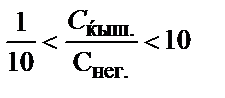 ; 5)
; 5) 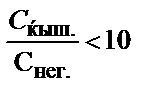 .
.
20. Әлсіз негізді (Kb=10-4) күшті қышқылмен рТ=5 индикатор қатысында титрлегенде титрлеу қателігі немен анықталады?
1) индикатордың рТ шамасының бейтараптау нүктесіне сәйкес келмеуімен;
2) индикатордың рТ мәнінің «тұзды эффект» нәтижесінде өзгеруімен;
3) индикатордың рТ мәнінің эквивалентті нүктедегі рН мәніне сәйкес келмеуімен;
4) индикатордың түсі ауысу аралығы мен титрлеу қисығының күрт өзгеру шамасының сәйкес келмеуімен;
5) дұрыс жауап келтірілмеген.
|
|
|
|
|
Дата добавления: 2014-11-25; Просмотров: 1447; Нарушение авторских прав?; Мы поможем в написании вашей работы!