
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Порядок выполнения работы. Капиллярный вискозиметр Освальда (см
|
|
|
|
Описание прибора
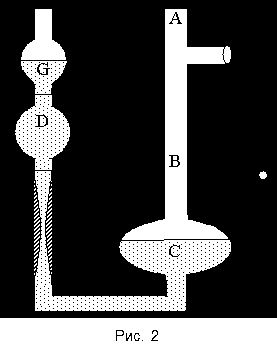
Капиллярный вискозиметр Освальда (см. рис. 2 на следующей стр.) представляет собой U-образную стеклянную трубку, широкое колено АВ которой заканчивается внизу расширением С. Другое колено KDG состоит из капилляра К, заканчивающегося наверху расширениями D и G.
На короткую трубку В надета резиновая трубка Е с грушей F. Через отверстие А с помощью воронки в широкое колено наливается определенный объем исследуемой жидкости до уровня b. Затем, закрыв пальцем отверстие А, сжимают резиновую грушу F и перегоняют жидкость из расширения С в расширение D и G. Как только некоторая часть жидкости оказывается в расширении G, перегонку жидкости заканчивают. Далее наблюдают перетекание жидкости через капилляр К из левого колена в правое. В тот момент, когда мениск проходит через метку т, включают секундомер, а в момент прохождения метки n останавливают секундомер.
1. Наливают в вискозиметр определенный объем воды и три раза измеряют время 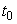 ее
ее
протекания через капилляр вискозиметра. Находят 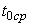 .
.
2. Используя табличное значение 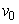 для воды при той температуре воздуха, которая есть в данный момент в лаборатории, вычисляют постоянную прибора
для воды при той температуре воздуха, которая есть в данный момент в лаборатории, вычисляют постоянную прибора  .
.
3. Выливают воду из вискозиметра, поочередно заливают в него растворы спирта различной концентрации С и определяют время  их протекания.
их протекания.
4. По формуле  определяют значение кинематической вязкости каждого раствора.
определяют значение кинематической вязкости каждого раствора.
5. Строят график 
17. Термодинамическая система — выделяемая (реально или мысленно) для изучения макроскопическая физическая система, состоящая из большого числа частиц и не требующая для своего описания привлечения микроскопических характеристик отдельных частиц[1], «часть Вселенной, которую мы выделяем для исследования»[2]. Единицей измерения числа частиц в термодинамической системе обычно служит число Авогадро[3]. Ограничения на природу материальных частиц, образующих термодинамическую систему, не накладываются: это могут быть атомы, молекулы, электроны, ионы, фотоны и т. д.[4], [5]. Любой объект, видимый невооружённым глазом или с помощью оптических приборов (микроскопы, телескопы и т. п.), можно отнести к термодинамическим системам: «Термодинамика занимается изучением макроскопических систем, пространственные размеры которых и время существования достаточны для проведения нормальных процессов измерения»[4].
Любую часть термодинамической системы называют подсистемой.
Для описания термодинамической системы используются макроскопические параметры, характеризующие не свойства составляющих её частиц, а свойства самой системы: температуру, давление, магнитную индукцию, электрическую поляризацию, массу и химический состав компонентов и др.[6], [7].
Каждая термодинамическая система имеет границы, реальные или условные, отделяющие её от окружающей среды[8]. Иногда вместо окружающей среды говорят о термостате[4].
Термодинамические системы служат предметом изучения термодинамики, статистической физики и физики сплошных сред.
Классификация термодинамических систем
По характеру взаимодействия с окружающей средой различают системы[8]:
· изолированные, не обменивающиеся с внешней средой ни энергией, ни веществом;
· адиабатически изолированные, не обменивающиеся с внешней средой веществом, но допускающие обмен энергией в виде работы[9];
· закрытые, обменивающиеся с внешней средой энергией, но не обмениваются веществом;
· открытые, обменивающиеся с внешней средой и энергией, и веществом.
Реальную изоляцию термодинамической системы от окружающей среды осуществляют посредством стенок (поверхностей раздела, перегородок, оболочек)[10]: подвижных и неподвижных, проницаемых и непроницаемых для вещества (существуют и полупроницаемые перегородки). Сосуд Дьюара служит хорошим примером адиабатической оболочки. Перегородка, не препятствующая обмену энергией, называется диатермической.
Термодинамическую систему называют гомогенной, если её свойства непрерывно изменяется от точки к точке[11]. Гомогенную систему с одинаковыми свойствами в любой точке называют однородной [11]. Примерами гомогенных систем служат растворы (газовые, жидкие и твердые). Газовая фаза большой протяженности вдоль градиента поля тяготения (например, земная атмосфера в безоблачный и безветренный день) — пример неоднородной гомогенной фазы (см. Барометрическая формула).
Термодинамическую систему называют гетерогенной, если она состоит из нескольких гомогенных частей с разными свойствами. На поверхностях, разделяющих гомогенные части гетерогенной системы, свойства системы меняются скачком[12]. Часто (но не всегда) эта поверхность является видимой.
Гомогенную часть гетерогенной системы называют фазой [12]. Менее строго, но более наглядно фазами называют «гомогенные части системы, отделенные от остальных частей видимыми поверхностями раздела»[7]. Примером может служить система «лёд — вода — влажный воздух». Гомогенная система содержит только одну фазу; гетерогенная система состоит из двух или более фаз[13]. Число фаз в гетерогенной системе подчиняется правилу фаз Гиббса. Одно и то же вещество в твёрдомагрегатном состоянии может иметь несколько фаз (ромбическая и моноклинная сера, серое и белое олово и др.)
Термодинамическими величинами называют физические величины, используемые для описания состояний и процессов в термодинамических системах. Термодинамика рассматривает эти величины как некоторые макроскопические параметры, присущие системе или процессу в системе, но не связывает их со свойствами системы на микроскопическом уровне рассмотрения. Это служит предметом рассмотрения в статистической физике.
Функции состояния
Функцией состояния называют любую термодинамическую величину, которая зависят только от текущего состояния системы и не зависят от того, каким путём система пришла в это состояние. В термин функция при этом вкладывают смысл, отличающийся от принятого в математике. С математической точки зрения одна и та же термодинамическая функция состояния может — в зависимости от ситуации — рассматриваться и какнезависимая переменная, и как функция других термодинамических величин, характеризующих состояние системы.
К функциям состояния относятся, например,
· температура,
· давление,
· объём,
· теплоёмкость,
· энтропия,
· термодинамические потенциалы.
Эти величины не являются независимыми. Связь между термодинамическими функциями состояния для конкретной системы задаётся уравнениями состояния.
|
|
|
|
|
Дата добавления: 2014-11-08; Просмотров: 574; Нарушение авторских прав?; Мы поможем в написании вашей работы!