
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Абсолютные значения энтропии
|
|
|
|
Постулат Планка используется при термодинамическом исследовании химических процессов для вычисления абсолютных значений энтропии химических соединений — величин, которые имеют большое значение при расчете химических равновесий.
Энтропия твердого вещества вычисляется по уравнению (II, 27):
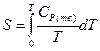 (II, 28)
(II, 28)
Для вычисления необходимо знать экспериментальные значения теплоемкости, определенные до возможно более низких температур. Значение теплоемкости до 0 К находят путем экстраполяции по уравнению Дебая, либо с помощью эмпирических приемов. Если минимальную температуру, при которой определено значение теплоемкости, обозначить Т*, то можно определить значение коэффициента a’ в уравнении Дебая, приравняв выражение для теплоемкости твердого тела по закону Т — кубов и выражение для теплоемкости в виде степенной функции (I, 17), считая, что при Т* они равны:

Принимая во внимание, что в приведенном уравнении известны все величины, кроме коэффициента a’, его легко определить. Тогда интеграл (II, 27) можно разложить на два:
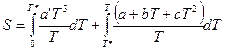
При переходе в жидкое состояние при нормальной температуре плавления энтропия возрастает на величину приведенной теплоты плавления. Нагреванию жидкости отвечает увеличение энтропии, вычисляемое по уравнению (II, 27), причем в подынтегральную функцию входит теплоемкость жидкости:
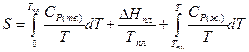 (II, 29)
(II, 29)
Испарению жидкости при постоянном давлении (например, при Р = 760 мм рт. ст.) и нагреванию газа соответствует увеличение энтропии, аналогично тому, как это имеет место при плавлении твердого тела и нагревании жидкости. Таким образом, уравнение для вычисления энтропии газа при некоторой температуре Т будет иметь вид:
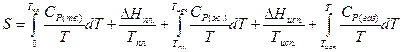 (II, 30)
(II, 30)
По этому уравнению можно вычислить энтропию идеального газа при температуре Т и 1 атм (если испарение проводилось при нормальной температуре кипения).
В том случае, когда вещество в твердом состоянии имеет не одну, а две или более модификации, в правой части уравнения (II, 28) добавятся соответствующие члены — прирост энтропии при переходе первой модификации во вторую, прирост энтропии при нагревании второй модификации и т. д.
Интегральные члены уравнений (II, 28), (II, 29) и (II, 30) можно найти графически. Для этого строят кривые СР / Т= φ (Т) или СР= φ (lnТ) и численное значение интеграла определяют по величине площади, ограниченной кривыми и осью абсцисс, заключенными между соответствующими температурами.
Величина энтропии сложным образом отражает всю совокупность свойств соединения в данном его агрегатном состоянии. Энтропия веществ зависит от молекулярной массы (увеличивается с ее ростом в ряду близких по свойствам веществ), от агрегатного состояния веществ (возрастает при переходе от твердых тел к жидким и особенно к газообразным), а также от кристаллического строения, изотопного состава и структуры молекул.
|
|
|
|
|
Дата добавления: 2014-11-29; Просмотров: 671; Нарушение авторских прав?; Мы поможем в написании вашей работы!