
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Стандартная энтропия. Изменение энтропии при протекании химической реакции
|
|
|
|
Энтропию, как и другие термодинамические функции, принято относить к стандартному состоянию вещества.
Напомним, что стандартное состояние характеризуется стандартными условиями: давлением Р0 и составом (мольная доля x0). В качестве основного стандартного состояния для всех газообразных веществ определено чистое вещество (х0 = 1) в состоянии идеального газа с давлением Р0 = 1 атм. (1,01325 · 105 Па или 760 мм рт.ст.) при любой фиксированной температуре. Для твердых и жидких веществ основное стандартное состояние — это состояние чистого вещества (х0 = 1), находящегося под внешним давлением Р 0 = 1 атм.
Это означает, что вычисление стандартной энтропии (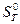 ) требует внесения поправки на изменение давления при переходе системы от состояния, характеризующегося значением энтропии
) требует внесения поправки на изменение давления при переходе системы от состояния, характеризующегося значением энтропии  и параметрами Р и Т, к состоянию Р0 и Т.
и параметрами Р и Т, к состоянию Р0 и Т.
Из уравнения (II, 21) и теоремы 1 (смотри стр.33) следует:
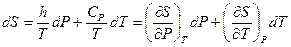 (II, 31)
(II, 31)
Следовательно, 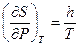 или, принимая во внимание (I, 42) и уравнение Менделеева‑Клапейрона,
или, принимая во внимание (I, 42) и уравнение Менделеева‑Клапейрона, 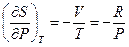
Т. к. T=const, частную производную можно заменить на полную:
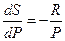 и
и  , тогда
, тогда 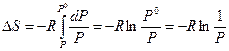
Тогда окончательно имеем:
 (II, 32)
(II, 32)
Стандартную энтропию вещества  также можно вычислить, если известна его энтропия в жидком или твердом состоянии при указанной температуре. Это делают по уравнениям:
также можно вычислить, если известна его энтропия в жидком или твердом состоянии при указанной температуре. Это делают по уравнениям:
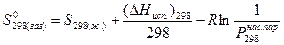
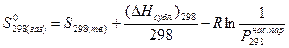 ,
,
где 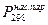 (атм) — давление насыщенных паров над веществом в жидком или твердом состоянии при 298 К, (D Hисп.)298 — теплота испарения, (D Hсубл.)298 — теплота сублимации.
(атм) — давление насыщенных паров над веществом в жидком или твердом состоянии при 298 К, (D Hисп.)298 — теплота испарения, (D Hсубл.)298 — теплота сублимации.
Известные значения стандартной энтропии веществ дают возможность вычислить  химической реакции:
химической реакции:
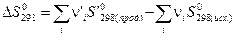
При произвольной температуре  реакции вычисляют по формуле:
реакции вычисляют по формуле:
 (II, 33)
(II, 33)
|
|
|
|
|
Дата добавления: 2014-11-29; Просмотров: 536; Нарушение авторских прав?; Мы поможем в написании вашей работы!