
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Добуток розчинності
|
|
|
|
При розчиненні твердого малорозчинного електроліту в розчин переходять не молекули, а йони. Саме тому і рівновага в насиченому розчині встановлюється між твердим електролітом і йонами, які перейшли в розчин. Наприклад, між насиченим розчином і твердим аргентум хлоридом встановлюється рівновага:
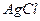 L
L 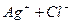
тверда фаза розчин
Константа цієї рівноваги буде:
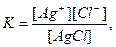 або
або 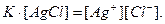
Концентрація твердого аргентум хлориду є величиною сталою. Отже, і добуток K . [AgCl] є величиною сталою. Тому при певній температурі і добуток концентрацій йонів Аргентуму і хлорид-йонів буде величиною сталою. Цей добуток концентрацій йонів в насиченому розчині електроліту називають добутком розчинності і позначають Д.Р. Для розглянутого електроліту одержимо:
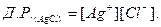
Отже, добуток розчинності будь-якого малорозчинного електроліту при певній температурі є сталою величиною, яка характеризує його розчинність.
Числове значення добутку розчинності електроліту можна обчислити, знаючи його розчинність, і навпаки. Наприклад, розчинність магній гідроксиду при 180 С дорівнює 1,7.10-4 моль/л. Це означає, що в насиченому розчині концентрація йонів Mg2+ дорівнює 1,7 .10-4 моль/л, а йонів OH- вдвічі більша, тобто 3,4 . 10-4 моль/л, тому що при розчиненні кожного моль Mg(OH)2 в розчин переходить 1 моль йонів Mg2+ і два моль йонів ОН-. Отже,
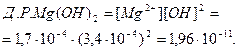
Не враховувати коефіцієнти активності і користуватись молярними концентраціями йонів можна тільки для малорозчинних електролітів через те, що коефіцієнти активності близькі до одиниці тільки в дуже розбавлених розчинах.
Для більш концентрованих розчинів замість концентрацій йонів необхідно користуватись їхніми активностями у виразі для добутку розчинності.
|
|
|
|
|
Дата добавления: 2015-05-24; Просмотров: 2863; Нарушение авторских прав?; Мы поможем в написании вашей работы!