
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Химические свойства моносахаридов
|
|
|
|
Химия углеводов основывается на двух типах функциональных групп-карбонильной (альдегидного или кетонного типа) и спиртовой гидроксильной группы.
4.1. Реакции моносахаридов по карбонильной группе
Восстановление моносахаридов приводит к образованию полигидроксиалканов, которые называются глицитами. Глицит, образующийся при восстановлении D-глюкозы и D-фруктозы (в качестве восстановителя используют боргидрид натрия), называется глюцитом или сорбитом. Сорбит используют для синтеза L-сорбозы (кетогексозы), которая служит исходным веществом для синтеза L-аскорбиновой кислоты (витамина С).
Сорбит широко распространен в растениях. Много его в плодах (яблоки, груши, сливы, вишни, абрикосы, персики). Особенно много сорбита в плодах рябины - до 7%.
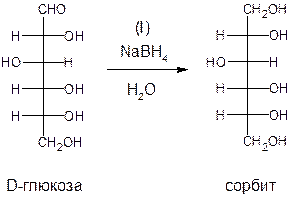
При восстановлении рибозы образуется пятиатомный спирт - рибит, участвующий в построении ферментных систем.

При восстановлении маннозы и фруктозы образуется шестиатомный спирт D- маннит. Его много в овощах и плодах (морковь, лук, оливки, ананасы), в грибах (до 11%), в водорослях (5-20%). Обычно манит получают из морской капусты. Часто он выделяется на коре некоторых деревьев в виде «манны» (оливковое дерево, некоторые виды ясеня).

D-галактоза при восстановлении образует шестиатомный спирт-дульцит:

Дульцит содержится во многих растениях и в выделениях на коре и листьях некоторых деревьев.
При окислении моносахаридов, в зависимости от природы используемых окислителей и условий реакции, образуются кислоты трех типов.
Мягкие окислители, например, бромная вода, фелингова жидкость, аммиачный раствор оксида серебра, окисляют только альдегидные группы альдоз, образуя одноосновные полигидроксикислоты, называемые альдоновыми или гликоновыми. D-Глюкоза в этих условиях окисляется до D-глюконовой кислоты (II). При одновременном окислении альдегидной и первичной спиртовой групп образуются двухосновные полигидроксикислоты, которые называются сахарными или гликаровыми. В частности, при окислении D- глюкозы азотной кислотой образуется D-глюкаровая кислота (III).

При окислении маннозы образуется манноновая, а затем манносахарная кислоты:
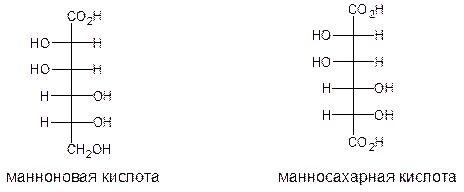
При окислении D-галактозы образуется D-галактоновая, а затем галактаровая кислоты:
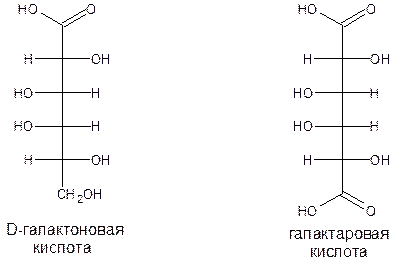
При окислении D-ксилоза образует D-ксилоновую, а затем тригидроксиглутаровую кислоту, которую используют в пищевой промышленности в качестве заменителя лимонной кислоты.
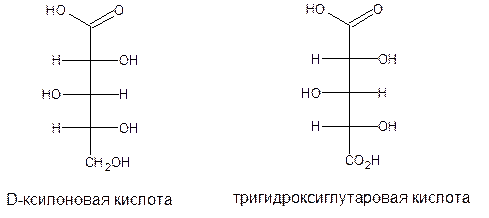
При окислении только первичной спиртовой группы у моносахаридов до карбоксильной образуются гидроксикислоты, называемые уроновыми. Названия этих кислот производятся от названий соответствующих моносахаридов путем добавления окончания «уроновая кислота». Например, D-глюкуроновая, L-гулуроновая, D-маннуроновая, 2-амино-2-дезокси-D-галактуроновая, D-галактуроновая кислоты имеют следующие формулы:

Уроновые кислоты широко распространены в природе и имеют важное биологическое значение. Среди уроновых кислот чаще всего встречается D-глюкуроновая кислота. В небольших количествах в свободном состоянии она найдена в крови, моче. Преимущественно D-глюкуроновая кислота в природе находится в связанном состоянии. Она входит в состав некоторых растительных гликозидов, растительных полисахаридов (гемицеллюлозы, камеди), мукополисахаридов (гиалуроновая кислота, гепарин, хондронтинсульфаты).
D-галактуроновая кислота встречается главным образом в пектиновых веществах.
D-маннуроновая и L-гулуроновая кислоты содержатся в полисахариде бурых водорослей – альгиновой кислоте.
При использовании тетраацетата свинца или периодата натрия, которые избирательно окисляют 1,2-диолы, происходит окислительное расщепление углеводов по схеме:

По числу молей израсходованного реагента (NaIO4 или Pb(OCOCH3 )4) и образовавшихся альдегида (формальдегида) и муравьиной кислоты возможно установление структуры углеводов.
Взаимодействие моносахаридов с цианистым водородом приводит к образованию циангидринов (IV). Эту реакцию используют для увеличения длины углеродной цепи альдоз на один углеродный атом. С этой целью, образовавшийся по реакции (IV) циангидрин, подвергают последовательно гидролизу (V), дегидратации (VI), восстановлению (VII). В результате этой серии реакций углеродная цепь увеличивается на один атом. Необходимо обратить внимание на то, что в ходе этих реакций образуются две диастереомерные альдозы, поскольку в ходе реакции IV возможно образование изомерных циангидринов.
Продуктами взаимодействия моносахаридов с гидроксиламином являются оксимы (VIII). Исходя из альдоксимов, можно отщеплением воды получить нитрилы гликоновых кислот (IX). Действуя на эти продукты солью серебра, элиминировать синильную кислоту и получить альдозу (X), содержащую на один атом углерода меньше, чем исходная.
Существует и другой способ укорачивания цепи альдоз – это деградация по Руффу, заключающийся в декарбоксилировании соли гликоновой кислоты. Углеродная цепь укорачивается при действии на указанную соль смеси пероксида водорода и соли трехвалентного железа (XI).
Моносахариды взаимодействуют с фенилгидразином, образуя озазоны. Для образования озазонов необходимо использовать избыток фенилгидразина. При малом соотношении компонентов образуются фенилгидразоны (XII). Но процесс на этом не заканчивается, а наблюдается последующая реакция окисления соседней гидроксильной группы до карбонильной, на что расходуется еще одна молекула фенилгидразина, а далее новая карбонильная группа, подобно первой, конденсируется с третьей молекулой фенилгидразина (XIII). Образующиеся озазоны хорошо кристаллизируются и поэтому используются для идентификации моносахаридов.
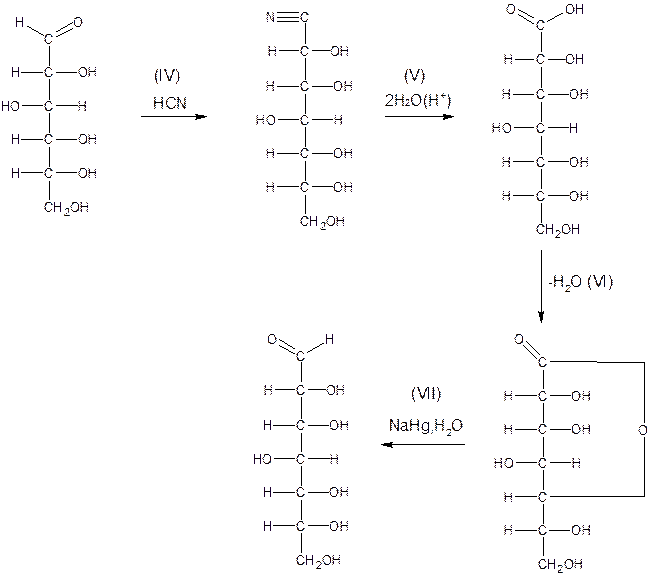
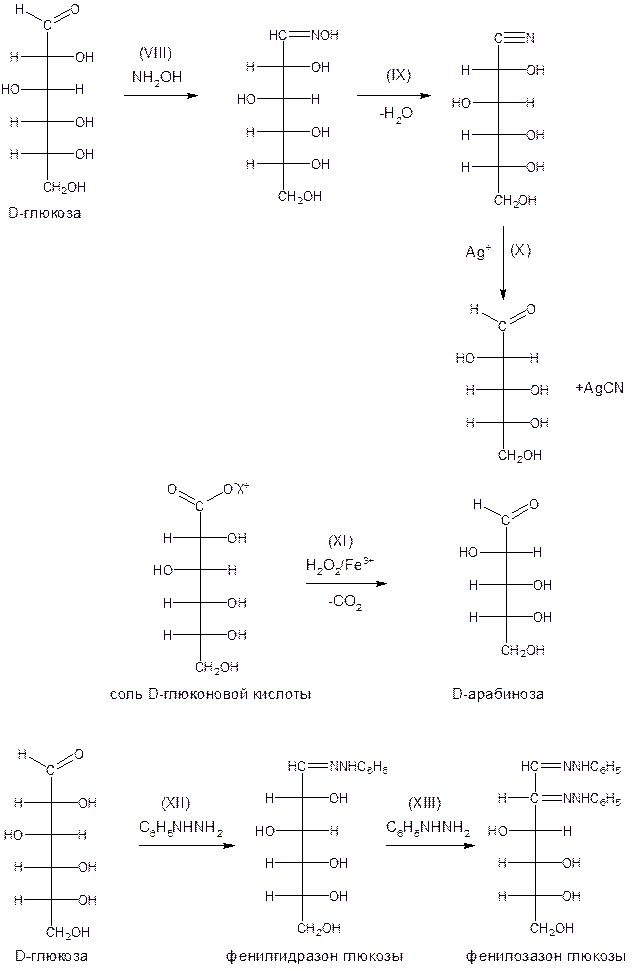
4.2 Реакции моносахаридов по спиртовой гидроксильной группе
Из типичных спиртовых свойств моносахаридов следует отметить, в первую очередь, реакции этерификации различного типа, ведущие к образованию простых алкиловых эфиров, сложных эфиров карбоновых кислот, сложных эфиров минеральных кислот. Поскольку в молекуле любого моносахарида содержится несколько спиртовых групп, то эти реакции могут иметь различную степень кратности, то есть могут быть получены, в зависимости от активности реагента, моноэфиры, диэфиры и т.д.
Гидроксильные группы сахаров могут вести себя как гидроксильные группы спиртов и поэтому сахара могут образовывать простые и сложные эфиры.
Моносахариды легко метилируются метиловым спиртом в кислой среде. В этих условиях метилированию подвергается только гидроксил, связанный в таутомерной циклической форме с бывшим карбонильным углеродом, т.е гликозидный гидроксил (реакция XIV). Соединения подобного типа, имеющие связь  , называются О-гликозидами. Этерификацию остальных гидроксильных групп проводят диметилсульфатом или йодистым метилом в щелочной среде (XV, XVI).
, называются О-гликозидами. Этерификацию остальных гидроксильных групп проводят диметилсульфатом или йодистым метилом в щелочной среде (XV, XVI).

Полуацетальный гидроксил обладает большей реакционной способностью по сравнению с остальными гидроксильными группами. Это позволило при взаимодействии с ним силиката щелочного металла получить продукт реакции – кремнийсодержащий сахарид: диглюкозо-кремниевое и дифруктозо-кремниевое соединения. Эксперименты по биологической эффективности данных кремнийсодержащих сахаридов показали, что употребление животными обогащенных кремнием кормовых рационов, сопровождается усилением активности физиологических процессов, выразившихся в увеличении массы тела.
Моносахариды могут реагировать с кислотами, образуя сложные эфиры. Особенно большое значение в живых клетках имеют сложные эфиры сахаров с фосфорной кислотой – сахарофосфаты, которые легко вступают в биохимические реакции между сахарофосфатами или с их участием. Примеры сахарофосфатов:

Наличие в молекуле углеводов спиртовых гидроксилов открывает возможность одновременного участия в реакции двух из них. Взаимодействие карбонильных соединений (ацетальдегид, ацетон, бензальдегид) с моносахаридами приводит к образованию циклических ацеталей (кеталей). Обычно в таких реакциях участвуют два цис – расположения гидроксильных групп:
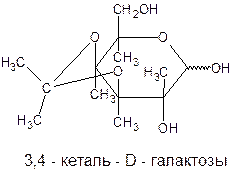
Сближение в пространстве двух гидроксильных групп моносахаридов может привести в условиях образования простых эфиров (нагревание в кислой среде) к образованию бициклических соединений, называемых ангидросахарами. Такая реакция эффективно протекает в молекуле иодозы:

Важным свойством сахаров является их способность образовывать гликозиды. Гликозиды – это соединения, которые получаются в результате реакции гликозидного гидроксила с каким – нибудь соединением (агликоном). α- и β- стереоизомеры образуют, соответственно, α- и β- гликозиды. Наиболее часто встречаются О- и N - β – гликозиды.
|
|
|
|
|
Дата добавления: 2015-07-13; Просмотров: 7134; Нарушение авторских прав?; Мы поможем в написании вашей работы!