
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Блиц – тест. Гомогенными называются такие химические реакции, в которых исходные вещества и продукты взаимодействия находятся в одной и той же фазе - газовой или жидкой
|
|
|
|
Глоссарии
Гомогенными называются такие химические реакции, в которых исходные вещества и продукты взаимодействия находятся в одной и той же фазе - газовой или жидкой, при этом молекулы, атомы, ионы взаимодействуют по всему занятому объему.
Гетерогенным и называются такие химические реакции, когда участвующие в реакции вещества (включая и катализаторы) находятся в различных фазах, а сам процесс химического превращения протекает на границе раздела этих фаз.
Диффузией - называется процесс самопроизвольнош выравнивания концентрации растворенного вещества, приводящий к установлению равномерного распределения концентраций в объеме раствора или расплава. Роль диффузии в кинетике гетерогенных процессов большая - чтобы процесс протекал с достаточной скоростыо, продукты реакции должны удаляться с поверхности раздела фаз, что также происходит путем диффузии.
|
|
|
|
|
|
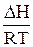 В. Kp =
В. Kp = 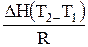 С.
С. 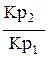 = =  D. ln
D. ln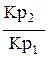 = =  E. lnKp =
E. lnKp = 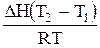
|
Литература:
- Теория металлургических процессов: учебник для вузов. Рыжонков Д.И., Арсентьев П.П., Яковлев В.В. и др. - М.: Металлургия, 1989, 392 с.
- Теория металлургических процессов: учебное пособие для вузов. Попель С.И., Сотников А.И., Бороненков В.И. М.: Металлургия, 1986. с.483
- Теория металлургических процессов. С.И. Филиппов.
М: Металлургия, 1967 – 279 с
Борнацский И.И. Теория металлургических процессов, учебное пособие. Киев, Донецк Высш.шк. 1978, 288 с.
- Казачков Е.А. Расчеты по теории металлургических процессов, Ю М., «Металлургия», 1986, 288 с.
Лекции №3 «Термодинамика и закономерности взаимодействия газов и сложных газовых атмосфер»
План лекции:
1. Механизм взаимодействия реагентов с окислителем в газовых смесях.
2. Баланс взаимодействия и образования газов.
3. Диссоциация газов на атомы и радикалы.
4. Термодинамический анализ процессов диссоциации.
5. Состав и свойства газов и низкотемпературной плазмы. Образование и диссоциация химических соединений.
6. Термодинамический анализ процессов образования и диссоциации соединений в гетерогенных системах.
7. Газообразная и конденсатная диссоциация их особенности.
Цель лекции:
Ознакомление с закономерностями взаимодействия в газовых атмосферах
|
|
|
|
|
Дата добавления: 2014-01-05; Просмотров: 510; Нарушение авторских прав?; Мы поможем в написании вашей работы!